
【题目】下列关于图像的描述错误的是( )
A.图I表示向盐酸中滴加NaAlO2溶液,沉淀质量随NaAlO2溶液体积的变化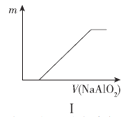
B.图II表示向NH4Al(SO4)2溶液中滴加NaOH溶液,沉淀质量随NaOH溶液体积的变化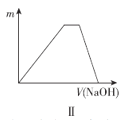
C.图III表示向NH4Cl溶液中加入稍过量Na2O2固体,产生气体的体积随Na2O2质量的变化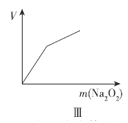
D.图IV表示向Na2CO3溶液中滴加稀盐酸,产生气体的体积随盐酸溶液体积的变化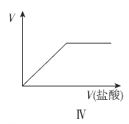
【答案】D
【解析】
A.向盐酸中滴加NaAlO2溶液,先生成AlCl3,开始一段时间内没有沉淀生成,当盐酸全部转化为AlCl3后,AlCl3与NaAlO2反应生成氢氧化铝沉淀,图象符合,故A正确;
B.向NH4Al(SO4)2溶液中滴加NaOH溶液,氢氧化钠先与铝离子反应生成氢氧化铝沉淀,然后氢氧化钠与铵根离子反应,最后氢氧化钠与氢氧化铝反应,沉淀完全溶解,图象符合,故B正确;
C.向NH4Cl溶液中加入稍过量Na2O2固体,开始一段时间内,生成氧气和氨气,气体体积增大的较快,当过氧化钠过量时,只是过氧化钠与水反应,只有氧气生成,气体的体积增大的较慢,图象符合,故C正确;
D.Na2CO3溶液中滴加稀盐酸,开始生成碳酸氢钠和NaCl,所以开始一段时间内没有气体生成,当碳酸钠全部转化为碳酸氢钠,碳酸氢钠与盐酸反应生成气体,所以一开始时没有气体生成,图象不符合,故D错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】现有X、Y、Z、T四种短周期元素,原子序数依次增大。请根据下列相关信息,回答问题。
元素 | 相关信息 |
X | 原子的1s轨道上只有1个电子 |
Y | 原子的L层上s电子数等于p电子数 |
Z | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的 |
T | 负二价的元素T的氢化物在通常情况下是一种液体,且T的质量分数为88.9% |
(1) Z2X4分子中Z原子采取________杂化,写出与之互为等电子体的有机物的结构简式_____________________
(2) Cl2T分子的空间构型___________, Z2T的电子式_________________
(3) 请用价层电子对互斥理论解释ZX![]() 和ZX3的键角∠XZX的大小:_____________。
和ZX3的键角∠XZX的大小:_____________。
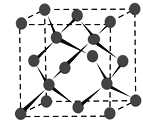
(4) Y晶体的晶胞如图所示,该晶胞含有______个Y原子,若晶胞的密度为d g·cm-3,阿伏加德罗常数的值为NA(mol-1),则晶胞参数为a=_______ pm。(用含d 、NA的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素X、Y、Z、W在周期表中的位置如图所示,其中Z元素的最外层电子数是内层电子总数的![]() 。下列说法不正确的是
。下列说法不正确的是
X | Y | |
Z | W |
A.Z元素位于周期表的第3周期第VA族
B.X、W元素的最高价氧化物对应水化物的酸性:W强于X
C.Y元素的气态氢化物的热稳定性比Z的高
D.X和Y都只能形成一种氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组同学对乙醛与新制的Cu(OH)2反应的实验进行探究。
实验Ⅰ:取2mL 10%的氢氧化钠溶液于试管中,加入5滴2%的CuSO4溶液和5滴5%的乙醛溶液,加热时蓝色悬浊液变黑,静置后未发现红色沉淀。
实验小组对影响实验Ⅰ成败的因素进行探究:
(1)探究乙醛溶液浓度对该反应的影响。
编号 | 实验Ⅱ | 实验Ⅲ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变红棕色,静置后底部有大量红色沉淀 | 加热,蓝色悬浊液变红棕色,静置后上层为棕黄色油状液体,底部有少量红色沉淀 |
已知:乙醛在碱性条件下发生缩合反应:CH3CHO+CH3CHO![]() CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
① 能证明乙醛被新制的Cu(OH)2 氧化的实验现象是______。
② 乙醛与新制的Cu(OH)2 发生反应的化学方程式是______。
③ 分析实验Ⅲ产生的红色沉淀少于实验Ⅱ的可能原因:______。
(2)探究NaOH溶液浓度对该反应的影响。
编号 | 实验Ⅳ | 实验Ⅴ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,蓝色悬浊液变红棕色, 静置后底部有红色沉淀 |
依据实验Ⅰ→Ⅴ,得出如下结论:
ⅰ. NaOH溶液浓度一定时,适当增大乙醛溶液浓度有利于生成Cu2O。
ⅱ. 乙醛溶液浓度一定时,______。
(3)探究NaOH溶液浓度与乙醛溶液浓度对该反应影响程度的差异。
编号 | 实验Ⅵ | 实验Ⅶ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,静置后底部有红色沉淀 |
由以上实验得出推论: ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
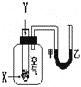
【题目】某学生用下图所示装置进行化学反应X+2Y==2Z能量变化情况的研究。当往试管中滴加试剂Y时,看到U型管中液面甲处降、乙处升。关于该反应的下列叙述:
①该反应为放热反应;
②该反应为吸热反应;
③生成物的总能量比反应物的总能量更高;
④反应物的总能量比生成物的总能量更高;
⑤该反应过程可以看成是“贮存”于X、Y内部的部分能量转化为热量而释放出来。
其中正确的是
A.①③B.①④⑤C.②③⑤D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
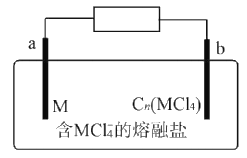
【题目】某新型二次电池反应原理为M+3Cn(MCl4)+4MC14-![]() 4M2C17-+3Cn(M代表金属,Cn代表石墨)。装置如图所示。下列说法正确的是
4M2C17-+3Cn(M代表金属,Cn代表石墨)。装置如图所示。下列说法正确的是
A. 放电时,MCl4-向b极迁移
B. 放电时,a极反应为M-3e-+7MCl4-=4M2Cl7-
C. 充电时,阳极反应式为Cn+MCl4-+e-=Cn(MCl4)
D. 电路上每转移lmol电子最多有3 mol Cn(MCl4)被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验探究CuSO4分解产物
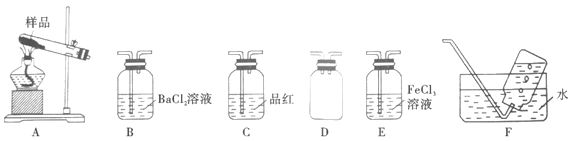
Ⅰ.甲同学选择下列装置设计实验探究硫酸铜分解的气态产物SO3、SO2和O2,并验证SO2的还原性。
回答下列有关问题
(1)CuSO4水溶液呈酸性,其原因是______________________(用离子方程式表示)。
(2)上述装置按气流从左至右排序为A、D、___________E、F(填代号)。
(3)装置D的作用是___________;能证明有SO3生成的实验现象是___________。
(4)在实验过程中C装置中红色溶液逐渐变为无色溶液,说明A中分解产物有___________;待C中有明显现象后,F开始收集气体,F装置中集气瓶收集到了少量气体,该气体是___________(填化学式)。
(5)为了验证SO2的还原性,取E装置中反应后的溶液于试管中,设计如下实验:
a 滴加少量的NH4SCN溶液 b 滴加少量的K3[Fe(CN)6]溶液
c 滴加酸性KMnO4溶液 d 滴加盐酸酸化的BaCl2溶液
其中,方案合理的有___________(填代号),写出E装置中可能发生反应的离子方程式:_________。
Ⅱ.乙同学利用A中残留固体验证固体产物(假设硫酸铜已完全分解)
查阅资料知,铜有+2、+1价。Cu2O在酸性条件下不稳定,发生反应:Cu2O+2H+=Cu+Cu2++H2O。
(6)为了验证固体产物中是否有Cu2O,设计了下列4种方案,其中能达到实验目的的是___________。
甲:取少量残留固体于试管,滴加足量的稀硝酸,观察溶液颜色是否变为蓝色
乙:取少量残留固体于试管,滴加足量的稀硫酸,观察溶液颜色是否变为蓝色
丙:取少量残留固体于试管,滴加足量的稀盐酸,观察是否有红色固体生成
丁:取少量残留固体于试管,通入氢气,加热,观察是否生成红色固体
(7)经检验CuSO4分解生成CuO、Cu2O、SO3、SO2和O2,且CuO、Cu2O的质量之比为5:9,SO2、O2、SO3的体积之比(同温同压下测定)为4:3:2。写出CuSO4分解的化学方程式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于加成反应的是
A.2C2H5+13/2O2![]() 4CO2+5H2O
4CO2+5H2O
B.CH2=CH2+H2![]() CH3CH3
CH3CH3
C.![]() +HO—NO2
+HO—NO2![]()
![]() +H2O;
+H2O;
D.2CH3COOH+Na2CO3![]() 2CH3COONa+CO2↑+H2O
2CH3COONa+CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaNO2是一种食品添加剂,过量摄入能致癌。酸性KMnO4 溶液与NaNO2反应的方程式是MnO4-+NO2-+![]() ―→Mn2++NO3-+H2O。下列叙述中正确的是
―→Mn2++NO3-+H2O。下列叙述中正确的是
A. 该反应中NO2-被还原
B. 反应过程中溶液的pH增大
C. 生成1 mol NaNO3需消耗0.2 mol KMnO4
D. ![]() 中的粒子是OH-
中的粒子是OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com