
【题目】下列离子中,所带电荷数与该离子的核外电子层数相等的是( )
A.Mg2+
B.Al3+
C.Be2+
D.H+
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】已知五种元素的原子序数的大小顺序为 C> A> B >D >E,A、C同周期,B、C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出以下元素的名称 A_________ C_________
(2)B元素在元素周期表中的位置是_______________;D2分子的结构式是______________。
(3)实验室制取D的氢化物的化学反应方程式为_________________________。
(4)用电子式表示化合物A2B的形成过程______________________。
(5)M、N均由A、B、C、E四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)在下列化合物中:H2O 、Na2O 、I2 、NaCl、KOH、CO2、NH4Cl、Na2O2,请填空:
(1)只由非金属组成的离子化合物是________________,
(2)含有极性共价键的离子化合物是________________,
(3)只含有非极性共价键的是______________________,
(4)既有离子键又有非极性键的化合物是___________________。
(Ⅱ)有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如右图所示。E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同。

请回答下列问题:
(1)写出B元素的原子结构示意图_______________________;
(2)A与氢元素能形成原子物质的量之比为1:1的化合物,其电子式为______________;
(3)向D与E形成的化合物的水溶液中滴入NaOH溶液直至过量,观察到的现象是:_______________,最后阶段反应的离子方程式为___________________;
(4)B、C、D、E的最高价氧化物的水化物的酸性从强到弱的顺序为(物质用化学式表示):___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个化学过程的示意图。
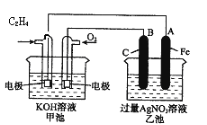
请根据该示意图完成下列题目:
(1)请问:甲池是________装置,乙池是________装置。
(2)在甲池中:通入C2H4的电极名称是___________,通入O2的电极的电极反应式是________。甲池中发生的反应的化学方程式为:________。
(3)在乙池中:B(石墨)电极的名称是________,A(Fe)电极的电极反应式为________。
(4)乙池中反应的化学方程式为________。
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2________mL(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国科学家将铅和氪两种元素的原子核对撞,获得了一种质子数为118,质量数为293的新元素,该元素原子核内的中子数和核外电子数之差为( )
A.47
B.57
C.61
D.175
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
Ⅰ.(1)实验室用金属铜和稀硝酸制取NO的离子方程式为
___________________________________________________。
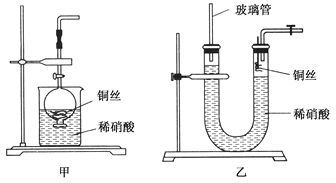
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填选项编号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是____________________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反就开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是___________________________________。
②让反应停止的操作方法及原因是________________________。
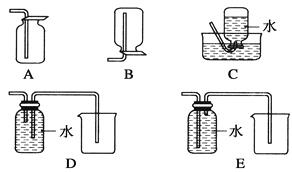
(4)以下收集NO气体的装置,合理的是________(填选项代号)。
(5)假设实验中12.8 g Cu全部溶解,需要通入标况下________mL O2才能使NO全部溶于水。
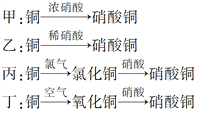
Ⅱ.用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________(填“甲”、“乙”、“丙”或“丁”),理由是___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是( )
A. 对2HI(g)![]() H2(g)+I2(g)平衡体系增加压强使颜色变深
H2(g)+I2(g)平衡体系增加压强使颜色变深
B. 反应CO(g)+NO2(g)![]() CO2(g)+NO(g)△H<0升高温度使平衡向逆方向移动[
CO2(g)+NO(g)△H<0升高温度使平衡向逆方向移动[
C. 合成氨反应:N2(g)+3H2(g)![]() 2NH3(g)△H<0,为使氨的产率提高,理论上应采取低温高压的措施
2NH3(g)△H<0,为使氨的产率提高,理论上应采取低温高压的措施
D. 在溴水中存在如下平衡:Br2(g)+H2O(l)![]() HBr(aq)+HBrO(aq),当加入NaOH溶液后颜色变浅]
HBr(aq)+HBrO(aq),当加入NaOH溶液后颜色变浅]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水溶液一定呈中性的是
A.c(NH4+)=c(C1-)的NH4Cl 溶液
B.c(H+)=1×10-7mol·L-1的溶液
C.pH=7的溶液
D.室温下将pH=3的酸与pH= 11的碱等体积混合后的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是中学化学常见物质,A、D为单质,G是含A元素的酸性气体。已知:A(s)+B(g)=C(g)+D(g) ΔH= +131.4 kJmol-1,某同学实验测知,4 g A发生上述反应吸收43.8 kJ的热量。
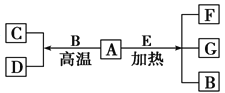
(1)写出A元素的名称________。
(2)另外知:
A(s)+O2(g)=G(g)ΔH= -393.6 kJmol-1
C(g)+ O2(g)=G(g)ΔH=-283 kJmol-1
D(g)+ O2(g)=B(g)ΔH=-242 kJmol-1由此判断“因为283 kJmol-1+242 kJmol-1>393.6 kJmol-1,所以A燃烧时加少量B可以放出更多的热量”这种说法是否正确?___________,理由是_____________________;
(3)写出A+O2→C的热化学方程式:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com