
【题目】a、b、c、d四个金属电极,有关的实验装置、部分实验现象如下:
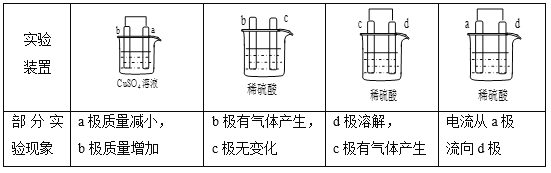
由此可判断这四种金属的活动性顺序是
A. a>b>c>d B. d>a>b>c C. b>c>d>a D. a>b>d>c
科目:高中化学 来源: 题型:
【题目】A、B、C和D是同一周期的四种元素,A、B、C的原子序数依次相差1;A元素的单质化学性质最活泼,能与水直接发生反应.B元素的氧化物2.0g恰好跟100mL0.5mol/L的H2SO4完全反应.B元素的单质跟D元素单质反应生成BD2型化合物.根据以上事实回答:
(1)A原子的结构示意图为
(2)C在周期表中的位置:
(3)BD2含有的化学键类型为
(4)A、C两元素最高价氧化物的水化物相互反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Cl2通入液复水中发生3Cl2+8NH3·H2O =6NH4Cl+N2+8H2O.下列说法正确的是
A. 浓氨水是弱电解质
B. Cl2的氧化性比N2的强
C. 向1L 0.1mol/L氨水加入盐酸至显中性,生成NH4+数为0.1×6.02×1023
D. 常温常压下,上述反应每生成2.24LN2,转移电子数为0.6×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周
期序数与族序数相等,请回答下列问题:
Q | R | ||
T | W |
(1)T的原子结构示意图为____________
(2)元素原子的得电子能力为Q____W(填“>”或“<”)。
(3)W的单质与其最高价氧化物对应的水化物浓溶液共热能发生反应,生成两种物质,其中一种是具有漂白性的气体,反应的化学方程式为
________________________________________________________________________
(4)原子序数比R多1的元素的一种氢化物在二氧化锰催化作用下易分解为它的另一种氢化物,此分解反应的化学方程式是
________________________________________________________________________
(5)将12 g Q单质在足量的氧气中燃烧,所得气体通入1 L 1.5 mol·L-1NaOH溶液中,完全吸收后,溶液中大量存在的离子有______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在10 mL浓度均为0.1 mol/LNaOH和NH3·H2O混合溶液中滴加0.1 mol/L盐酸,下列有关溶液中粒子浓度关系正确的是( )
A.未加盐酸时:c(OH-)>c(Na+)=c(NH3·H2O)
B.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
C.加入10 mL盐酸时:c(NH![]() )+c(H+)=c(OH-)
)+c(H+)=c(OH-)
D.加入20 mL盐酸时:c(Cl-)=c(NH![]() )+c(Na+)
)+c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关丙烯酸(CH2=CHCOOH)的说法正确的是
A. 丙烯酸使溴水褪色属于氧化反应
B. 丙烯酸能发生加成反应但不能发生取代反应
C. 丙烯酸分子中所有碳原子不可能处于同一平面
D. 反应 CH2=CHCOOH+H2![]() CH3CH2COOH的原子利用率为100%
CH3CH2COOH的原子利用率为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生课外活动小组利用右图所示装置分别做如下实验:

(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是_________溶液;加热时溶液由红色逐渐变浅的原因是:________________________________________。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________________溶液;加热时溶液由无色变为红色的原因是: ______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOC1)的沸点为-5.5℃,具有刺鼻恶臭味,在潮湿空气中易水解,溶于浓硫酸,是而机合成中的重要试剂。某同学用下图装置,由NO与干燥纯净的Cl2反应制备NOCl。

己知:①Cl2沸点为-34.6℃,NO2Cl沸点为-15℃
②2NO+Cl2= 2NOC1![]() 2NO2 + Cl2=2NO2C1
2NO2 + Cl2=2NO2C1
回答下列问题:
(1)铜与稀硝酸反应的化学方程式为_______________;装置A中设计了可上下移动的铜丝,其优点是_____________________。
(2)上图中实验装置的连接顺序为:a→__________________。
(3)实验时,先制取氯气使充满除A、B、C外的整套装置,目的是______________;
装置中充满氯气后,下—步是制取NO,具体操作是_______________;
E中冰盐水的温度可低至-22℃,其作用是_______________。
(4)该同学的实验设计可能的不足之处是__________________(答出一条即可)。
(5)若无C装置,则不利于NOCl的制备,主要原因是_________(用化学方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com