
【题目】下列离子方程式中正确的是( )
A. 钠与水反应: Na +2H2O![]() Na++2OH– + H2↑
Na++2OH– + H2↑
B. 向氢氧化钡溶液中加入稀硫酸: Ba2++OH–+ H++ ![]()
![]() BaSO4↓+H2O
BaSO4↓+H2O
C. 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3﹒H2O=Al(OH)3↓+3NH4+
D. 向碳酸氢铵溶液中加入足量石灰水: Ca2++![]() +OH–
+OH–![]() CaCO3↓+H2O
CaCO3↓+H2O
【答案】C
【解析】先根据所给物质的化学性质判断其反应产物,再根据离子方程式书写要求判断离子方程式是否正确。
钠与水反应生成氢氧化钠和氢气,A选项电荷不守恒,正确的是:2Na +2H2O=2Na++2OH– + H2↑,A选项错误;向氢氧化钡溶液中加入稀硫酸生成硫酸钡和水,1mol氢氧化钡电离出2mol氢氧根离子,1mol硫酸电离出2mol氢离子,反应的离子方程式:Ba2++2OH–+ 2H++SO42-=BaSO4↓+2H2O,B选项错误;氨水是弱碱,氢氧化铝溶于强碱,不溶于弱碱,向Al2(SO4)3溶液中加入过量氨水生成氢氧化铝沉淀和硫酸铵,反应的离子方程式:Al3++3NH3﹒H2O=Al(OH)3↓+3NH4+,C选项正确;向碳酸氢铵溶液中加入足量石灰水生成碳酸钙沉淀和氨气,D选项错误,正确选项C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸;在空气中迅速被氧化成绿色;见光则分解,变成褐色.如图是工业上以制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl﹣)生产CuCl的流程:
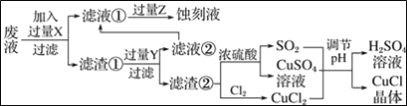
根据以上信息回答下列问题:
(1)写出生产过程中所加试剂:X_______,Y________
(2)生产中为了提高CuCl产品的质量,采用抽滤法快速过滤,析出的CuCl晶体不用水而用无水乙醇洗涤的目的是_________________;生产过程中调节溶液的pH不能过大的原因是__
(3)写出产生CuCl的化学方程式:__________________________________
(4)在CuCl的生成过程中除环境问题、安全问题外,还应该注意的关键问题是________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3S+6KOH=K2SO3+2K2S+3H2O中,被还原与被氧化的硫原子数之比为
A. 1:2 B. 2:1 C. 1:1 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是用石墨和铁作电极电解饱和食盐水的装置,请填空:
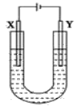
(1)X的电极名称是________极,发生的电极反应式为:_______________________。Y极的电极材料是__________,检验X极产物的方法是___________________________________________。
(2)写出该电极总反应的离子方程式:___________________________________。
(3)若食盐水为100mL 两极共放出2.24L气体(标准状况),则电路中通过电子的物质的量为___________。(假定电解后仍为100mL)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校的化学兴趣小组利用下列实验装置探究二氧化硫的性质,E中装有常见气体,与E装置相连的玻璃导管可根据需要变换长短。
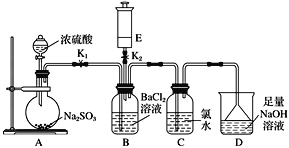
实验开始时关闭K2打开K1,从分液漏斗中向烧瓶内加入浓硫酸。
(1)A中发生反应的化学方程式是:________________________________________,B中的现象是_____________________________________。
(2)C中的现象是______________写出C中反应的化学方程式:___________________________________。
(3)D的作用是________________________,反应的离子方程式为__________________________________。
(4)A中反应完成后,关闭K1,打开K2,将E中的无色气体缓缓注入B中,有白色沉淀产生:
①若E是无色有刺激性气味气体,它的分子式为________,产生的白色沉淀是_______________(填化学式)
②若E是无色无味气体,它的分子式为________, 产生的白色沉淀是_______________(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 写出镍原子的电子排布式_____________。
(2) 丙酮(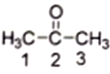 )分子中2号碳原子的杂化方式为__________;与CS2互为等电子体的阴离子是__________(写一种)。
)分子中2号碳原子的杂化方式为__________;与CS2互为等电子体的阴离子是__________(写一种)。
(3)含0.1mol[Cr(H2O)Cl]Cl2·H2O的水溶液与足量硝酸银溶液反应生成_______molAgCl沉淀。
(4)H2O分子的键角比H2S分子的键角大,原因是_______ 。
(5)N,P属于同族元素,但是它们的简单氢化物NH3,PH3在水中溶解度差异很大,其原因是 _________
(6) 由铜与氯形成的一种化合物的晶胞结构如图所示(黑点代表铜原子)。
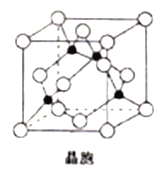
①该晶体的化学式为_______。
②将晶胞内的4个黑点相互连接所形成的立体构型是_______。
③晶体中与一个氯原子距离最近的氯原子有_______个。
④已知该晶体的密度为ρg.cm-3,阿伏加德罗常数的值为NA,则该晶体中铜原子和氯原子之间的最短距离为_______pm(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为周期表的一部分,已知A,B,C,D,E五种元素原子核外共有85个电子,E原子核外有四个电子层,B元素是( )
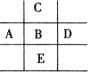
A. PB. MgC. ClD. S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,能大量共存的是
A.Fe3+、I-、Cl-、Na+B.Cl-、K+、AlO2-、OH-
C.H+、Na+、K+、CO32-D.Ba2+、Mg2+、HCO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某抗癌新药H的一种合成路线如下:
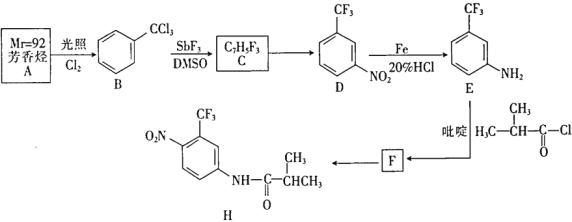
回答下列问题:
(1)A的名称是____________。
(2)B→C的反应类型是__________________。
(3)吡啶的结构简式为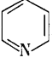 具有碱性,在E→F中吡啶的作用是_________________。
具有碱性,在E→F中吡啶的作用是_________________。
(4)写出E→F的化学方程式_____________。
(5)T(C7H7NO2)是E在碱性条件下的水解产物,同时符合下列条件的T的同分异构体有______种。
①-NH2直接连在苯环上;②能与新制氢氧化铜悬浊液共热产生红色固体
其中,在核磁共振氢谱上有4个峰且峰的面积比为1:2:2:2的结构简式为_________________。
(6)以CH3CH2COCl和![]() 为原料,经三步合成某化工产品(
为原料,经三步合成某化工产品(![]() )路线为(无机试剂任选):___________________。
)路线为(无机试剂任选):___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com