
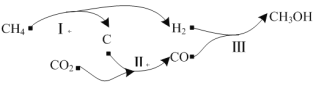
【题目】以天然气为原料经由合成气(CO、H2)制化学品是目前天然气转化利用的主导技术路线。制备CH3OH的反应转化关系如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
A.用1 mol CH4理论上能生产标准状况下CH3OH 22.4 L
B.等物质的量的CH3OH和CH4,CH3OH的质子数比CH4多8NA
C.44 g CO2气体和44 g CH4与CO的混合气体,所含C原子数均为NA
D.用CH4制备合成气的反应中,若生成1 mol CO,反应转移电子数为3NA
【答案】D
【解析】
根据图中信息可知,制备CH3OH的反应过程为:CH4(g)=C(s)+2H2(g) ,CO2(g)+C(s)=2CO (g) ,2H2(g)+CO(g)=CH3OH(l),总反应为:CH4(g)+CO2(g)=CH3OH(l)+CO(g),据此分析。
A.CH3OH在标况下不是气体,故无法得出标况下的体积是22.4 L的结论,故A错误;
B.1mol的CH3OH和CH4,一个甲醇分子含有18个质子,一个甲烷分子含有10个质子,一个甲醇分子比一个甲烷分子多8个质子,1mol的CH3OH比CH4多8NA 个质子,但等物质的量没给出具体的物质的量数值,故CH3OH的质子数不一定比CH4多8NA,故B错误;
C.44 g CO2气体的物质的量为![]() ,一氧化碳的相对分子质量为28,甲烷的相对分子质量为16,44 g CH4与CO的混合气体假设全部是CH4气体,物质的量为
,一氧化碳的相对分子质量为28,甲烷的相对分子质量为16,44 g CH4与CO的混合气体假设全部是CH4气体,物质的量为![]() >1mol,44 g CH4与CO的混合气体假设全部是CO气体,物质的量为
>1mol,44 g CH4与CO的混合气体假设全部是CO气体,物质的量为![]() >1mol,故44 g CH4与CO的混合气体的物质的量大于1mol,所含C原子数大于1mol,故C原子数大于NA,故C错误;
>1mol,故44 g CH4与CO的混合气体的物质的量大于1mol,所含C原子数大于1mol,故C原子数大于NA,故C错误;
D.制备CH3OH的反应过程中生成一氧化碳,发生反应:CO2(g)+C(s)=2CO(g),生成2mol一氧化碳时,转移2mol电子消耗1mol碳原子,消耗的碳原子来自于甲烷的分解,CH4(g)=C(s)+2H2(g) ,甲烷中碳的化合价从-4价升高到0价,生成1mol碳原子转移的电子的物质的量为4mol,要生成2mol一氧化碳共需要转移6mol电子,则若生成1 mol CO,反应转移电子的物质的量为3mol,转移的电子数为3NA;
答案选D。


科目:高中化学 来源: 题型:
【题目】咖啡酸苯乙酯可用于预防或治疗破骨细胞活性异常导致的疾病,其结构简式为![]() ,在一定条件下可以发生如下转化:
,在一定条件下可以发生如下转化:
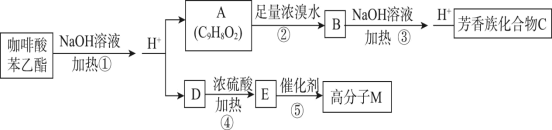
请回答以下问题:
(1)A的结构简式为________,E中官能团的结构简式为________。
(2)反应①~⑤中,属于取代反应的是________。
(3)④的化学反应方程式为_______;⑤的化学反应方程式为_______。
(4)由两分子C形成的六元环酯的结构简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g) + 3B(g) = 2C(g) + 2D(g)在四种不同情况下的反应速率分别为① v(A)=0.45 molL1s1 ② v(B)=0.6 molL1s1、③ v(C)=0.4 molL1s1、④ v(D)=0.45 molL1s1,该反应进行的快慢顺序为( )
A.① > ③ = ② > ④B.① > ② > ③ = ④
C.② > ① = ④ > ③D.① > ④ > ② = ③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃结构式如下:![]() -C≡C-CH=CH-CH3,有关其结构说法正确的是( )
-C≡C-CH=CH-CH3,有关其结构说法正确的是( )
A.所有原子可能在同一平面上B.在同一平面上的原子最多有14个
C.在同一直线上的碳原子有6个D.在同一平面上碳原子可能有11个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常利用SiO2 和碳反应来制取硅,写出反应的化学方程式___________________。
工业上还可以利用镁制取硅,反应为2Mg+SiO2 = 2MgO+Si,同时会发生副反应:2Mg + Si = Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:

(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 ___________________________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃.用化学方程式表示这两个反应①________________________②___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大 ④保持压强不变,充入N2使容器体积变大
A.①④B.②③C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ![]() 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是( )
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是( )
①N2O4的消耗速率与NO2的生成速率之比为1∶2;②NO2的生成速率与NO2消耗速率相等;③烧瓶内气体的压强不再变化;④烧瓶内气体的质量不再变化;⑤NO2的物质的量浓度不再改变;⑥烧瓶内气体的颜色不再加深;⑦烧瓶内气体的平均相对分子质量不再变化;⑧烧瓶内气体的密度不再变化。
A. ②③⑥⑦ B. ①④⑧
C. 只有①④ D. 只有⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,1mol -OH中含有9NA个电子
B.在精炼铜的过程中,当阳极有32g铜参加反应时转移电子数为NA
C.常温下,0.1mol环氧乙烷(![]() )中含有的共价键数目为0.3NA
)中含有的共价键数目为0.3NA
D.1L0.5mol/LpH=7的CH3COONH4溶液中![]() 数目为0.5NA
数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2Fe2++Cl2=2Cl﹣+2Fe3+,2Br﹣+Cl2=Br2+2Cl﹣,2Fe2++Br2=2Br﹣+2Fe3+。在bL FeBr2溶液中通入amol Cl2时,使溶液中50% 的Br﹣氧化为Br2,则原FeBr2的物质的量浓度为
A. a/bmolL﹣1 B. 2a/bmolL﹣1 C. 3a/bmolL﹣1 D. 5a/bmolL﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com