
【题目】家用炒菜铁锅用水清洗放置后会出现红棕色的锈斑,某同学欲对其原理及条件进行分析。该同学准备了下列实验用品:20%的NaCl溶液、蒸馏水、酚酞试液、KSCN溶液、新制氯水、纯铁丝、碳棒、U形管、导线等;请设计一个实验方案验证铁被腐蚀的电极产物,简述操作过程并写出溶液中有关反应的离子方程式:________
【答案】用导线连接纯铁丝和碳棒后插入盛有20%NaCl溶液的U形管中,放置一段时间后,向插入纯铁丝的一端滴入1~2滴KSCN溶液,无明显变化,再滴入新制氯水,溶液显红色,证明负极有![]() 生成,相关的离子方程式为
生成,相关的离子方程式为![]() ,
,![]() ;向插入碳棒的一端滴入酚酞试液,溶液显红色,证明有
;向插入碳棒的一端滴入酚酞试液,溶液显红色,证明有![]() 生成
生成
【解析】
为加速腐蚀,实验应选用20%的NaCl溶液作电解质溶液,以纯铁丝和碳棒作两极,分别对两极产物![]() 和
和![]() 进行检验;操作过程为:用导线连接纯铁丝和碳棒后插入盛有20%NaCl溶液的U形管中,放置一段时间后,向插入纯铁丝的一端滴入1~2滴KSCN溶液,无明显变化,再滴入新制氯水,溶液显红色,证明负极有
进行检验;操作过程为:用导线连接纯铁丝和碳棒后插入盛有20%NaCl溶液的U形管中,放置一段时间后,向插入纯铁丝的一端滴入1~2滴KSCN溶液,无明显变化,再滴入新制氯水,溶液显红色,证明负极有![]() 生成;向插入碳棒的一端滴入酚酞试液,溶液显红色,证明有
生成;向插入碳棒的一端滴入酚酞试液,溶液显红色,证明有![]() 生成;相关的离子方程式为:
生成;相关的离子方程式为:![]() ,
,![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】美托洛尔可治疗各型高血压及作血管扩张剂,它的一种合成路线如下:
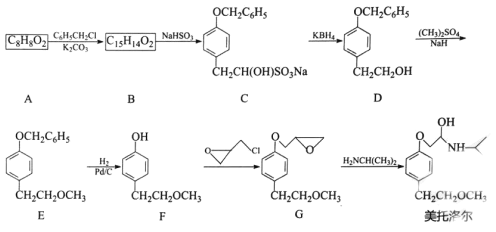
已知:![]() +
+![]()
![]()
![]() +HCl
+HCl
(1)A的化学名称是 _________,B的结构简式为__________,美托洛尔中含氧官能团的名称是_____________。
(2)A合成B的反应中,加人K2CO3的作用可能是 _________。
(3)B合成C的反应类型是________ 。
(4)F生成G的化学方程式为________ 。
(5)氯甲基环氧乙烷(![]() ) 是合成有机化合物的重要原料,实验室检验卤代烃中氯原子的常用试剂是______。
) 是合成有机化合物的重要原料,实验室检验卤代烃中氯原子的常用试剂是______。
(6)芳香族化合物M是F的同分异构体.则符合下列条件的M共有___种(不含立体异构)。
①苯环上只有2个取代基
②1molM与足量 Na 充分反应能生成1mol H2
③能与FeCl3溶液发生显色反应。
其中核磁共振氢谱为5组峰同分异构体的结构简式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国在太阳能光电催化-化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法正确的是(已知质子交换膜只允许H+通过)( )

A.该制氢工艺中光能最终转化为化学能
B.该装置工作时,H+由b极区流向a极区
C.a极上发生的电极反应为Fe3++e-=Fe2+
D.a极区需不断补充含Fe3+和Fe2+的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于溶液的说法中正确的是
A.pH=7的溶液中,Na+、NH4+、CH3COO-、NO3-可以大量共存
B.Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9,任何条件下二者不可能相互转化
C.1mol/LNa2SO4溶液中阴离子数目大于1mol/LNa2CO3溶液中阴离子数目
D.Na2S溶液与FeC13溶液混合后产生沉淀,该沉淀一定是Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究温度对反应2H2S(g)![]() 2H2(g) +S2(g)的影响,兴趣小组进行如下探究:向三个体积均为2L的恒容密团容器(A1、A2、A3)中分别加入等量的H2S,进行H2S分解实验。在T1、T2、T3,下测得H2的物质的量与时间的关系如下图所示:
2H2(g) +S2(g)的影响,兴趣小组进行如下探究:向三个体积均为2L的恒容密团容器(A1、A2、A3)中分别加入等量的H2S,进行H2S分解实验。在T1、T2、T3,下测得H2的物质的量与时间的关系如下图所示:

(1)该反应的△H____0(填“>”“<”或“=”,下同),T2、T3温度下的平衡常数K2______K3。
(2)T1温度下,前5min用S2(g)表示的反应速率为_____。
(3)图中P、Q、M三点逆反应速率由小到大的顺序是_____。
(4)已知v正=k正c2(H2S),v逆=k逆c2(H2)c(S2), 温度为T1时,k逆=3.4k正。则该温度下的化学平衡常数的值为___(保留小数点后两位数字)。
(5)在A容器中,下列选项中能标志反应2H2S(g)![]() 2H2(g) +S2(g)达到平衡的是___(填写序号)。
2H2(g) +S2(g)达到平衡的是___(填写序号)。
a v正(H2S)=2v逆(S2) b H2和S2的浓度之比为2;1
c 密度不再变化 d 平均相对分子质量不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L H2SO4溶液450 mL。根据这两种溶液的配制情况回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号)。仪器C的名称是________。本实验所需玻璃仪器E的规格和名称是________。
(2)下列操作中,容量瓶所不具备的功能有________(填序号)
A.配制一定体积准确浓度的标准溶液 B.长期贮存溶液
C.用来加热溶解固体溶质 D.量取220 mL溶液
(3)在配制NaOH溶液的实验中,其他操作均正确,若定容时仰视刻度线,则所配制溶液的浓度将________0.1 mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度将________0.1 mol/L。
(4)根据计算得知:所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为________mL(计算结果保留一位小数)。如果实验室有10 mL、25 mL、50 mL规格的量筒,应选用________mL的最好。
(5)如果定容正确的操作是_________________________。
(6)引流需要玻璃棒,其正确的放置方式_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是
A. 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B. 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C. 由氯代环己烷消去制环己烯;由丙烯加溴制![]() 二溴丙烷
二溴丙烷
D. 由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重要的农药、医药中间体-碱式氯化铜[CuaClb(OH)c·xH2O],可以通过以下步骤制备。步骤 1:将铜粉加入稀盐酸中,并持续通空气反应生成 CuCl2。已知Fe3+对该反应有催化作用,其催化原理如图所示。步骤2:在制得的CuCl2溶液中,加入石 灰乳充分反应后即可制备碱式氯化铜。下列有关说法不正确的是

A.图中M、N分别为Fe2+、Fe3+
B.a、b、c 之间的关系式为:2a=b+c
C.步骤1充分反应后,加入少量CuO是为了除去Fe3+
D.若制备1 mol的CuCl2,理论上消耗标况下11.2 LO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1.0 L恒容密闭容器中放入0.10 mol X,在一定温度下发生反应:X(g)![]() Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是 ( )
Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是 ( )
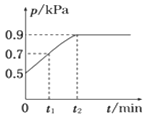
A. 该温度下此反应的平衡常数K=3.2
B. 从反应开始到t1时的平均反应速率v(X)=0.2/t1 mol·L-1·min-1
C. 欲提高平衡体系中Y的百分含量,可加入一定量的X
D. 其他条件不变,再充入0.1 mol气体X,平衡正向移动,X的转化率减少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com