
【题目】下列实验操作中选用的部分仪器,不合理的是( )
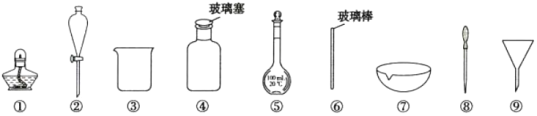
A.配制100 mL0.1 mol·L-1NaC1溶液,选用③、⑤、⑥和⑧
B.盛放NaOH溶液,选用④
C.分离I2的四氯化碳溶液和水,选用②、③
D.从食盐水中获得食盐,选用①、⑥、⑦
【答案】B
【解析】
A.配制100 mL0.1 mol·L-1NaC1溶液,要将已经准确称量的NaCl在烧杯中进行溶解,为促进物质溶解要使用玻璃棒搅拌,待溶液冷却至室温后,通过玻璃棒引流转移至已经查漏的100 mL容量瓶中,向容量瓶中加水至凹液面离刻度线1~2 cm处,用胶头滴管滴加水,直至凹液面与刻度线相切,因此需选用的仪器序号有③、⑤、⑥和⑧,A合理;
B.NaOH溶液显碱性,能够与玻璃中的SiO2发生反应产生具有粘性Na2SiO3,将玻璃瓶与玻璃塞粘在一起,因此不能使用玻璃塞,应该使用橡胶塞,B不合理;
C.I2的四氯化碳溶液和水是互不相溶的两层液体物质,应该使用分液方法分离,把下层液体用烧杯承接,因此使用仪器序号为②、③,C合理;
D.NaCl的溶解度受温度的影响变化较小,从食盐水中获得食盐,应该采用蒸发结晶方法,使用仪器有酒精灯、蒸发皿、玻璃棒,故使用仪器序号为①、⑥、⑦,D合理;
综上所述,所用仪器不合理的是B,故选B。


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】我国某科研机构设计如图装置,利用K2Cr2O7实现含苯酚废水的有效处理,一段时间后,中间室中NaCl溶液的浓度减小。下列说法正确的是( )
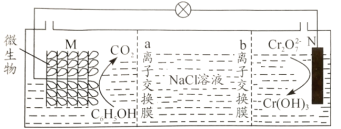
A.M为该电池的正极
B.该装置在高温下处理含苯酚废水效果更佳
C.a为阳离子交换膜,b为阴离子交换膜
D.N电极反应式为:Cr2O![]() +6e-+8H+=2Cr(OH)3↓+H2O
+6e-+8H+=2Cr(OH)3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)![]() 3C(g)+4D(g)中,表示该反应速率最快的是:
3C(g)+4D(g)中,表示该反应速率最快的是:
A.V(A)=0.5mol·L-1·s-1B.V(B)=0.3mol·L-1·s-1
C.V(C)=0.8mol·L-1·s-1D.V(D)=1mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X(g)+3Y(g) ![]() 2Z(g) ΔH=-a kJ·molˉ1 ,一定条件下,将1 mol X和3 mol Y通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4 mol。下列说法正确的是( )
2Z(g) ΔH=-a kJ·molˉ1 ,一定条件下,将1 mol X和3 mol Y通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4 mol。下列说法正确的是( )
A.10min内,消耗0.2 mol X,生成0.4 mol Z
B.第10min时,X的反应速率为0.01 mol·Lˉ1·minˉ1
C.10min内,Y的平均反应速率为0.03 mol·Lˉ1·sˉ1
D.10min内,X和Y反应放出的热量为a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列变化进行推断:
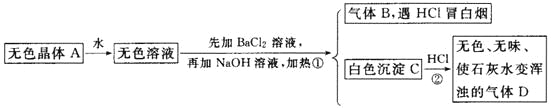
且已知对A加强热产生的气态物质的平均相对分子质量为26.3。
(1)推断A、B、C、D的化学式:A________,B________,C________,D________。
(2)写出①②变化的离子方程式:
①________________________________________________________________;
②________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为14,中子数为7;X的离子与NH4+具有相同的质子、电子数目;W与Y的氧化物均能导致酸雨的形成;Z的非金属性在同周期主族元素中最强。
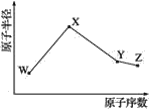
(1)Y在周期表中的位置是__。
(2)X3W遇水可释放出使酚酞溶液变红的气体A,化学方程式是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在生产生活中有着广泛的应用。请回答下列问题:
(1)铜元素位于元素周期表中_____区,基态Cu原子有______种不同能级的电子。
(2)铜合金可用于制造航母螺旋桨。制造过程中产生的含铜废液可利用铜萃取剂M,通过如下反应实现铜离子的富集回收。
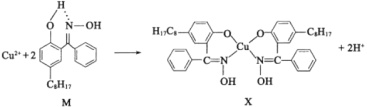
①M所含元素的电负性由大到小的顺序为______(用元素符号表示)。
②X中采用sp3杂化的非金属原子有______(填元素名称)。
(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体Y产生。Y分子的立体构型是_______,Y的沸点比水低的主要原因是_______。
(4)向蓝色{[Cu(H2O)4]2+}硫酸铜溶液中加入稍过量的氨水,溶液变为深蓝色{[Cu(NH3)4]2+}。通过上述实验现象可知,与Cu2+的配位能力:H2O________NH3(填“大于”或“小于”)。
(5)CuCl2和CuCl是铜的两种氯化物。
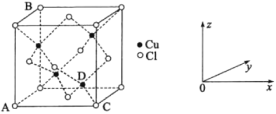
①图中表示的是_______(填“CuCl2”或“CuCl”)的晶胞。
②原子坐标参数可用来表示晶胞内各原子的相对位置,图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,0,0);则D原子的坐标参数为______。
③晶胞中C、D两原子核间距为298 pm,阿伏加德罗常数的值为NA,则该晶体密度为__g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨的催化氧化是制硝酸的主要反应之一,其微观示意图如下。下列说法正确的是( )

A.甲的化学式为NH3 , 其水溶液呈碱性B.该反应中元素的化合价都发生改变
C.该反应中甲、乙的质量比为17 :32D.生成物丙、丁的分子个数比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com