
【题目】某无色溶液里只含有下列7种离子中的某几种:Mg2+ 、H+ 、Ag+ 、Na+ 、Cl- 、HCO3- 、OH- 。已知:该溶液能跟金属铝反应,且放出氢气。试回答:
(1)若铝跟溶液反应后只有AlO2-生成,则原溶液一定含有的大量离子是_______ ,发生该反应的离子方程式是__________;还可能含有离子是__________。
(2)若铝跟溶液反应后只有Al3+生成,则原溶液中一定不能大量含有的离子是_____。
【答案】Na+、OH- 2Al+2OH-+2H2O![]() 2AlO2-+3H2↑ Cl- HCO3- 、OH- 、Ag+
2AlO2-+3H2↑ Cl- HCO3- 、OH- 、Ag+
【解析】
跟金属铝反应生成H2的溶液可能为酸溶液,也可能为碱溶液,当生成Al3+时,溶液为酸溶液,当生成AlO2-时,溶液为碱溶液,然后利用离子的共存来分析,并注意离子在水中的颜色。
离子均为无色,所有离子均与无色透明溶液符合;铝既能与酸作用产生氢气,也能与碱作用产生氢气。
(1)溶液和铝粉反应后有AlO2-生成,离子反应方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,溶液显碱性时,Mg2+、H+、Ag+、HCO3-不能存在,根据溶液不显电性,一定存在阳离子,即阳离子只有Na+,说明原溶液中的阴离子一定含OH-,可能含Cl-,
故答案为:Na+、OH-;2Al+2OH-+2H2O=2AlO2-+3H2↑;Cl-。
(2)溶液和铝粉反应后有Al3+生成,离子反应方程式为:2Al+6H+=2Al3++3H2↑,溶液显酸性,则HCO3-、OH-不存在,根据溶液不显电性,一定存在阴离子,即溶液中肯定有Cl-,而Ag+可与Cl-生成沉淀,说明原溶液中也不存在Ag+,即溶液中一定含有大量的H+、Cl-,可能含Na+、Mg2+,一定不能含有:Ag+、OH-、HCO3-,
故答案为:Ag+、OH-、HCO3-。


 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
【题目】某同学组装了如图所示的电化学装置。电极I为Al,其他电极均为Cu,则( )

A. 电极I发生还原反应 B. 电极II逐渐溶解
C. 电流方向:电极IV―→![]() ―→电极I D. 电极III的电极反应:Cu2++2e-=Cu
―→电极I D. 电极III的电极反应:Cu2++2e-=Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1mol·L1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是
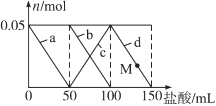
A. a曲线表示的离子方程式为:AlO2-+H++H2O===Al(OH)3↓
B. b和c曲线表示的离子反应是相同的
C. M点时,溶液中沉淀的质量为3.9g
D. 原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是 ( )
A. 澄清石灰水与过量苏打溶液混合:Ca2++2OH-+2HCO3-=CaCO3↓ +CO32-+2H2O
B. 用惰性电极电解NaHS溶液:HS-+ H2O![]() S↓+H2↑+OH-
S↓+H2↑+OH-
C. 向摩尔盐溶液中加入过量的Ba(OH)2溶液:2NH4+ + Fe2+ + 2SO42- + 2Ba2+ + 4OH- = 2BaSO4↓+ Fe(OH)2↓+ 2NH3·H2O
D. 明矾溶液中加入Ba(OH)2溶液至生成的沉淀质量最多:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铜片放入0.1mol·L-1FeCl3溶液中,反应一段时间后取出铜片,溶液中![]() ,则反应后溶液中
,则反应后溶液中![]() 与
与![]() 的物质的量之比为 ( )
的物质的量之比为 ( )
A. 3:2 B. 3:4 C. 3:5 D. 4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置可用于二氧化锰与浓盐酸在加热条件下制取相应的产物,并利用产物进行后续实验,请填写下列空白:

(1)写出二氧化锰与浓盐酸反应的化学方程式_____________________。
(2)洗气瓶B中放有饱和食盐水、洗气瓶C是为了干燥所制得的气体,在洗气瓶D中放有石灰乳,则B装置的作用是:_________;C瓶中盛装的试剂是______ ;D瓶中发生的化学反应方程式是__________ ,工业上据此反应原理制备__________。
(3)在A装置的反应中参加反应的氧化剂与还原剂物质的量之比为:_______。
(4)若反应中制得的气体标准状况下体积为8.96L,则参与氧化还原反应的还原剂的物质的量是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油裂解气主要含有丙烯、1,3-丁二烯等不饱和烃,以它们为原料可合成CR橡胶和医药中间体G,,合成路线如下:

已知:①B、C、D 均能发生银镜反应;
②
(1)A的顺式异构体的结构简式为___________________。
(2)C中含氧官能团的名称是____________,反应①的反应类型为____________________。
(3)写出E→ 反应的化学方程式:_________________________________。
(4)写出同时满足下列条件的医药中间体G的同分异构体的结构简式: __________________。
①与D 互为同系物; ②核磁共振氢谱有三组峰。
(5)用简要语言表述检验B中所含官能团的实验方法:_______________________。
(6)以A为起始原料合成CR橡胶的线路为______________________(其它试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫、钴及其相关化合物用途非常广泛。回答下列问题:
(1)基态Co原子价电子轨道排布式为________,第四电离能I4(Co)<I4(Fe),其原因是_______;Co与Ca同周期且最外层电子数相同,单质钴的熔沸点均比钙大,其原因是_______.
(2)单质硫与熟石灰加热产物之一为CaS3,S32-的几何形状是_______,中心原子杂化方式是_______,与其互为等电子体的分子是_______ (举1例)。
(3)K和Na位于同主族,K2S的熔点为840℃,Na2S的熔点为950℃,前者熔点较低的原因是_______ 。
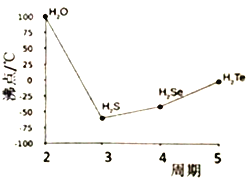
(4)S与O、Se、Te位于同一主族,它们的氢化物的沸点如右图所示,沸点按图像所示变为的原因是_______ 。
(5)钴的一种化合物晶胞结构如下图所示。

①已知A点的原子坐标参数为为(0,0,0),B点为(![]() ,0,
,0,![]() ),则C点的原子坐标参数为_____。
),则C点的原子坐标参数为_____。
②已知晶胞参数为a=0.5485nm,则该晶体的密度为_____g/cm3(列出计算表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两种物质:

(1)乙中含有的官能团的名称为__________________(不包括苯环)。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
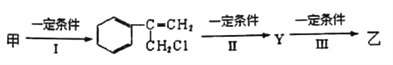
反应I的化学其中反应I的反应类型是____________________,反应II的条件是________,反应III的化学方程式为_________________(不需注明反应条件)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com