
| A、摩尔是七个物理量之一 |
| B、摩尔是物质的质量单位 |
| C、1mol水中含有1mol氧和2mol氢 |
| D、0.5mol NaOH中含有Na+为0.5NA |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、啤酒开启后泛起大量泡沫 |
| B、实验室中常用排饱和食盐水的方法收集氯气 |
| C、将食物放在冰箱里延长保质期 |
| D、工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
| B、2mol | ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(N2)=0.40mol?L-1?s-1 |
| B、v(H2)=0.80mol?L-1?s-1 |
| C、v(NH3)=0.60mol?L-1?s-1 |
| D、v(NH3)=1.20mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸和硬脂酸互为同系物,C2H6和C9H20也互为同系物 |
| B、氨基酸是人体必需的营养物质,其晶体主要以内盐形式存在,调节溶液的pH可改变它的溶解度 |
| C、丙氨酸和苯丙氨酸脱水,最多可生成3种二肽 |
| D、向鸡蛋清溶液中加入饱和(NH4)2SO4溶液,有沉淀析出,再加水沉淀会溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ClO2在反应中是氧化产物 |
| B、NaClO3在反应中失去电子 |
| C、H2SO4在反应中作氧化剂 |
| D、1mol氧化剂在反应中得到1mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
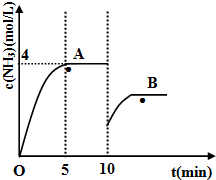 运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.| 压强/MPa转化率/%温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
| 7 |
| 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com