
反应A(g)+B(g) 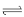 C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
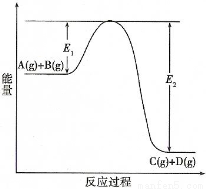
(1)该反应是____________________反应(填“吸热”、“放热”);
(2)当反应达到平衡时,升高温度,A的转化率______(填“增大”、“减小”或“不变”),原因是___________________________________________________________________;
(3)反应体系中加入催化剂对反应热是否有影响?________,原因是__________________________________________________________________________________________;
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2 ________(填“增大”、“减小”或“不变”)。
科目:高中化学 来源:2014-2015学年广东省第一学期高一第一次月考化学试卷(解析版) 题型:选择题
将30mL 0.5 mol/LNaOH溶液加水稀释到500 mL,稀释后溶液中NaOH的物质的量浓度为()
A.0.03 mol/L B.0.3 mol/L C.0.05 mol/L D.0.04 mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东东莞市高二上学期第一次月考化学试卷(解析版) 题型:选择题
已知反应:①101 kPa时,2C(s)+O2(g)====2CO(g);ΔH=-221 kJ·mol-1②稀溶液中,H+(aq)+OH-(aq)=H2O(l);ΔH=-57.3 kJ·mol-1。下列结论正确的是 ( )
A.碳的燃烧热大于110.5 kJ·mol-1
B.①的反应热为221 kJ·mol-1
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高一上学期第一次考试化学试卷(解析版) 题型:选择题
在一定温度和压强下,1体积X2气体与3体积Y2气体化合生成2体积
某气体,则该气体的化学式为 ( )
A.XY3 B.XY C.X3Y D.X2Y3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高一上学期第一次考试化学试卷(解析版) 题型:选择题
2004年2月22日是第35个“世界地球日”,我国确定的主题是“善待地球——科学发展”。下列行为中不符合这一主题的是( )
A.采用“绿色化学”工艺,使原料尽可能转化为所需要的物质
B.减少直至不使用对大气臭氧层起破坏作用的氟氯烃
C.大量开采地下水,以满足社会对水的需求
D.节约能源,提高能源利用率
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二10月月考化学试卷(解析版) 题型:选择题
如图表示反应2 SO2(g)+O2(g) 2 SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是
2 SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是

A.t1时减小了SO2 的浓度,增加了SO3的浓度,平衡向逆反应方向移动
B.t1时降低了温度,平衡向正反应方向移动
C.t1时减小了压强,平衡向逆反应方向移动
D.t1时增加了SO2 和O2的浓度,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二10月月考化学试卷(解析版) 题型:选择题
反应2A(g) 2B(g)+E(g)△H>0达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是
2B(g)+E(g)△H>0达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是
A.加压 B.减压 C.减少E的浓度 D.降温
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西大学附中第一学期高二化学试卷(解析版) 题型:选择题
下列化合物跟溴和铁粉反应,氢原子被取代,所得一溴代物C8H9Br有二种同分异构体的是
A.  B.
B. C.
C.  D.
D.
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊三县市高一上学期联考化学试卷(解析版) 题型:填空题
(12分)某无色溶液中可能含有Na+、Ba2+、Cu2+、CO32-、Cl-、Mg2+中的一种或几种离子。
①向此溶液中滴加足量稀盐酸无明显现象。
②取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入足量的NaOH溶液,有白色沉淀产生。
(1)原溶液中一定含有的离子是________,一定不含有的离子是________,不能确定是否含有的离子是________。
(2)②中反应的离子方程式为 。
(3)若另取10mL①的溶液于锥形瓶中,然后向此溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示。

①OA段反应的离子方程式为 。
②AB段反应的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com