
����Ŀ������������
��1����ҵ����FeCl3��Һ��ʴͭ����·�壬 ��ӦΪCu+2FeCl3=CuCl2+2FeCl2���ݴ�������ԭ��Ӧ����Ƴ�ԭ��أ��ָ���������ͭ����ʯī�缫��ԭ��صĸ���Ϊ �� �����缫��Ӧ����ʽ �� ����������6.4�ˣ����·��ת�Ƶ��ӵ����ʵ���Ϊ ��
��2����һ�ܱյ�2L��������װ��4mol SO2��2mol O2 �� ��һ�������¿�ʼ��Ӧ��2minĩ��������й���5.6mol ���壬�Լ��㣺 ��i��2minĩSO3��Ũ�� ��
��ii����SO2��ʾ�÷�Ӧ��ƽ����Ӧ���� ��
���𰸡�
��1��Cu��Fe3++e��=Fe2+��0.2mol
��2��0.4mol/L��0.2mol/��L��min��
���������⣺��1���ɷ�Ӧ��2FeCl3+Cu=2FeCl2+CuCl2����֪����Ӧ��ͭʧ���Ӷ���������ӦΪԭ��ظ���������ӦΪ�����Ա�ͭ���Ľ�����ķǽ������ϣ���ʯī�缫Ϊ������Fe3+�������õ����Ӷ�����ԭ����缫��ӦΪ��2Fe3++2e��=2Fe2+ �� �������ҺΪFeCl3 �� ���·�е��ӴӸ����������ƶ�������������6.4�ˣ����ܽ��Cu�����ʵ���Ϊ ![]() =0.1mol����ת�Ƶĵ���Ϊ0.2mol ���Դ��ǣ�Cu��2Fe3++2e��=2Fe2+��0.2mol��
=0.1mol����ת�Ƶĵ���Ϊ0.2mol ���Դ��ǣ�Cu��2Fe3++2e��=2Fe2+��0.2mol��
����2��������������
2SO2+ | O2 | = | 2SO3 | |
��ʼ����mol�� | 4 | 2 | 0 | |
��Ӧ����mol�� | 2x | x | 2x | |
ƽ������mol�� | 4��2x | 2��x | 2x |
4��2x+2��x+2x=5.6��
x=0.4mol��
2minĩ��n��SO3��=0.8mol��c= ![]() =
= ![]() =0.4mol/L��
=0.4mol/L��
v= ![]() =
= ![]() =
= ![]() =0.2molL��1min1 ��
=0.2molL��1min1 ��
���Դ��ǣ�0.4mol/L��0.2molL��1min1 ��
�����㾫����������Ĺؼ��������⻯ѧƽ��ļ�������֪ʶ�����շ�Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���һ�������¼��ܷ���������Ӧ�����ܷ���ˮ���������Ӧ���ǣ� ��
A.��������
B.������
C.�������
D.����ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���� ( )
A.ʯ���ѽ⡢ʯ�ͷ���ú�ĸ����ǻ�ѧ�仯
B.��װ�ò��Ͼ���ϩ�;�����ϩ��������
C.��һ�������£�����Һ�塢�������������屽��������������ȡ����Ӧ
D.���ͼױ��������ڷ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����(Rb)��������ȷ����
A. ��λ�����ڱ��ĵ������ڡ��ڢ�A��B. ���ơ��ء��3�ֵ����У�卑��۵����
C. �������������D. ����������ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.���Ĵ�������һ������Ĺ̵���ʽ
B.��ҵұ�������������AlCl3����
C.�����ۼ���FeCl3��CuCl2�����Һ�У���ַ�Ӧ��ʣ��Ĺ����в�һ������
D.�ü��ȷֽ�ķ����ɽ�NH4Cl�����Ca��OH��2����Ļ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ͼ��ʾʵ�飬��ȷ��ij��������к���C2H4��SO2 �� ������壬�����Լ��У�
A��Ʒ����Һ B��NaOH��Һ
C��ŨH2SO4 D�����Ը��������Һ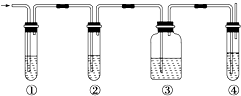
�Իش��������⣺
��1��д��ͼ�Т١��ڡ��ۡ���װ�ÿ�ʢ�ŵ��Լ����������й��Լ����������ո��ڣ��� �� �� �� �� �� �� �� ��
��2��ʹ��װ�âڵ�Ŀ���� ��
��3��д��SO2�����Ը�����ط�Ӧ�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̪��������ŵ�����֣�����ҩ��ҵԭ�ϣ���ṹ��ͼ��ʾ���йط�̪˵������ȷ���ǣ� �� 
A.����ʽΪC20H14O4
B.���Է���ȡ����Ӧ���ӳɷ�Ӧ��������Ӧ
C.���еĹ��������ǻ�������
D.1mol�����ʿ���H2����ˮ������Ӧ������H2��Br2�����ֵΪ10mol��4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���Ƚϣ�����ȷ���ǣ� ��
A.���ȶ��ԣ�HBr��HCl
B.���ԣ�Al��OH��3��Mg��OH��2
C.�����ԣ�O��F
D.��ԭ�ԣ�S2����O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4NH3��g��+5O2��g�� ![]() 4NO+6H2O��2L���ܱ������н��У�30s��NO�����ʵ���������0.30mol������˵����ȷ���ǣ� ��
4NO+6H2O��2L���ܱ������н��У�30s��NO�����ʵ���������0.30mol������˵����ȷ���ǣ� ��
A.������NH3�����ʵ���һ��������0.30mol
B.������H2O��g�������ʵ�������Ϊ0.45mol
C.NH3��ƽ����Ӧ����Ϊ0.010mol/��Ls��
D.NH3��O2��NO��H2O�����ʵ���֮��һ��Ϊ4��5��4��6
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com