
����Ŀ���״����ַdz���Ҫ�Ļ���ԭ�ϣ���ҵ��CO2 ��������ȼ�ϼ״������ܻ�������ЧӦ��ҲΪ�״��ĺϳ�Ѱ������������
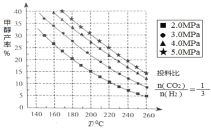
(1)�״��ĺϳɣ��ϳɼ״��ķ�ӦΪ��CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H ���ڴ��������£���ü״��IJ����뷴Ӧ�¶ȡ�ѹǿ��ϵ����ͼ��ʾ�� ��ͼ�����ݿ�֪����H______0(ѡ ��������������������)���״���������ѹǿ�仯����ͼʾ���ɵ�ԭ����_______��
(2)�״���Ӧ�ã���Ȳ�������һ����Ҫ���л�����ԭ�ϣ�������ˮ�����³�Һ̬���е�Ϊ 103~105 �档ʵ���ҿ��ü״�����һ�л�ԭ�� M ��һ���������Ʊ���ʵ�鲽�����£�
���� 1���ڷ�Ӧƿ�У����� 13 g ԭ�� M��50 mL �״��� 2 mL Ũ���ᣬ���裬���Ȼ���һ��ʱ�䡣
���� 2�����������ļ״�(װ�ü���ͼ)��
���� 3����ӦҺ��ȴ�������ñ��� NaCl ��Һ�� 5%Na2CO3 ��Һ��ˮϴ�ӣ�������л��ࡣ
���� 4���л��ྭ��ˮ Na2SO4 ������ˡ����� �ñ�Ȳ�������

�ٲ��� 1 �з�Ӧ�Ļ�ѧ����ʽ��_____________��
�ڲ��� 1 �У���������״���Ŀ����_____________��
�۲��� 3 �� Na2CO3 ��Һϴ����Ҫȥ����������______���ò����в��õ�����Ũ�ȵ�NaOH ��Һ����Na2CO3 ��Һϴ����Ҫԭ����___________��
���𰸡��� ����Ӧ���������ʵ�����С�ķ�Ӧ������ѹǿ��ƽ�������ƣ���ˣ�����������ͬʱ��ѹǿԽ�״��IJ���Խ�� HC��CCOOH+CH3OH![]() HC��CCOOCH3+H2O ��� M��ת���� ��Ȳ�ᣨ���л�ԭ�ϣ� NaOH ����ǿ��ʹ��ˮ��̶������������
HC��CCOOCH3+H2O ��� M��ת���� ��Ȳ�ᣨ���л�ԭ�ϣ� NaOH ����ǿ��ʹ��ˮ��̶������������
��������
(2)�÷�Ӧ�DZ�Ȳ��ͼ״���������Ӧ���״�������Ϊ�������һ����Ӧ���Ȳ���ת���ʣ�����Na2CO3 ��Һ��Ϊ�˳�ȥ��Ȳ�ᣬ����NaOH��Һ����Ϊ����̫ǿ���ᵼ������ˮ�⣬���Ͳ��ʡ�
(1)��ͼ�������״��IJ������¶�����С��˵��ƽ��������У������¶ȣ�ƽ�������ȵķ����ƶ���˵���淴Ӧ���ȣ�������Ӧ�Ƿ��ȷ�Ӧ����H<0���״���������ѹǿ������������ԭ���ǣ�����Ӧ���������ʵ�����С�ķ�Ӧ������ѹǿ��ƽ�������ƣ���ˣ�����������ͬʱ��ѹǿԽ�״��IJ���Խ�ߣ�
(2)�ٲ���1�DZ�Ȳ��ͼ״���������Ӧ����Ӧ��ѧ����ʽ��HC��CCOOH+CH3OH![]() HC��CCOOCH3+H2O��
HC��CCOOCH3+H2O��
��������ӦΪ���淴Ӧ���״������������ڱ�Ȳ���ת������������ʣ��ʴ�Ϊ����� M��ת���ʣ�
�۱�Ȳ��������ԣ�����̼������Һ��Ӧ������뱥��̼������Һ�ɳ�ȥ��Ȳ�ᣬ���ɵı�Ȳ�����������ˮ����Һ�ֲ㣬���÷�Һ�ķ������룻
���õ�����Ũ�ȵ�NaOH ��Һ����Na2CO3 ��Һϴ����Ҫԭ���ǣ�NaOH ����ǿ��ʹ��ˮ��̶�����������ʣ��ʴ�Ϊ����Ȳ�NaOH ����ǿ��ʹ��ˮ��̶�����������ʡ�


 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д� �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��10 ������NaHCO3������Һ����ø���Һ��pH�������µı仯��
�¶�(��) | 10 | 20 | 30 | ������к���ȴ��50 �� |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
(1)��ͬѧ��Ϊ������Һ��pH���ߵ�ԭ����HCO3-��ˮ��̶����ʼ�����ǿ����ˮ�ⷴӦ�����ӷ���ʽΪ______________��
(2)��ͬѧ��Ϊ����ҺpH���ߵ�ԭ����NaHCO3���ȷֽ⣬������Na2CO3�����ƶ�Na2CO3��ˮ��̶�________(��������������С����)NaHCO3���÷ֽⷴӦ�Ļ�ѧ����ʽΪ____��
(3)��ͬѧ��Ϊ�ס��ҵ��ж϶�����֡�����Ϊ��
��ֻҪ�ڼ�����е���Һ�м����������Լ�BaCl2��Һ�������������������ж���ȷ��ԭ����____________��д����Ӧ�����ӷ���ʽ�����ܲ���ѡ��Ba(OH)2��Һ��______(������������������)��
�������Ⱥ����Һ��ȴ��10 ��������Һ��pH________(������������С��������������)8.3����________(����������������)�ж���ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о���ͬ pH ʱ CuSO4 ��Һ�� H2O2 �ֽ�Ĵ����á����ϣ�a��Cu2O Ϊ��ɫ���壬������ˮ�����������ᣬ���� Cu ��Cu2+��b��CuO2 Ϊ�غ�ɫ���壬������ˮ�����������ᣬ���� Cu2+�� H2O2��c��H2O2 �������ԣ�H2O2 ![]() H+ +HO2-��HO2-
H+ +HO2-��HO2- ![]() H+ +O22-��
H+ +O22-��
��� | ʵ�� | ���� |
�� | �� 1 mL pH��2 �� 1 mol��L 1 CuSO4��Һ�м��� 0.5 mL 30% H2O2 ��Һ | ������������ |
�� | �� 1 mL pH��3 �� 1 mol��L 1 CuSO4��Һ�м��� 0.5 mL 30% H2O2 ��Һ | �������������ػ�ɫ���������ֽ��������� |
�� | �� 1 mL pH��5 �� 1 mol��L 1CuSO4��Һ�м��� 0.5 mL 30% H2O2 ��Һ | �������������غ�ɫ������������������ |
��1�� ���������ɵ������Ϊ O2������ CuSO4 ���ֽ� H2O2 �Ļ�ѧ����ʽ��__��
��2���Ԣ����غ�ɫ�����ijɷ���� 2 �ּ��裺��.CuO2����.Cu2O ��CuO2 �Ļ���Ϊ�����������裬����ʵ��������ˢ��еij�����ϴ�ӣ�����������ᣬ������ȫ�ܽ⣬��Һ����ɫ���������������ݡ�
�����������ɵij���Ϊ CuO2���䷴Ӧ�����ӷ���ʽ��__��
�����ݢ��г�����ȫ�ܽ⣬��ͬѧ��Ϊ���袢����������ͬѧ��ͬ���ͬѧ�Ĺ۵㣬������__��
��Ϊ̽���������Ƿ���� Cu2O���������ʵ�飺
�����г���ϴ�ӡ������ȡ a g �������ڹ���ϡ���ᣬ��ּ��ȡ���ȴ�������Һ pH���� PAN Ϊָʾ��������Һ�еμ� c mol��L 1EDTA ��Һ���ζ��յ㣬���� EDTA ��Һ V mL��V=__����֪�����в��� Cu2O�����袡����������֪��Cu2++EDTA= EDTA-Cu2+��M(CuO2)��96 g��mol 1��M(Cu2O)��144 g��mol1��
��3����Ϸ���ʽ�����û�ѧ��Ӧԭ�����͢������ɵij������ڢ��е�ԭ��__ ��
��4���о����в�ͬ pH ʱ H2O2 �ֽ����ʲ�ͬ��ԭ��
ʵ��������Թ��зֱ�ȡ 1 mL pH��2��3��5 �� 1 mol��L1 Na2SO4 ��Һ�������и����� 0.5 mL 30% H2O2 ��Һ����֧�Թ��о�����������
ʵ�����__����ʵ�����������˵�� CuO2 �ܹ��� H2O2 �ֽ⡣
��5���ۺ�����ʵ�飬���в�ͬ pH ʱ H2O2 �ķֽ����ʲ�ͬ��ԭ����__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������к��зḻ�ĵ�Ԫ��(��I��ʽ����)��ʵ��������ȡ����������£�

��1��ʵ���������������________��������Ҫ��������Ϊ________��
��2����ȡ��Ĺ����У��ɹ�ѡ����л��Լ���________(�����)��
A���ƾ�(�е�78 ��) B�����Ȼ�̼(�е�77 ��)
C������(�е�290 ��) D����(�е�80 ��)
��3���ڲ������У���Һ����������ICl(ICl����������������)��Ϊ���������ʣ�ʹ��ȫ�����������Ӧ��������________(�����)��Һ����Ӧ�����ӷ���ʽ___________________��
A��KIO3 B��HClO C��KI D��Br2
��4�����õ���л���Һ�õ�����I2�ķ�����_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ž��з���Ԫ��������150���ꡣ�±���Ԫ�����ڱ���һ���֣�W��X��Y��ZΪ����������Ԫ�أ�W��X������ϼ�֮��Ϊ8������˵����������
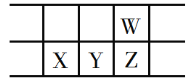
A.ԭ�Ӱ뾶��Y>W
B.Yԭ��ͨ����ʧ���Ӷ������ף�������Ȼ���У�YԪ�ز���������̬
C.��ͼ��⻯��ķе㣺W<Z
D.X������������ˮ����������ᷴӦ������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��ͬѧ̽����ʵ������![]() ����ĸ������ء�
����ĸ������ء�
(1)������Һ���Ƿ���![]() ʱ���ù������Ὣ��Һ�ữ����Ŀ�����ų�_______________��
ʱ���ù������Ὣ��Һ�ữ����Ŀ�����ų�_______________��![]() ��Ag+�����ӿ�����ɵĸ��š�
��Ag+�����ӿ�����ɵĸ��š�
(2)Ϊ����֤�����ܷ��ų�![]() �ĸ��ţ���С��ͬѧ����������ʵ�飺
�ĸ��ţ���С��ͬѧ����������ʵ�飺
������ȡһ�������Ũ����(ʢ��Ũ�����Լ�ƿ�ı�ǩ�в�����Ϣ����ͼ)��ϡ�ͣ����Ƴ� 5 mol/L ��ϡ���ᡣ

��ͬѧȡ 0.3 g δ���ʵ� Na2SO3 ���壬�����м������� 5mol/L ϡ�����������������������ݡ������μ� 4 ��BaCl2 ��Һ��Ѹ�ٲ�����ɫ���ǣ�������ɫ���ǵ�ԭ������ǣ�
��______________��
�������к��� Fe3+��ʵ��֤ʵ���� Fe3+�ķ����ǣ�___________________�������ӷ���ʽ������ Fe3+������ɫ���ǵ�ԭ��__________��
(3)��ͬѧ���������![]() ʱ�ܷ��������ữ���ų�
ʱ�ܷ��������ữ���ų�![]() �ĸ��ţ���ͬѧ��Ϊ�����У�������(�����ӷ���ʽ��ʾ)____________________________������ʵ�飺��ȡ 5 �� 0.3 g δ���ʵ�Na2SO3 ���壬�ֱ������м��� 10 mL ��ͬŨ�ȵ����ᣬ ���ٵμ� 4 ��BaCl2 ��Һ���۲첢��¼ʵ���������±���
�ĸ��ţ���ͬѧ��Ϊ�����У�������(�����ӷ���ʽ��ʾ)____________________________������ʵ�飺��ȡ 5 �� 0.3 g δ���ʵ�Na2SO3 ���壬�ֱ������м��� 10 mL ��ͬŨ�ȵ����ᣬ ���ٵμ� 4 ��BaCl2 ��Һ���۲첢��¼ʵ���������±���
����Ũ��(mol/L) | �μ��Ȼ�����Һ֮ǰ���� | �μ��Ȼ�����Һ֮������ |
15.0(Ũ����) | ������������ɫ���壬��Һ�ʻ�ɫ | ��������������ɫ���� |
7.5 | ������������ɫ���壬��Һ�ʵ���ɫ | ��������������ɫ���� |
4.8 | ����������ɫ���̼�����ζ���壬��Һ��ɫ | ��ʼ������Լ 60 min ����Һ��ʼ����� |
2.0 | ����������ɫ���̼�����ζ���壬��Һ��ɫ | ��ʼ������Լ 70 min ����Һ��ʼ����� |
0.5 | ����������ɫ���̼�����ζ���壬��Һ��ɫ | ��ʼ������Լ 120 min ����Һ��ʼ����� |
��������ʵ��ó��Ľ����ǣ�________________��
(4)��ͬѧ�������Ϻ������Cl-�Ĵ���Ҳ���![]() �ļ���������š��� Cl-�������£�ϡ����ɽ�
�ļ���������š��� Cl-�������£�ϡ����ɽ�![]() ����Ϊ
����Ϊ ![]() ��Ϊ֤�������۵㣬�������ʵ�飬�뽫ʵ�颢�IJ�������������
��Ϊ֤�������۵㣬�������ʵ�飬�뽫ʵ�颢�IJ�������������
ʵ�� | ʵ����� | ʵ������ |
�� | �� 0.3 g Na2SO3 �� 0.3 g NaCl �����ϣ����� 10 mL 2.0mol/L ��ϡ���ᣬ���ٵμ� 4 �� BaCl2 ��Һ�� | ��������������ɫ������ |
�� | ____________�� | ������Сʱ����Һδ����ǡ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��ķ�Ӧԭ������Ӧ�����ӷ���ʽ����ȷ����
A.�����²���Ȼ����ҺpH<7��֤��һˮ�ϰ������NH4+��H2O![]() NH3��H2O��H��
NH3��H2O��H��
B.������������Һ��ȥþ���е���������2Al��2OH��=2AlO2-��H2��
C.��Ũ�����ữ��KMnO4��Һ��H2O2��Ӧ��֤��H2O2���л�ԭ�ԣ�2MnO4-��6H����5H2O2=2Mn2����5O2����8H2O
D.�����Ը�����ر���Һ�ζ����2MnO4-��16H����5C2O42-=2Mn2����10CO2����8H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������зḻ����ʳƷ���������Դ��ҩ���ˮ����Դ���ȣ�����˵����ȷ����

A.�������г�ȥ��ɳ��Ca2+��Mg2+������ʱ�����漰��ѧ�仯����
B.��ҵ�ϣ�ͨ�������������ˮ��Һ������ȡ������
C.�������ķ�Ӧ���������ڿ�����ֱ�Ӽ�����
D.���������������о��漰������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڲ�ͬ����²��A(g)��3B(g)![]() 2C(g)��2D(s)�����з�Ӧ���ʣ����з�Ӧ����������
2C(g)��2D(s)�����з�Ӧ���ʣ����з�Ӧ����������
A.v(D)=0.8molL-1s-1B.v(C)=0.010 molL-1s-1
C.v(B)=0.6 molL-1min-1D.v(A)=0.2molL-1min-1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com