
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是
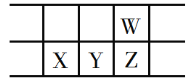
A.原子半径:Y>W
B.Y原子通常得失电子都不容易,但在自然界中,Y元素不存在游离态
C.最低价氢化物的沸点:W<Z
D.X的最高价氧化物的水化物既能与酸反应又能与碱反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列三组实验进行一段时间后,溶液中均有白色沉淀生成,下列结论不正确的是
实验① | 实验② | 实验③ |
2mL1mol/LBaCl2溶液 4mL1mol/LNaHCO3溶液 | 2mL1mol/LBaCl2溶液 4mL1mol/LNa2SO3溶液 | 2mL1mol/LBaCl2溶液 4mLH2SO3溶液 |
A.实验①中生成的沉淀是BaCO3
B.实验①中有气体生成
C.实验②沉淀中可能含有BaSO4
D.实验③生成沉淀的离子方程式是:Ba2++H2SO3=BaSO3↓+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解的知识叙述中,错误的是
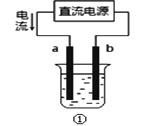
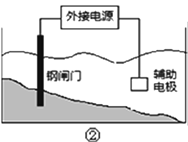
A.用装置①精炼铜,则a极为粗铜,电解质溶液可为CuSO4溶液
B.工业上通过电解氯化钠溶液的方法制备金属钠
C.装置②的钢闸门应与外接电源的负极相连
D.向电子元件上镀上一层银,常需要电子元件做阴极,金属银作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象预测正确的是
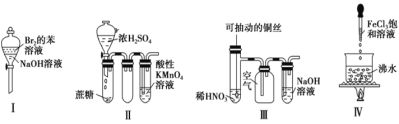
① 实验Ⅰ:振荡后静置,上层溶液颜色保持不变
② 实验Ⅱ:酸性 KMnO4 溶液中出现气泡,且颜色逐渐褪去
③ 实验Ⅲ:微热稀 HNO3 片刻,溶液中有气泡产生,广口瓶内始终保持无色
④ 实验Ⅳ:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
A.①②B.③④C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向 10mL 0.01 mol/L NaCN 溶液中逐滴滴加 10mL0.01 mol/L 的盐酸,其 pH 变化曲线如图所示。下列溶液中的关系一定正确的是(忽略体积微小变化)
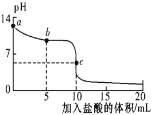
A.a 点溶液的 pH ≥12
B.b 点的溶液:c(CN-)> c(Cl-)>c(HCN )
C.pH =7 的溶液:c(Na+)+ c(H+) =c(Cl-)+ c(CN-)
D.c 点的溶液:c(CN-)+c(HCN ) +c(Cl-)=0.01 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是种非常重要的化工原料,工业上CO2 用于生产燃料甲醇,既能缓解温室效应,也为甲醇的合成寻找了新渠道。
(1)甲醇的合成:合成甲醇的反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H ;在催化剂作用下,测得甲醇的产率与反应温度、压强关系如下图所示, 由图中数据可知,△H______0(选 填“>”“<”“=”),甲醇产率随着压强变化呈现图示规律的原因是_______。
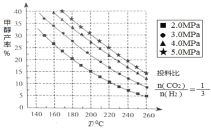
(2)甲醇的应用:丙炔酸甲酯是一种重要的有机化工原料,不溶于水,常温呈液态,沸点为 103~105 ℃。实验室可用甲醇和另一有机原料 M 在一定条件下制备,实验步骤如下:
步骤 1:在反应瓶中,加入 13 g 原料 M、50 mL 甲醇和 2 mL 浓硫酸,搅拌,加热回流一段时间。
步骤 2:蒸出过量的甲醇(装置见下图)。
步骤 3:反应液冷却后,依次用饱和 NaCl 溶液、 5%Na2CO3 溶液、水洗涤;分离出有机相。
步骤 4:有机相经无水 Na2SO4 干燥、过滤、蒸馏, 得丙炔酸甲酯。

①步骤 1 中反应的化学方程式是_____________。
②步骤 1 中,加入过量甲醇的目的是_____________。
③步骤 3 中 Na2CO3 溶液洗涤主要去除的物质是______。该步骤中不用等量等浓度的NaOH 溶液代替Na2CO3 溶液洗涤主要原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,将C12缓慢通入100 mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1 mol·L-1 NaOH溶液,整个过程溶液中H+的浓度变化如图所示。(已知常温常压下C12溶于水时,只有部分C12会和水发生反应)下列叙述正确的是

A. ①处溶液的酸性比②处溶液的酸性强
B. 依据②处c(H+)可计算溶解的C12的物质的量
C. 整个实验过程中,溶液的颜色先变深后变浅,最后变为无色
D. ④处表示C12与NaOH溶液恰好完全反应,共转移了0.1mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种白色晶体A极易溶于水,将A配成溶液进行如下框图所示的实验,实验现象及转化关系如下列框图所示。A为含硫氮正盐其中硫元素化合价为+4,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝。试回答下列问题:

(1)写出下列物质化学式:D:__________;F:__________。
(2)写出下列反应的离子方程式:
①A和酸性KMnO4溶液反应__________;
②D和新制氯水:__________。
(3)通过本题的解答,在检验SO42-时,应使用__________。
A.盐酸酸化的BaCl2溶液 B.硝酸酸化的Ba(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如下图所示,对该反应的推断合理的是( )

A. 该反应的化学方程式为3B+4D![]() 6A+2C
6A+2C
B. 反应进行到1 s时,v(A)=v(D)
C. 反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D. 反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com