
| V |
| Vm |
| m(HCl) |
| m(HCl)+m(水) |
| 1000ρw |
| M |
| 224L |
| 22.4L?mol-1 |
| 365g |
| 365g+635g |
| 1000ρw |
| M |
| 1000×1.18×36.5% |
| 36.5 |


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
| A、NF3是氧化剂,H2O是还原剂 |
| B、NF3是极性分子,在干燥空气中泄漏会看到红棕色气体 |
| C、若生成1mol HNO3,转移2NA个电子 |
| D、每消耗0.02mol氧化剂,可收集到2.24L气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池工作时,正极和负极上不一定都发生氧化还原反应 | |||
B、xLi+Li1-xNiO2
| |||
| C、在铅、银和盐酸构成的原电池工作时,铅板上有5.175 g铅溶解,正极上就有1120 mL(标准状况)气体析出 | |||
| D、在理论上可将该反应:CH4(g)+2O2(g)→CO2(g)+H2O(l)△H<0,设计成原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol?L-1HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示.
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol?L-1HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
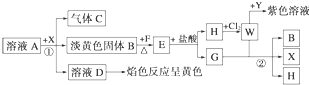
查看答案和解析>>
科目:高中化学 来源: 题型:
 研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素.
短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素.查看答案和解析>>
科目:高中化学 来源: 题型:

- 4 |
- 2 |
 ═□Mn2++□NO
═□Mn2++□NO- 3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com