
【题目】表是25℃时某些弱酸的电离平衡常数,下列说法正确的是( )
化学式 | CH3COOH | HClO | H2CO3 |
Ka | 1.8×10﹣5 | 3.0×10﹣8 | Ka1=4.1×10﹣7Ka2=5.6×10﹣11 |
A. 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是:c(Na+)>c(ClO﹣)>c(CH3COO﹣)>c(OH﹣)>c(H+)
B. 向0.1mol·L﹣1CH3COOH溶液中滴加NaOH溶液至溶液pH=5,此时:c(CH3COOH):c(CH3COO﹣)=9:5
C. 少量碳酸氢钠固体加入到新制的氯水中,c(HClO)增大
D. 等体积等物质的量浓度的CH3COONa(aq)与NaClO(aq)中离子总数大小:N前<N后
【答案】C
【解析】A.醋酸的电离常数大于次氯酸,所以醋酸钠的水解程度小于次氯酸钠,醋酸钠和次氯酸钠都是强碱弱酸盐,其混合溶液呈碱性,所以相同物质的量浓度的CH3COONa和NaClO的混合液中,各离子浓度的大小关系是:c(Na+)>c(CH3COO-)>c(ClO-)>c(OH-)>c(H+),故A错误;B.CH3COOH的电离常数为1.8×10-5,向0.1molL-1CH3COOH溶液中滴加NaOH溶液至溶液pH=5,则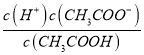 =1.8×10-5,c(CH3COOH):c(CH3COO-)=10-5:1.8×10-5=5:9,故B错误;C.氯水中存在Cl2+H2OH++Cl-+HClO,少量碳酸氢钠固体加入到新制的氯水中,碳酸氢钠只与盐酸反应,则平衡正向移动,c(HClO)增大,故C正确;D.HClO酸性较弱,NaClO水解程度较大,根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-)、c(Na+)+c(H+)=c(OH-)+c(ClO-),由于NaClO水解程度较大,溶液中氢离子浓度较小,且两溶液钠离子浓度相等,所以CH3COONa溶液中离子总数大于NaClO溶液,即N前>N后,故D错误;故选C。
=1.8×10-5,c(CH3COOH):c(CH3COO-)=10-5:1.8×10-5=5:9,故B错误;C.氯水中存在Cl2+H2OH++Cl-+HClO,少量碳酸氢钠固体加入到新制的氯水中,碳酸氢钠只与盐酸反应,则平衡正向移动,c(HClO)增大,故C正确;D.HClO酸性较弱,NaClO水解程度较大,根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-)、c(Na+)+c(H+)=c(OH-)+c(ClO-),由于NaClO水解程度较大,溶液中氢离子浓度较小,且两溶液钠离子浓度相等,所以CH3COONa溶液中离子总数大于NaClO溶液,即N前>N后,故D错误;故选C。


科目:高中化学 来源: 题型:
【题目】有机物的性质与其结构有着密切关系。苯有如下性质:
①苯与溴的四氯化碳溶液不反应;
②苯与酸性高锰酸钾溶液不反应;
③1mol苯在一定条件下可与3mol氢气发生加成反应
由此推断苯分子中6个碳原子之间的键是( )
A. 一种典型的单键
B. 一种典型的双键
C. 一种介于单键和双键之间独特的键
D. 极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述正确的是( )
A. 煤的干馏和石油的分馏均属于化学变化
B. 蛋白质和蔗糖都属于高分子化合物,一定条件下都能水解
C. 乙烯的产量是衡量一个国家的石油化工发展水平的标志
D. 淀粉与纤维素互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将190 g MgCl2溶于水配制成1 L溶液。
(1)该溶液中MgCl2的物质的量浓度为________,溶液中Cl的物质的量浓度为________。
(2)配制1 mol/L的MgCl2溶液500 mL,需该溶液的体积为________。
(3)向(2)中500 mL溶液中再通入一定量的HCl气体后,溶液中Cl的浓度为3 mol·L1(假设溶液体积不变),则溶液中H+的物质的量浓度为_____, 通入HCl气体的体积(标况下)为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂方式正确的是
A. CO2气体中含有的少量杂质SO2可通过饱和Na2CO3溶液除去
B. NaOH溶液中含有少量的Ba(OH)2可加入适量的Na2SO4过滤除去
C. K2CO3固体中含有少量的NaHCO3杂质可用加热的方式提纯
D. Cu粉中含有的少量杂质Fe可加入FeCl3溶液除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组通过灼烧法测定CuxSy的组成,并验证气体产物SO2的部分性质,设计实验如下(夹持装置略去):
I.测定CuxSy的组成

步骤一:用上图所示装置高温灼烧16.0gCuxSy至固体质量不再变化,停止加热,继续通入O2至硬质玻璃管冷却。
步骤二:向装置D所得溶液中加入足量双氧水,再加入过量BaCl2溶液;将生成的沉淀过滤、洗涤、干燥、称量得沉淀质量为23.3 g。
(1)装置C中用于加热的仪器名称为___________________。
(2)步骤一中,停止加热后,继续通入O2的主要作用为___________________。
(3)由实验数据推断得CuxSy的化学式为___________________。
(4)若无装置E,则所测x∶y的值 ________(填“偏大”“ 偏小”或“无影响”)。.
Ⅱ.该小组选用实验I中的装置A、B、C和下图所示装置,依次验证SO2的漂白性,氧化性和还原性。

(5)按气流方向,装置的合理连接顺序为A→B→C→______________(填装置字母)。
(6)试剂X的名称为_____________。能证明SO2有还原性的实验现象为______________。
(7)装置G中发生反应的离子方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向100 mL一定浓度的草酸(H2C2O4)溶液中加入0.1mol·L-1NaOH 溶液,溶液的pH随NaOH溶液体积的变化曲线如图所示。下列有关说法正确的是

A. a点溶液的pH=2,草酸溶液的浓度为0.005 mol ·L-1
B. b点对应溶液中:c(Na+)>c(HC2O4-)>c(OH-)>c(C2O42-)
C. b→c段,反应的离子方程式为HC2O4- +OH-=C2O42-+H2O
D. c→d段,溶液中C2O42-的水解程度逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500 mL含有MgCl2、NaCl、Na2SO4三种物质的混合溶液,已知其中含有Cl为1.8 mol,Na+为2 mol,Mg2+为0.5 mol,则![]() 的物质的量浓度为
的物质的量浓度为
A.0.6 mol /L B.0.7 mol /L C.1.2 mol /L D.1.0 mol /L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com