
����Ŀ����190 g MgCl2����ˮ���Ƴ�1 L��Һ��
��1������Һ��MgCl2�����ʵ���Ũ��Ϊ________����Һ��Cl�����ʵ���Ũ��Ϊ________��
��2������1 mol/L��MgCl2��Һ500 mL�������Һ�����Ϊ________��
��3������2����500 mL��Һ����ͨ��һ������HCl�������Һ��Cl��Ũ��Ϊ3 mol��L1��������Һ���������������Һ��H+�����ʵ���Ũ��Ϊ_____�� ͨ��HCl�����������������Ϊ_____��
���𰸡���1��2 mol/L 4 mol/L
��2��250 mL
��3��1 mol/L 11.2 L
����������1��n(MgCl2)=![]() =2 mol��c(MgCl2)=
=2 mol��c(MgCl2)=![]() =2 mol/L��c(Cl)=2c(MgCl2)=4 mol/L��
=2 mol/L��c(Cl)=2c(MgCl2)=4 mol/L��
��2������ϡ������c(Ũ)��V(Ũ)=c(ϡ)��V(ϡ)����2 mol/L��V(Ũ)=1 mol/L��500 mL������V(Ũ)=250 mL��
��3�����ݵ���غ���c(H+)+2c(Mg2+)=c(Cl)����c(H+)+2��1 mol/L=3 mol/L������c(H+)=1 mol/L��n(HCl)=1 mol/L��0.5 L=0.5 mol��V(HCl)=0.5 mol��22.4 L/mol=11.2 L��


 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֺ�ɫ��ĩ����ͭ�������������������̡�ʯī�ۣ�ֻ�����һ���Լ����ɽ������������� �����Լ���(����)
A. ����������Һ B. ϡ����
C. Ũ���� D. ����ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڹ����˵����ȷ����(����)
A. ������һ�ֲ�����ˮ�ĺ����� B. �������ˮ����һ�ַǵ����
C. ��������Ա�̼��ǿ D. ������ɶ���������ˮ��Ӧ�Ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NO��NO2 ��CO��Ϊ������Ⱦ������������ܹ�ע����ش��������⣺
I����Һ���շ�
��1��NaOH��Һ�ɽ�NO��NO2�Ļ������ת��ΪNaNO2���÷�Ӧ�����ӷ���ʽΪ_________________________________________��
��2��25��ʱ��HNO2�ĵ��볣��Ka=4.6��10-4�������£���NaNO2��Һ�еμ���������Һ��pH=3ʱ����Һ��![]() =_________��������λ��Ч���֣�
=_________��������λ��Ч���֣�
��.��֪�ۺ�����NO��CO��ԭ��Ϊ
i. 2NO(g)+2CO(g)![]() N2(g)+2CO2 (g) ��H=-746.5kJmol-1
N2(g)+2CO2 (g) ��H=-746.5kJmol-1
ii. C(s)+ 2NO(g)![]() N2(g)+ CO2 (g) ��H= +172.5 kJmol-1
N2(g)+ CO2 (g) ��H= +172.5 kJmol-1
��3�������£�1mol C(s)��CO2 ��ȫ��Ӧ����CO���Ȼ�ѧ����ʽΪ________________________��
��4��һ�������£�ij�ܱ������з�����Ӧi�ͷ�Ӧii���ﵽƽ��������������䣬�����¶ȣ�CO���������_______������� ��С������Ӱ�족����
��5��һ�������£������ܱ������з�����Ӧi������ʼ�����![]() =y��NO��ƽ��ת����(a)��y���¶ȣ�T���Ĺ�ϵ��ͼ��ʾ��
=y��NO��ƽ��ת����(a)��y���¶ȣ�T���Ĺ�ϵ��ͼ��ʾ��

��y1_____y2���>����<����=����
��M���N���Ӧ�ĸ÷�Ӧ���ʣ�M_________N���>����<����=����
��6��t��ʱ�����ݻ�Ϊ10L�ĺ�ѹ�ܱ������м���1mol C(s)��2molNO(g)��������Ӧii��5min�ﵽƽ��ʱ�����0��5min�ڣ���CO2��ʾ�ĸ÷�Ӧ����v(CO2)=0.016 molL-1��min-1��N2���������Ϊa����
��t��ʱ���÷�Ӧ��ƽ�ⳣ��K=_____________��
���������������䣬��ʼ��������а�������ȼ������ʣ��ﵽƽ��ʱ��N2�����������Ϊa����____________________����ѡ����ĸ��
A.0.5molC��2mol NO B.2mol N2��2mol CO2
C.1 mol C��1 mol N2��1mol CO2 D.1 mol C��1 mol NO��1mol N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���мס��ҡ���������Һ���������²�����
![]()
��ס��ҡ���������Һ�е����ʿ����ֱ���
A��BaCl2��H2SO4��MgCl2 B��CaCl2��HNO3��AgNO3
C��CaCl2��HNO3��NaCl D��BaCl2��HCl��Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������25��ʱijЩ����ĵ���ƽ�ⳣ��������˵����ȷ���ǣ� ��
��ѧʽ | CH3COOH | HClO | H2CO3 |
Ka | 1.8��10��5 | 3.0��10��8 | Ka1=4.1��10��7Ka2=5.6��10��11 |
A. ��ͬŨ��CH3COONa��NaClO�Ļ��Һ�У�������Ũ�ȵĴ�С��ϵ�ǣ�c��Na+����c��ClO������c��CH3COO������c��OH������c��H+��
B. ��0.1mol��L��1CH3COOH��Һ�еμ�NaOH��Һ����ҺpH=5����ʱ��c��CH3COOH����c��CH3COO����=9��5
C. ����̼�����ƹ�����뵽���Ƶ���ˮ�У�c��HClO������
D. ����������ʵ���Ũ�ȵ�CH3COONa��aq����NaClO��aq��������������С��Nǰ��N��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��Na��O�γɵ�һ��ֻ�������Ӽ������ӻ�����ľ����ṹ������ͼ����һ����������Χ���������������Ϊ���㹹�ɵļ�����Ϊ____________��
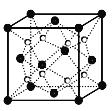
��2��ij���Ӿ��徧���ṹ��ͼ��ʾ��X(![]() )λ��������Ķ��㣬Y(��)λ������������ġ��Է�����
)λ��������Ķ��㣬Y(��)λ������������ġ��Է�����
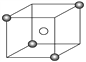
�پ�����ÿ��Yͬʱ����____��X��
�ڸþ���Ļ�ѧʽΪ_____��
����þ����Ħ������ΪM g��mol-1��������ܶ�Ϊ��g��cm-3�������ӵ�������ֵΪNA���������������������X֮��ľ���Ϊ_________nm���ú�M������NA��ʽ�ӱ�ʾ���룩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����������ת��
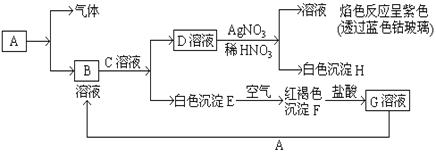
��1��Aת��ΪB�������ⲽ��Ӧ��Ӧ������Լ���_______�������ƣ���
��2��д��B�Ļ�ѧʽ_______ D�Ļ�ѧʽ_______
��3��д����Eת���F�Ļ�ѧ����ʽ_____________________________
��4��д����G��Һ�м���A���й����ӷ�Ӧ����ʽ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijŨH2SO4 �ܶ�1.84 g/mL�����ʵ���Ũ��Ϊ18.4 mol/L����������Ϊ98%��ȡ10 mLŨH2SO4��a mLˮ��ϵ����ʵ���Ũ��Ϊc mol/L����������Ϊb%�����������ȷ����
(1)��c=9.2����a>10 b>49
(2)��c=9.2����a>10 b��49
(3)��b=49����a=18.4 c��9.2
(4)��b=49����a=18.4 c>9.2
A��(1)(3) B��(1)(4) C��(2)(3) D��(2)(4)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com