
将一定量的铁片和浓硫酸混合加热,充分应后得到溶液X,X中除Fe3+外还可能含有Fe2+。若要确认其中的Fe2+,应选用( )
| A.KSCN溶液和氯水 | B.铁粉和KSCN溶液 |
| C.浓氨水 | D.酸性KMnO4溶液 |
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:实验题
(7分)海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
(1)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_____________________。
(2)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_________________,
由此反应可知,除环境保护外,在工业生产中应解决的主要问题是: _________________。
(3)兰州一中某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:
请你参与分析讨论:
①图中仪器B的名称是__________。
②实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件? ____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
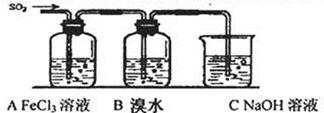
硫及其化合物有广泛的应用,对SO2性质的研究是高中化学教学的一项重要内容。
I.对比研究是一种重要的研究方法。若将硫的单质及部分化合物按如下表所示分成3 组,则第2组中物质M的化学式是 。
| 第1组 | 第2组 | 第3组 |
| S (单质) | SO2、H2SO3、M、NaHSO3 | SO3、H2SO4、Na2SO4、 NaHSO4 |
| n(SO32—):n(HSO3—) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
| 序号 | 实验方案 | 实验现象 | 结论 |
| 方案① | 往第一份试液中加入KMnO4溶液溶液 | 紫红色褪去 | SO2与Fe3+反应生成了Fe2+ |
| 方案② | 往第二份试液中加入 | | SO2与Fe3+反应生成了Fe2+ |
| 方案③ | 往第二份试液中加入 | | SO2与Fe3+反应生成了SO42— |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示,甲、乙、丙、丁分别代表Na2CO3、NaOH、NaHCO3、CO2四种物质,a、b、c、d、e、f分别表示两种物质间的转化关系。对于图中两种物质间的转化,通过一步反应就能实现的有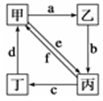
| A.只有a、b、c、d | B.只有b、c、d、e |
| C.只有c、d、e、f | D.a、b、c、d、e、f |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是
| A.合金的熔点一般比组分金属低 |
| B.铝钠合金若投入一定量的水中可得无色溶液,则n(Al)≤n(Na) |
| C.铝钠合金投入到足量氯化铜溶液中,会有氢氧化铜沉淀也可能有铜析出 |
| D.若m g不同组成的铝钠合金投入足量盐酸中,放出的H2越多,则铝的质量分数越小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
科学家研制出了一种新型的贮氢材料——镁铝合金。这种镁铝合金具有特定的组成,其成分可表示为Mg17Al12。其贮氢和释氢的原理可表示为:Mg17Al12+17H2  17MgH2+12Al
17MgH2+12Al
下列有关说法正确的是( )
| A.该合金的熔点介于镁和铝的熔点之间 |
| B.Mg17Al12是离子化合物 |
| C.732g的合金能吸收380.8L氢气 |
| D.熔炼制备Mg17Al12时需通入氩气,目的是防止金属被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定量的Fe、FeO、Fe2O3的混合物中,加入100mL、1.1mol/L的盐酸反应并放出标准状况下224mL气体,反应后溶液中阳离子只有Fe2+、H+,且溶液的pH=1(不考虑盐的水解及溶液体积的变化)。则反应后溶液Fe2+的物质的量浓度(mol·L-1)为
| A.0.05 | B.0.5 | C.0.55 | D.1.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列陈述中,Ⅰ、Ⅱ都正确且两者间具有因果关系的一组是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | FeCl3溶液能腐蚀Cu | Fe的金属性强于Cu |
| B | Na2O2使酚酞溶液变红 | Na2O2是碱性氧化物 |
| C | Cl2可部分与水反应 | 用排饱和食盐水法收集Cl2 |
| D | 浓H2SO4可干燥NO和SO2 | NO和SO2还原性都弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com