
����Ŀ�������仯������������˽ũҵ��������Ҫ��������NAΪ�����ӵ�������ֵ�������й�˵��������ǣ� ��
A.��״���£�5.6LNO��5.6LO2��ֻ�Ϻ�ķ�����Ϊ0.5NA
B.��״���£�22.4L15NH3���е�������Ϊ10NA
C.13.8gNO2������ˮ��Ӧ��ת�Ƶĵ�����Ϊ0.2NA
D.�����£�1L0.1mol��L1NH4NO3��Һ�к��еĵ�ԭ����Ϊ0.2NA
���𰸡�A
��������
A. ��״���£�5.6LNO�����ʵ���Ϊ0.25mol��5.6LO2�����ʵ���Ϊ0.25mol�����߳�ֻ�Ϻ���2NO ��O2 ��2NO2�����ݷ���ʽ��ϵ������O2�����ʵ���Ϊ0.125mol��NO��Ӧ�꣬����0.25mol NO2���ܵ����ʵ���Ϊ0.25 mol��0.125mol��0.375mol�����ڶ������������Է��������淴Ӧ����������������������ʵ���С��0.375mol��������С��0.375NA����A����
B. 1��15NH3����10�����ӣ���״���£�22.4L15NH3�����ʵ���Ϊ1mol�����22.4L15NH3 ���е�������Ϊ10NA����B��ȷ��
C. NO2������ˮ��Ӧ3 NO2��H2O ��2HNO3��NO��3mol NO2ת��2mol���ӣ�13.8gNO2�����ʵ���![]() �����13.8gNO2������ˮ��Ӧת�Ƶĵ�����Ϊ0.2NA����C��ȷ��
�����13.8gNO2������ˮ��Ӧת�Ƶĵ�����Ϊ0.2NA����C��ȷ��
D. �����£�1L0.1mol��L1NH4NO3��Һ���ʵ���Ϊ![]() ����˺��еĵ�ԭ����Ϊ0.2 NA����D��ȷ��
����˺��еĵ�ԭ����Ϊ0.2 NA����D��ȷ��
������������ΪA��


 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪28 g CuO��MgO�Ĺ���������200 mLijH2SO4��Һǡ����ȫ��Ӧ������Ӧ�����ҺС�����ɣ��õ�����68 g����ԭH2SO4��Һ�����ʵ���Ũ�Ⱥ�ԭ������������Ԫ�ص����������ֱ���( )
A.2.5 mol��L��1��28.57%B.2.2 mol��L��1��23.07%
C.1.5 mol��L��1��24.55%D.2.5 mol��L��1��18.37%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25�桢101kPa�����£�C��s����H2��g����CH3COOH��l����ȼ���ȷֱ�Ϊ393.5kJ/mol��285.8kJ/mol��870.3kJ/mol����2C(s)+2H2(g)+O2(g)=CH3COOH(l)�ķ�Ӧ��Ϊ
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(10��)����ͼ��ʾװ�ÿ�������ȡ�۲�Fe(OH)2�ڿ����б�����ʱ��ɫ�ı仯��ʵ��ʱ����ʹ����м��6 mol/L�����ᣬ�����Լ���ѡ����д���пհס�
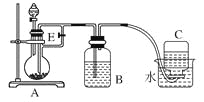
��1��B��ʢһ������NaOH��Һ��A��ӦԤ�ȼ�����Լ���____________��A�з�Ӧ�����ӷ���ʽ�ǣ�_________��
��2��ʵ�鿪ʼʱ���Ƚ�����E______(�������������ر���)��C���ռ����������Ҫ�ɷ���________��
��3����������Fe(OH)2�IJ�������________________��
��4����ȥװ��B�е���Ƥ����ʹ�������룬д���йط�Ӧ�Ļ�ѧ����ʽ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ʵ�ת����ϵ�У�A��һ�ֹ��嵥�ʣ��ҳ����뵼����ϣ�E��һ�ְ�ɫ������F����������嵥�ʡ�
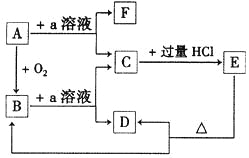
�ݴ���д��
��1��B�Ļ�ѧʽ��____________��Ŀǰ���ִ�ͨѸ����B�ѱ�����_____________��Ҫԭ�ϡ�
��2��B��a��Һ��Ӧ�����ӷ���ʽ��_____________________��
��3��A��a��Һ��Ӧ�����ӷ���ʽ��_____________________��
��4��C�������ᷴӦ�����ӷ���ʽ��____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ�ý���ʵ�飬��д�й�����ѧ����ʽ��
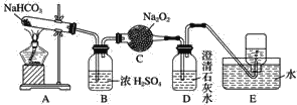
(1)A��������________________________________��
(2)B��Ũ�����������__________________________��
(3)C�з�����Ӧ�Ļ�ѧ����ʽΪ____________________________________��
(4)D�������______________________________��
(5)E���ռ���������____________(������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С��ͬѧ�����ij��������Ʒ���������Ĵ���(���������ɷֲ����ᷴӦ��Ҳ������ˮ)������������ʵ�飺��ȡ10.00 g��������Ʒ�����뵽�ձ��У��ټ���92.50 g ��ϡ���ᣬǡ����ȫ��Ӧ�����˵�����2.50 g���Լ��㣺
(1)��������Ʒ��������������������___________
(2)������Ӧ��������Һ�����ʵ�����������___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѧ���������ɫ���ɡ����롣�ѿ����е�CO2����ת������ʹ֮��H2��Ӧ���ɿ�������Դ�״���
��1����ҵ�����п�����H2��ԭCO2�Ʊ������Դ�״���
�����й������ܵ�˵����ȷ����____��
A�������������Դ B�������Ƕ�����Դ
C�������Dz���������Դ D����̬����Դ�����ױ��������
����֪CO��g����H2��g����ȼ���ȣ���H���ֱ�Ϊ-283.0kJmol-1��-285.8kJmol-1��CO��H2�ϳɼ״��������仯��ͼ����ʾ��
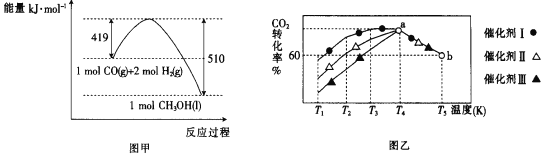
����CO2��g����H2��g���Ʊ�Һ̬�״����Ȼ�ѧ����ʽΪ____��
�۽�һ������CO2��H2���뵽ij�����ܱ������У�����ڲ�ͬ���������£���ͬʱ����CO2��ת�������¶ȵı仯��ͼ����ʾ����Ч����õ��Ǵ���____��ѡ�������
��2������CO��ˮ����������H2����Ӧ�Ļ�ѧ����ʽ��CO��g��+H2O��g��CO2��g��+H2��g��������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������н������·�Ӧ���õ��������������ʾ��
�¶�/�� | ��ʼ�� | �ﵽƽ�� | |||
CO/mol | H2O/mol | H2/mol | COת���� | ʱ��/min | |
650 | 4 | 2 | 1.6 | 10 | |
900 | 3 | 2 |
| 5 | |
900��ʱ���ﵽƽ��ʱ�ķ�Ӧ����v��H2O��=____��������2λС������
��3����ѧ�һ��о�������ת����������ķ�����������ͼ��ʾװ�ÿ��Խ�CO2ת��Ϊ����ȼ��CO����װ�ù���ʱ��N�缫�ĵ缫��ӦʽΪ____��
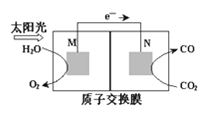
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������茶���[(NH4)2Fe(SO4)2��6H2O]������ˮ���ڶ��������г����������������ӵı���Һ��ij��ѧ����С��ͬѧ��Ʋ��������ʵ�顣
I.(NH4)2Fe(SO4)2��6H2O����ȡ
ʵ�鲽�裺
�ٳ�ȡ4.2g����м����ƿ�У�����10mL30%��NaOH��Һ��������У���ʱ�䡣��ȥ��Һ��ˮϴ�����ԡ�
������������м�м���25mL3mol/LH2SO4��ˮԡ��������Ӧ��ȫ�����ȹ��ˡ�
������Һ�м��룭������ı���(NH4)2SO4��Һ������Ũ������ȴ�����ˣ�ϴ�ӣ�����ò�Ʒ��
��1��������м���NaOH��Һ��Ŀ����___��
��2������ڳ��ȹ��˵�Ŀ����___��
��3������ۼ���Ũ����Һʱ����Ҫ�������оƾ��ơ�___��___���̶����г��������⣩��
��.(NH4)2Fe(SO4)2��6H2O��FeSO4��7H2O�ȶ��ԵĶԱ��о�
��ͼ����2֧��ͬ��ע�����зֱ�װ������ʵ��������־��壬����2֧ע��������ʹ���������ȣ�����ͷ���������ע���������������ã����ϳ�ʱ���ȡ�����־��壬�ֱ�μ�2��0.01mol/LKSCN��Һ������������ʵ�������¼���£�
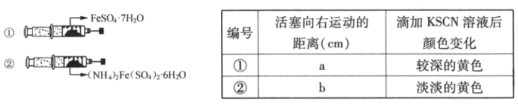
��4���ж�a___b������>������<������=���������ִ˽����ԭ�������___��
��5���жϴ�������(NH4)2Fe(SO4)2��6H2O���ȶ���___����������������С������FeSO4��7H2O��
��.����(NH4)2Fe(SO4)2��Һ���궨Ũ��
����(NH4)2Fe(SO4)2��Һ100mL��ȷ��ȡ20.00mL��������ƿ�У���10mLH2SO4���ڶ�����ָʾ��3��4�Σ���cmol/LK2Cr2O7��Һ�ζ�����Һ����غ�ɫ������K2Cr2O7��Һ�����ΪVmL��
��6������(NH4)2Fe(SO4)2��Һ��Ũ��Ϊ___ mol/L��
��7�����в�����ʹ������ҺŨ��ƫ�����___�����ţ���
A.��ƿ�ô�����Һ��ϴ
B.�ζ�ǰ�ζ��ܼ��촦�����ݣ��ζ���������ʧ
C.�ζ������о���ҡ����ƿ����Һ����
D.�ζ�ǰƽ�Ӷ������ζ����Ӷ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com