
【题目】图Ⅰ的目的是精炼铜,图Ⅱ的目的是保护钢闸门。
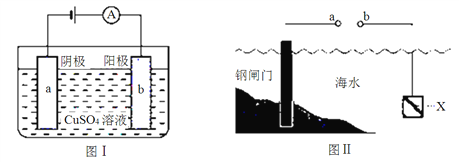
下列说法不正确的是
A. 图Ⅰ中a为纯铜
B. 图Ⅰ中![]()
![]() 向b极移动
向b极移动
C. 图Ⅱ中如果a、b间连接电源,则a连接负极
D. 图Ⅱ中如果a、b间用导线连接,则X可以是铜
科目:高中化学 来源: 题型:
【题目】为确定盐酸、碳酸、硅酸的酸性强弱,设计了如图所示的装置,一次实验即可达到目的(不必选其他酸性物质)。(提示:检验酸的酸性强弱可用强酸制取弱酸)
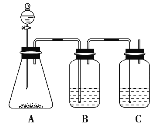
(1)锥形瓶中装某可溶性正盐,分液漏斗中所盛试剂应为________。
(2)装置B中所盛试剂是________________________________________,其作用是_____________。
(3)装置C中所盛试剂是___________________________________________,
C中反应的离子方程式是_________________________________________________。
(4)由此得到的结论是酸性:________>________>________。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为四个常用的电化学装置,关于它们的叙述正确的是
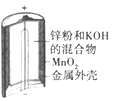
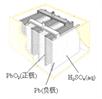
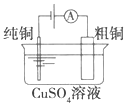
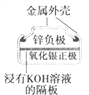
(a)碱性锌锰电池 (b)铅-硫酸蓄电池 (c)电解精炼铜 (d)银锌纽扣电池
A. 图(a)所示电池中,MnO2的作用是催化剂
B. 图(b)所示电池放电过程中,硫酸浓度不断增大
C. 图(c)所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图(d)所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨作电极电解KCl和CuSO4(等体积混合)混合溶液,电解过程中溶液pH随时间t的变化如图所示,下列说法正确的是
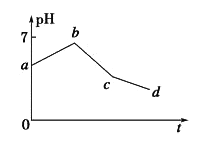
A. ab段H+被还原,溶液的pH 增大
B. cd 段相当于电解水
C. c点时加人适量CuCl2固体,电解液可恢复原来浓度
D. 原溶液中KCl和CuSO4的物质的量浓度之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于物质分类的正确组合是( )
分类组合 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | 纯碱 | HCl | 烧碱 | 氧化铝 | 二氧化碳 |
B | 烧碱 | 硫酸 | 食盐 | 氧化镁 | 一氧化碳 |
C | 苛性钠 | 醋酸 | 碳酸铵 | 过氧化钠 | 二氧化硫 |
D | 苛性钾 | HCl | 小苏打 | 氧化钠 | 三氧化硫 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用乙炔作为有机合成的原料时,下列过程可能生成产物为CH2Br—CHBrCl的是( )
A.加HCl再加Br2 B.加HCl再加HBr
C.加Cl2再加HBr D.加Cl2再加Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示装置中,石墨电极的电极反应式为___________________,如果开始加入的CuSO4足量,则电解一段时间,当电路中转移1.0 mol电子时,要使溶液恢复至原浓度,可向其中加入的物质是____________(填化学式),其质量为________g。
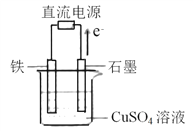
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以绿矾(FeSO4·7H2O)制备补血剂甘氨酸亚铁[(NH2CH2COO)2Fe] 有关物质性质如下:
甘氨酸(NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有强酸性和还原性 | 易溶于水,难溶于乙醇 |
实验过程:
Ⅰ.配制含0.10mol FeSO4的绿矾溶液。
Ⅱ.制备FeCO3:向配制好的绿矾溶液中,缓慢加入200mL 1.1mol·L-1NH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
Ⅲ.制备(NH2CH2COO)2Fe:实验装置如下图(夹持和加热仪器已省略),将实验Ⅱ得到的沉淀和含0.20 mol甘氨酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。
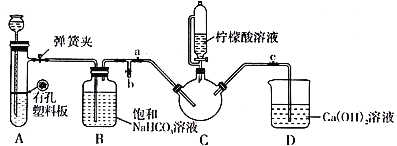
回答下列问题:
(1)实验I中:实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为_______(写化学式)。再滴加少量稀硫酸的作用是__________________________。
(2)实验II中:生成沉淀的离子方程式为__________________________。
(3)实验Ⅲ中:①C中盛柠檬酸溶液的仪器名称为___________________。
②装置A中所盛放的药品是___________________。(填序号)
A.Na2CO3和稀H2SO4 B.CaCO3和稀H2SO4 C.CaCO3和稀盐酸
③确认C中空气排尽的实验现象是____________________。
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是________________。
⑤洗涤实验Ⅲ中得到的沉淀,所选用的最佳洗涤试剂是___________________。(填序号)
A.热水 B.乙醇溶液 C.柠檬酸溶液
⑥若产品的质量为17.34g,则产率为________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识回答下列问题:
Ⅰ.丁腈橡胶(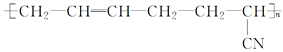 )具有优良的耐油、耐高温性能,合成丁腈橡胶的二种单体是_________________和_______________,是通过___________反应得到。
)具有优良的耐油、耐高温性能,合成丁腈橡胶的二种单体是_________________和_______________,是通过___________反应得到。
Ⅱ. 硅橡胶具有无毒,无味,耐高温又耐低温,可制成耐温垫圈,密封件和人造心脏,人造血管等,他是由单体二甲基二氯硅烷(CH3)2SiCl2水解得到二甲基硅二醇,经脱水缩聚成的聚硅氧烷再经交联制成的,请用化学方程式写出上述二甲基二氯硅烷水解及线性缩聚的方程式_________________和_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com