
【题目】在一定条件下,将N2、H2混合气体100 mL通入密闭容器内,达到平衡时,容器内的压强比反应前减小![]() ,测得此时混合气体的平均相对分子质量为9。试求:
,测得此时混合气体的平均相对分子质量为9。试求:
(1)原混合气中N2、H2各多少毫升______?
(2)H2的转化率是多少______?
【答案】20 mL、80 mL 37.5%
【解析】
(1)设出氢气、氮气的体积及转化的氮气体积,然后根据题中数据列式计算出a,然后根据容器内的压强比反应前减少1/5,利用化学平衡的三段式列式计算出原混合气体中N2和H2的体积;
(2)根据计算出转化的氮气计算出消耗的氢气体积,再计算出氢气的转化率。
(1)设原混合气体中N2的体积为x,H2的体积为y,反应中转化的N2的体积为a,则x+y=100mL ①

反应后气体的体积减小了2a,根据容器内的压强比反应前减少1/5,则达到平衡状态时气体的物质的量比反应前减少了![]() ,
,![]() =
=![]() ②,将①带人②解得,a=10mL,根据三段式:
②,将①带人②解得,a=10mL,根据三段式:
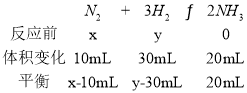
相同条件下,气体摩尔体积相同,设为Vm,根据质量守恒定律及反应后气体的体积可得,混合气体的平均分子量为: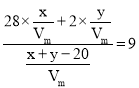 ③,由③化简有19x-7y+180=0 ④由①④联立,解得x=20mL,y=80mL;
③,由③化简有19x-7y+180=0 ④由①④联立,解得x=20mL,y=80mL;
(2)反应消耗10mL氮气,同时消耗了30mL氢气,所以氢气的转化率为:![]() ×100%=37.5%。
×100%=37.5%。


科目:高中化学 来源: 题型:
【题目】已知反应A2(g)+2B2(g)![]() 2AB2(g) ΔH<0,下列说法正确的是
2AB2(g) ΔH<0,下列说法正确的是
A. 达平衡后降低温度,混合气体平均相对分子质量减小
B. 使用催化剂能加快反应速率,缩短达平衡所需的时间且提高A2的转化率
C. 达平衡后升高温度并增大压强,有可能每一组分的百分含量都不改变,但平衡常数一定发生改变
D. 达平衡后,降低温度或减小压强都有利于该平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池的反应原理如图所示。下列有关氢氧燃料电池的说法不正确的是
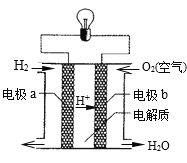
A.该电池中电极a是负极
B.该电池工作时化学能转化为电能
C.该电池的总反应为:2H2+O2=2H2O
D.外电路中电流由电极a通过导线流向电极b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解的催化效果,甲乙两组同学分别设计了如图一、图二所示的实验。
(1)可通过观察图一的现象:_______________,而定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是_____________,你认为还可以作何改进?____________________。
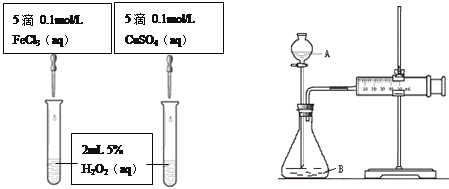
图一 图二
(2)检查图二装置气密性的方法是_______________________。图二所示实验中需测量的数据是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的是( )
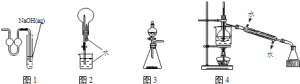
A.用图1装置作为制取二氧化碳的尾气吸收装置
B.用图2装置进行二氧化碳喷泉实验
C.用图3装置进行二氧化锰和浓盐酸制取氯气的实验
D.用图4装置进行石油的分馏实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是( )
甲 乙
乙
丙 丁
丁
A. 图甲是在不同温度下三个恒容容器中反应2H2(g)+CO(g)CH3OH(g) ΔH<0的平衡曲线,曲线X对应的温度相对较高
B. 图乙是一定温度下三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线,a点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-)
C. 图丙为MOH和ROH两种一元碱水溶液在常温下分别加水稀释时pH的变化曲线,可知ROH是强碱
D. 图丁为两个容器中在不同的压强下各投入1 mol CH4和1 mol CO2所发生反应CH4(g)+CO2(g)2CO(g)+2H2(g)的平衡曲线,N点化学平衡常数K=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应X(g)+2Y(g)Z(g)△H<0,一定温度下,在体积为2L的密闭容器中加入4mol Y和一定量的X后,X的浓度随时间的变化情况如图所示,则下列表述正确的是( )

A. 达到平衡时,X、Y、Z物质的量之比为1:2:1
B. a点正反应速率大于逆反应速率
C. 反应达平衡时,降低温度可以实现c到d的转化
D. 该条件下,反应达平衡时,X平衡转化率为25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某化学反应A2(g)+2B2(g)=2AB2(g) (A2、B2、AB2的结构式分别为A=A、B-B、B-A-B),能量变化如图所示,下列有关叙述中正确的是
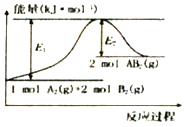
A. 该反应若生成2molAB2(g)则吸收的热量为(El-E2)kJ
B. 该反应的进行一定需要加热或点燃条件
C. 该反应断开化学键消耗的总能量小于形成化学键释放的总能量
D. 生成2molB-B键放出E2kJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com