
【题目】某二元弱碱B(OH)2(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀B(OH)2溶液中滴加等浓度盐酸溶液,B(OH)2、B(OH)+、B2+的浓度分数δ随溶液POH[POH=-lgc(OH)-]变化的关系如图,以下说法正确的是
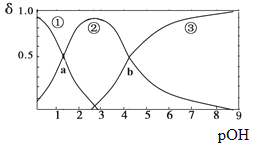
A. 交点a处对应加入的盐酸溶液的体积为5mL
B. 当加入的盐酸溶液的体积为10mL时存在c(Cl-)>c(B(OH)+)>c(H+)>c(OH-)>c(B2+)
C. 交点b处c(OH)=6.4×10-5
D. 当加入的盐酸溶液的体积为15mL时存在:c(Cl-)+c(OH-)= c(B2+)+c(B(OH)+)+ c(H+),
【答案】C
【解析】图中曲线①B(OH)2,②为B(OH)+ ③为B2+;交点a处对应加入的盐酸溶液的体积为5mL时,反应生成等浓度的B(OH)Cl和B(OH)2混合液,由于两种溶质水解电离能力不同,所以B(OH)2、B(OH)+ 浓度分数δ不相等,A错误;当加入的盐酸溶液的体积为10mL时,溶液为B(OH)Cl,溶液显酸性,根据B(OH)2(K1=5.9×10-2、K2=6.4×10-5)可知,c(Cl-)>c(B(OH)+)>c(H+)> c(B2+)>c(OH-),B错误;交点b处时,c(B(OH)+)= c(B2+),根据B(OH)+ ![]() B2++ OH-,K2= c(OH-)=6.4×10-5, C正确;当加入的盐酸溶液的体积为15mL时,生成等体积等浓度B(OH)Cl和BCl2的混合液,存在电荷守恒为c(Cl-)+c(OH-)= 2c(B2+)+c(B(OH)+)+ c(H+),D错误;正确选项C。
B2++ OH-,K2= c(OH-)=6.4×10-5, C正确;当加入的盐酸溶液的体积为15mL时,生成等体积等浓度B(OH)Cl和BCl2的混合液,存在电荷守恒为c(Cl-)+c(OH-)= 2c(B2+)+c(B(OH)+)+ c(H+),D错误;正确选项C。


科目:高中化学 来源: 题型:
【题目】CO、SO2是常见的大气污染物,应用化学原理变废为宝,意义重大。
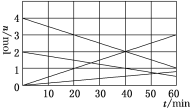
(1)CO与SO2用铝矾土作催化剂、475 ℃条件下反应生成CO2和硫蒸气,该反应可用于从烟道气中回收硫,反应过程中各组分的物质的量与反应时间的关系如图所示,该反应的化学方程式为________。
(2)利用CO可以合成新能源物质——甲醇。其原理为CO(g)+2H2(g)![]() CH3OH(g) ΔH。在压强分别为p1、p2,体积均为V L的两个容器中充入a mol CO、2a mol H2,在催化剂作用下反应生成甲醇,平衡时转化率与温度、压强的关系有下表数据:
CH3OH(g) ΔH。在压强分别为p1、p2,体积均为V L的两个容器中充入a mol CO、2a mol H2,在催化剂作用下反应生成甲醇,平衡时转化率与温度、压强的关系有下表数据:
50 ℃ | 100 ℃ | 200 ℃ | 300 ℃ | 400 ℃ | |
p1 | 0.65 | 0.50 | 0.40 | 0.32 | 0.24 |
p2 | 0.80 | 0.70 | 0.65 | 0.50 | 0.41 |
①ΔH________0,p1________p2。(填“>”“<”或“=”)。
②压强为p2,温度为300 ℃时,该反应的平衡常数K=________。
③压强为p1,温度为100 ℃时,达到平衡后,继续向其中通入0.5a mol CO、a mol H2、0.5a mol CH3OH,则平衡时CH3OH的体积分数________(填“增大”“减小”或“不变”)。
④下列说法正确的是________。
a.当n(CO)∶n(H2)∶n(CH3OH)=1∶2∶1时,可逆反应达到平衡状态
b.平衡后向体积为V L的容器内继续充入He,平衡不移动
c.使用新型催化剂,可提高CO的平衡转化率
(3)MnO2悬浊液、NaOH溶液都是SO2气体常用的吸收剂。
①已知MnO2+SO2=MnSO4,吸收SO2的装置如图所示。反应过程中,为使SO2尽可能转化完全,可采取的合理措施有___________、__________。
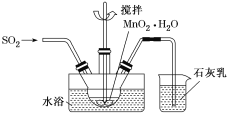
②将标准状况下4.48 L SO2气体缓缓通入100 mL 3 mol·L-1 NaOH溶液中,充分反应后c(Na+)=___ (填几种粒子浓度之和)。
③取②中所得溶液10 mL,加水稀释成1 L,向其中加入CaCl2固体至有沉淀CaSO3(Ksp=3.1×10-7)生成,则所加CaCl2固体的质量为_____mg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在烷烃分子中的基团:-CH3、-CH2-、![]() 、
、![]() 中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示。例如:
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示。例如: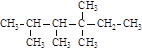 分子中,n1=6,n2=1,n3=2,n4=1。试根据不同烷烃的组成结构,分析出烷烃(除甲烷外)各原子数的关系。
分子中,n1=6,n2=1,n3=2,n4=1。试根据不同烷烃的组成结构,分析出烷烃(除甲烷外)各原子数的关系。
(1)烷烃分子中氢原子数n0与n1、n2、n3、n4之间的关系是n0=_________________。
(2)四种碳原子数之间的关系为n1=_________________________________________。
(3)若分子中n2=n3=n4=1,则该分子的结构简式可能为(任写一种)________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ⅢA族的硼、铝、镓、铟、铊等元素在化合物中通常表现出+3价,含ⅢA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题。
(1)基态Ga原子价层电子排布式_____。
(2)砷化镓属于第三代半导体,晶胞结构与金刚石相似。下列说法正确的是_____。
A.砷化镓晶胞结构中Ga原子的轨道杂化方式为sp3
B.第一电离能:As<Ga
C.电负性:As<Ga
D.砷和镓都属于p区元素
(3)BCl3的立体构型是____,由第二周期元素组成的与BCl3互为等电子体的阴离子为____。
(4)已知:Al的燃烧热为△H1=akJ·mol-1;Fe2O3(s)+2Al(s)=Al2O3(s)+2Fe(s);ΔH2=bkJ/mol,则:3O2(g)+4Fe(s)=2Fe2O3(s);ΔH3=____kJ/mol。
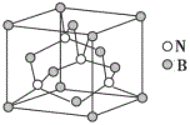
(5)人造立方氮化硼晶胞如图所示,判断该晶体结构中存在配位键的依据是____。设该晶体的摩尔质量为Mg/mol,晶体的密度为ag/cm3,阿伏加德罗常数的值为NA,则晶体中两个距离最近的B原子之间的距离为____cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
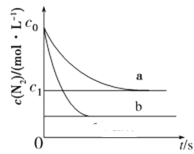
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述不正确的是( )
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述不正确的是( )
A.温度T下,该反应的平衡常数![]()
B.温度T下,随着反应的进行,混合气体的密度不变
C.曲线b对应的条件改变可能是增大压强
D.若曲线b对应的条件改变是温度,可判断该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】呋喃酚是合成农药的重要中间体,其合成路线如下:
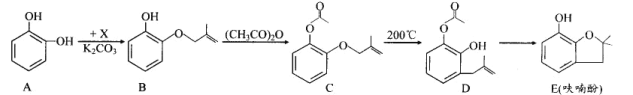
(1)A 物质核磁共振氢谱共有___________个峰,B→C 的反应类型是_____;E 中含有 的官能团名称是_____,D不能够发生的反应有_________(填代号)。
①氧化反应 ②取代反应 ③加成还原 ④消去反应
(2)已知 X 的分子式为 C4H7Cl,写出 A→B 的化学方程式:_____________。
(3)Y 是 X 的同分异构体,分子中无支链且不含甲基,则 Y 的名称(系统命名)是 ________。
(4)下列有关化合物 C、D 的说法正确的是_____________。
①可用氯化铁溶液鉴别 C 和 D ②C、D 含有的官能团完全相同
③C、D 互为同分异构体 ④C、D 均能使溴水褪色
(5)E 的同分异构体很多,写出符合下列条件的芳香族同分异构体的结构简式:____________。
①环上的一氯代物只有一种 ②含有酯基 ③能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把m mol乙烯跟n mol H2混合于一密闭容器中,在适当条件下反应并生成p mol C2H6,若将所得的混合气体燃烧,并全部生成CO2和H2O,需要氧气的物质的量(单位:mol)为
A.3m+nB.![]()
C.![]() D.3m+
D.3m+![]() -3p
-3p
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是

A. Ka2(H2X)的数量级为10-6
B. 曲线N表示pH与![]() 的变化关系
的变化关系
C. 当混合溶液呈中性时,![]()
D. NaHX溶液中![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com