
【题目】古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是( )
A. 粉身碎骨浑不怕,要留清白在人间
B. 野火烧不尽,春风吹又生
C. 春蚕到死丝方尽,蜡炬成灰泪始干
D. 爆竹声中一岁除,春风送暖入屠苏
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 60gSiO2和12g金刚石中各含有4NA个Si-O键和4NA个C-C键
B. H2O(g)通过足量Na2O2(s)充分反应,固体增重bg时,反应中转移的电子数为bNA/2
C. 1L0.2mo1/ LNaHCO3溶液中含HCO3-和CO32-的离子数之和为0.2NA
D. 足量的Mg与稀H2SO4完全反应,生成2.24LH2时,转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消細,与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
(1)方法一的离子方程式为______________________________。
(2)方法二中被氧化的物质是_______,若反应中有0.1 mol电子转移,则产生的ClO2气体在标准状况下的体积为_________L。
(3)用双线桥法标出方法一中方程式电子转移的方向和数目_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温密闭容器中发生反应:CaCO3(s)![]() CaO(s)+CO2(g) H>0,反应达到平衡后,tl时缩小容器体积, x随时间(t)变化的关系如下图所示。x不可能是
CaO(s)+CO2(g) H>0,反应达到平衡后,tl时缩小容器体积, x随时间(t)变化的关系如下图所示。x不可能是

A. υ逆(逆反应速率) B. ρ(容器内气体密度)
C. m(容器内CaO质量) D. Qc(浓度商)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一个绝热恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g)![]() CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示,由图可得出的结论正确的是
CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示,由图可得出的结论正确的是

A. 反应物浓度:a点小于c点
B. 该反应的正反应为放热反应
C. c点达到平衡状态
D. Δt1=Δt2时,H2的产率:a~b段大于b~c段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定温度下,X(g)+2Y(g)![]() mZ(g);ΔH =-akJ/mol(a>0)现有甲、乙两容积相等且固定的密闭容器,在保持该温度下,向密闭容器甲中通入1molX和2molY,达平衡状态时,放出热量bkJ;向密闭容器乙中通入2molX和4molY,达平衡状态时,放出热量ckJ,且2b < c,则下列各值关系正确的是
mZ(g);ΔH =-akJ/mol(a>0)现有甲、乙两容积相等且固定的密闭容器,在保持该温度下,向密闭容器甲中通入1molX和2molY,达平衡状态时,放出热量bkJ;向密闭容器乙中通入2molX和4molY,达平衡状态时,放出热量ckJ,且2b < c,则下列各值关系正确的是
A. a = b B. 2a < c C. m > 3 D. m < 3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiH2PO4是制备电池的重要原料。室温下,LiH2PO4溶液的pH随c初始(H2PO4–)的变化如图1所示,H3PO4溶液中H2PO4–的分布分数![]() 随pH的变化如图2所示,
随pH的变化如图2所示,![]() 下列有关LiH2PO4溶液的叙述正确的是
下列有关LiH2PO4溶液的叙述正确的是
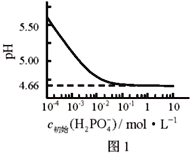
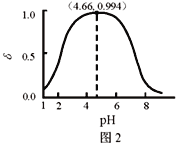
A. 含P元素的粒子有H2PO4–、HPO42–、PO43–
B. LiH2PO4溶液中存在2个平衡
C. 用浓度大于1 mol·L-1的H3PO4溶液溶解Li2CO3,当pH达到4.66时,H3PO4几乎全部转化为LiH2PO4
D. 随c初始(H2PO4–)增大,溶液的pH明显变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、D、E、G、M六种元素位于元素周期表前四周期,原子序数依次增大。其中,元素A的一种核素无中子,B的单质既有分子晶体又有原子晶体,化合物DE2为红棕色气体,G是前四周期中电负性最小的元素,M的原子核外电子数比G多10。
请回答下列问题:
(1)基态G原子的核外电子排布式是___________,M在元素周期表中的位置是_______,元素B、D、E的第一电离能由大到小的顺序为______________________(用元素符号表示)。
(2)元素A和E组成的阳离子空间构型为__________________________;化合物ABD的结构式为____________,其中B原子的杂化方式为____。

(3)G、M的晶体晶胞结构如图所示,这两种晶胞中原子的配位数之比为___________。若晶体M密度为8.9g·cm-3,则M的晶胞边长是____________________cm(不必计算出结果)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com