
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42-、OH- |

分析 测得乙中c电极质量增加了6.4g,则乙中含有Cu2+,结合离子的共存可知,乙为CuSO4,丙中pH不变,则为硫酸钠或硫酸钾,甲中pH增大,则A为KOH或NaOH,
(1)乙中c电极铜离子得电子,则c为阴极,即M为电源负极,则b为阳极,碱溶液中OH-放电,f是阳极,碱溶液中OH-放电,e是阴极,是氢离子得电子的还原反应,氢离子放电生成氢气;
(2)b为阳极,碱溶液中OH-放电;
(3)根据电解池的工作原理来书写电解方程式,根据电极反应结合电子守恒计算产生气体的物质的量.
解答 解:测得乙中c电极质量增加了6.4g,则乙中含有Cu2+,结合离子的共存可知,乙为CuSO4,丙中pH不变,则为硫酸钠或硫酸钾,甲中pH增大,则A为KOH或NaOH,
(1)乙中c电极铜离子得电子,则c为阴极,即M为电源负极,N是正极,则b为阳极,碱溶液中OH-放电,f是阳极,碱溶液中OH-放电,e是阴极,该电极上氢离子得电子的还原反应生成氢气,氢离子浓度减小,所以碱性增强,遇到酚酞显示红色,故答案为:负;e;
(2)b为阳极,碱溶液中OH-放电,电极反应为:4OH--4e-=O2↑+2H2O;故答案:4OH--4e-=O2↑+2H2O;
(3)乙烧杯电解质是硫酸铜溶液,电解的总反应离子方程式为:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+4H+,甲烧杯中盛有NaOH或是KOH,电解时的a极上发生反应:2H++2e-=H2↑;b电极上发生电极反应:4OH--4e-=O2↑+2H2O,乙中c电极质量增加6.4g,即产生Cu0.1mol,根据Cu~2e-,所以转移电子是0.2mol,产生氢气是0.1mol,产生氧气是0.,05mol,两电极上产生气体0.15mol,体积是0.15mol×22.4L/mol=3.36L.
故答案为:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+4H+;3.36.
点评 本题考查电解原理,明确发生的电极反应、电解反应及图象的分析是解答本题的关键,注意利用乙推出各物质及电源的正负极是解答的突破口,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 锗可用于制造半导体材料 | |
| B. | RbOH的碱性强于Ca(OH)2 | |
| C. | SrCO3是白色难溶于水易溶于盐酸的化合物 | |
| D. | 砹化银(AgAt)是白色难容于稀硝酸的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种元素组成的分子中所含化学键一定都是极性键 | |
| B. | 金属晶体的熔点一定比分子晶体的高 | |
| C. | 某晶体中含有阳离子,则一定也含有阴离子 | |
| D. | 含有阴离子的化合物一定含有阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
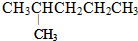 的是( )
的是( )| A. | CH3CH=CHCHCH2CH3 | B. | CH2=CHCHCH2CH3 | ||
| C. | CH≡CCHCH2CH3 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
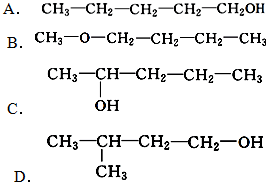
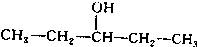 .
.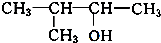 、
、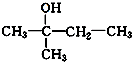 写出另外两种同分异构体的结构简式:
写出另外两种同分异构体的结构简式: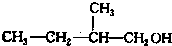 、
、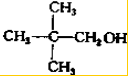 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 家用电器起火 常用液态CO2灭火 一般不用液态四氯化碳 | |
| B. | 将一氧化碳中毒者移到通风处抢救 | |
| C. | 眼睛里不慎溅进了药液 应立即用水冲洗 边洗边眨眼睛 不可用手揉眼睛 | |
| D. | 实验后 剩余的药品不能随便丢弃 或浪费 应放回原瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com