
【题目】甲醇是重要的化工原料,利用煤化工中生产的CO、CO2和H2可制取甲醇等有机物,发生的反应有:
①CO(g)+2H2(g)![]() CH3OH(g) △H1=-99kJ·mol-1
CH3OH(g) △H1=-99kJ·mol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
相关物质的化学键键能数据如下:
化学键 | C=O(CO2) | H—H | C—O | H—O | C—H |
E/(kJ·mol-1) | 803 | 436 | 343 | 465 | 413 |
(1)该反应△H2=___________。
(2)关于反应①下列说法,正确的是___________。
A.该反应在任何温度下都能自发进行
B.升高温度,正反应速率增大,逆反应速率减小
C.使用催化剂,不能提高CO的转化率
D.增大压强,该反应的化学平衡常数不变
(3)在某温度下,将1.0moCO与2.0molH2充入2L的空钢瓶中,发生反应①,在第5min时达到化学平衡状态,此时甲醇的物质的量分数为0.1。在第10min、20min时分别改变反应条件,甲醇的浓度在不同条件下的变化状况如下图所示:

①从反应开始到5min时,生成甲醇的平均速率为___________。
②H2的平衡转化率α=___________%,化学平衡常数K=___________。
③1min时,υ正___________υ逆(填“大于”“小于”或“等于”)
④1mim时υ正___________4min时υ逆(填“大于”“小于”或“等于”)
⑤比较甲醇在7~8min、12~13min和25~27min时平均反应速率[平均反应速率分别以υ(7~8)、υ(12~13)、υ(25~27)表示的大小_________________________________。
③若将钢瓶换成同容积的绝热容器,重复上述试验,平衡时甲醇的物质的量分数___________0.1。(填“>”、“<”或“=”)
【答案】-63 kJ·mol-1 CD 0.025 mol·L-1·min-1 25 0.59 大于 大于 υ (12~13)>υ(7~8)=υ(25~27) <
【解析】
(1)反应热=反应物总键能-生成物总键能;
(2)A、△G=△H-T△S<0反应才能自发;B、升高温度,正逆反应速率均增大;C、使用催化剂,不改变平衡;D、平衡常数与温度有关;
(3)根据三段式解析。①由速率的定义式计算;②根据转化率和平衡常数表达式计算;③反应正向进行时,正速率大。④平衡之前,正速率大于逆速率;⑤平衡时平均速率为0;⑥绝热条件,放热反应发生后体系温度升高。
(1)CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),该反应△H2=2×803kJ·mol-1+3×436kJ·mol-1-(3×413+343+465)kJ·mol-1-2×465kJ·mol-1=-63 kJ·mol-1 ;
CH3OH(g)+H2O(g),该反应△H2=2×803kJ·mol-1+3×436kJ·mol-1-(3×413+343+465)kJ·mol-1-2×465kJ·mol-1=-63 kJ·mol-1 ;
(2)①CO(g)+2H2(g)![]() CH3OH(g) △H1=-99kJ·mol-1
CH3OH(g) △H1=-99kJ·mol-1
A.△H1=-99kJ·mol-1,△S<0,△G=△H-T△S,该反应在低温下可能自发进行,故A错误;
B.升高温度,正反应速率增大,逆反应速率也增大,故B错误;
C.使用催化剂,不改变平衡,不能提高CO的转化率,故C正确;
D.平衡常数与温度有关,增大压强,该反应的化学平衡常数不变,故D正确;
故选CD。
(3)根据题目数据计算如下:
CO(g) + 2H2(g) ![]() CH3OH(g)
CH3OH(g)
起始/mol·L-1: 0.5 1 0
反应/mol·L-1: X 2X X
平衡/mol·L-1: 0.5-X 1-2X X
甲醇的物质的量分数为![]() =10%,所以 X=0.125mol·L-1。
=10%,所以 X=0.125mol·L-1。
①甲醇的速率为0.125mol·L-1÷5min=0.025 mol/(L·min)。
②由上述计算,反应的氢气为2×0.125 mol·L-1=0.25 mol·L-1,转化率为0.25 mol·L-1÷1 mol·L-1=25%。达平衡时CO、H2和CH3OH的物质的量浓度分别为:0.375mol·L-1、0.75mol·L-1和0.125mol·L-1,所以平衡常数K=0.125/(0.375×0.752)=0.59。
③1min时,没有达到平衡,甲醇的浓度增大,反应正向进行,υ正>υ逆;
④反应达平衡的速率图像如下图:
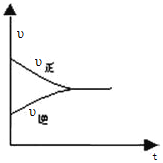
所以,在达平衡前任意点的正反应速率大于任意点的逆反应速率,即1min时的υ正(CH3OH)>4min 时υ逆(CH3OH )。
⑤12~13min处于非平衡状态,反应速度大,甲醇在7~8min、25~27min处于平衡状态,平均反应速率为0,甲醇在7~8min、12~13min和25~27min时平均反应速率的大小:υ(12~13)>υ(7~8)=υ(25~27);
⑥若将钢瓶换成同容积的绝热钢瓶,重复上述实验,则反应放出的热量不能散发,会使体系温度上升,正反应放热,温度升高,平衡逆向移动,甲醇体积分数将减小,所以小于0.1。


科目:高中化学 来源: 题型:
【题目】(NH4)2SO4是一种常见的化肥,某工厂用石膏、NH3、H2O、CO2制备(NH4)2SO4的工艺流程如下:

下列说法正确的是
A.通入NH3和CO2的顺序可以颠倒
B.操作1为过滤,操作2为蒸馏
C.通入的NH3和CO2均应过量,且工艺流程中CO2可循环利用
D.步骤②中反应的离子方程式为CaSO4+2NH3+CO2+H2O=CaCO3↓+2NH4++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.乙烯的产量是衡量一个国家石油化工发展水平的标志
B.含碳元素的化合物都是有机化合物
C.蛋白质水解最终生成氨基酸
D.乙烯、苯分子中的所有原子在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各方程式中,属于水解反应的是( )
A. HCO3—+H2O![]() H2CO3+OH- B. HCO3—+H2O
H2CO3+OH- B. HCO3—+H2O![]() CO32—+H3O+
CO32—+H3O+
C. HCO3—+OH-=CO32-+H2O D. CO32-+H+=HCO3—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物光化学烟雾,其中某些反应过程如图所示。下列说法不正确的是( )

A. NO2不是酸性氧化物B. O2和O3是氧的两种同素异形体
C. 反应I属于氧化还原反应D. 烟雾是一种固溶胶,其分散剂是空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃ 时,将3mol A和1molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(g) + B(g) ![]() xC(g)2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)从开始反应至达到平衡的状态,生成C平均反应速率为__________。
(2)x=__________;平衡常数K=____________。
(3)若继续向原混合物的容器中通入少量氦气(设氦气和A、B、C都不反应)后,化学平衡(填字母)____。
A、向正反应方向移动 B、向逆反应方向移动 C、平衡不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示的装置中,A是氯气发生装置,C、D 为气体净化装置(C中装有饱和食盐水;D 中装有浓硫酸),E 是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G 中装有氢氧化钠溶液。

试回答:
(1)仪器A的名称是__________;
(2)C装置的作用是__________;
(3)D 装置的作用是__________;
(4)E中发生化学反应的方程式为:_____________________________;
(5)烧杯G 中发生反应的化学方程式为:_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒(23V)是我国的丰产元素,广泛应用于催化及钢铁工业,有“化学面包”、金属“维生素”之称。回答下列问题:
(1)钒原子的核外电子排布式为________________,在元素周期表中的位置为______。
(2)V2O5常用作SO2转化为SO3的催化剂。基态S原子电子占据最高能级的电子云轮廓为________形;气态SO3以单分子形式存在,其分子的立体构型为_______形;固体SO3的三聚体环状结构如图所示,该结构中S—O键长有a、b两类,b的键长大于a的键长的原因为______________。

(3)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子中V的杂化轨道类型为___________;也可得到偏钒酸钠,其阴离子呈如图所示的无限链状结构,则偏钒酸钠的化学式为_____________。

(4)钒的某种氧化物晶胞结构如图所示。该氧化物的化学式为__________,若它的晶胞参数为x nm,则晶胞的密度为__________ g/cm3。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com