
【题目】物质中的化学能在一定条件下可转化为电能。
(1)将锌片放入盛有稀硫酸的烧杯中,反应的离子方程式是_________。
(2)将锌片、铜片按照下图所示装置连接,能证明化学能转化为电能的实验现象是:铜片上有气泡产生、_________。
(3)稀硫酸在下图所示装置中的作用是:传导离子、_________。

(4)下列反应通过原电池装置,可实现化学能直接转化为电能的是_________ (填序号)。
①CaCO3+2HCl=CaCl2+H2O+CO2↑
②2H2+O2![]() 2H2O
2H2O
③Pb+PbO2 +2H2SO4![]() 2PbSO4+2H2O
2PbSO4+2H2O
【答案】Zn + 2H+=Zn2++ H2↑ 电流表指针偏转 作正极反应物 ②③
【解析】
(1)锌和硫酸反应生成硫酸锌和氢气;
(2)该原电池中,Zn易失电子作负极,Cu作正极,正极上氢离子得电子发生还原反应,(3)电极反应式为2H++2e-=H2↑。
(4)能设计成原电池的反应是能自发的进行氧化还原反应。
(1)将锌片放入盛有稀硫酸的烧杯中,锌和硫酸反应生成硫酸锌和氢气,反应的离子方程式是Zn + 2H+=Zn2++ H2↑ 。
(2)将锌片、铜片按照图示装置连接,形成原电池,Zn易失电子作负极,铜作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,能证明化学能转化为电能的实验现象是铜片上有气泡产生、电流表指针偏转。
(3)稀硫酸在图示装置中的作用是传导离子、作正极反应物,发生2H++2e-=H2↑。
(4)①CaCO3+2HCl=CaCl2+H2O+CO2↑反应中没有化合价变化,是非氧化还原反应;
②2H2+O2![]() 2H2O,氢气作还原剂,氧气作氧化剂,是氧化还原反应。
2H2O,氢气作还原剂,氧气作氧化剂,是氧化还原反应。
③Pb+PbO2 +2H2SO4![]() 2PbSO4+2H2O,铅作还原剂,氧化铅作氧化剂,是氧化还原反应。
2PbSO4+2H2O,铅作还原剂,氧化铅作氧化剂,是氧化还原反应。
故选②③。


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。Z原子的最外层电子数是6,下列说法中正确的是
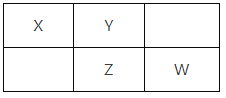
A. 原子半径: X>Y>Z>W
B. 最高价氧化物对应水化物的酸性: X> Z> W
C. 4种元素的单质中,Z单质的熔沸点最低
D. W单质能与水反应,生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,水只作氧化剂的是
①氟气通入水中 ②水蒸气经过灼热的焦炭 ③钠块投入水中
④铁与水蒸气反应 ⑤氯气通入水中
A. 只有①④ B. 只有①⑤
C. 只有②③ D. 只有②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的叙述错误的是
A. 用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同
B. 胶粒能透过滤纸,但不能透过半透膜
C. 胶体与其它分散系的本身区别是丁达尔现象
D. Al(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为有机化合物,它们之间的转化关系如下图所示(提示:RCH=CHR′在酸性高锰酸钾溶液中反应生成RCOOH和R′COOH,其中R和R′为烷基)。
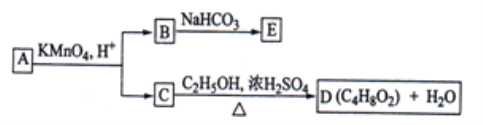
(1)直链化合物A的相对分子质量小于90,A分子中碳、氢元素的总质量分数为0.814,其余为氧元素,则A的分子式为______;
(2)已知B与NaHCO3溶液完全反应,其物质的量之比为1:2,则在浓硫酸的催化下,B与足量的C2H5OH发生反应的化学方程式是_____________________,反应类型为______;
(3)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是______;
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有______种,其相应的结构简式是_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组设计了如下实验,探究常温下催化剂对过氧化氢分解反应的影响。
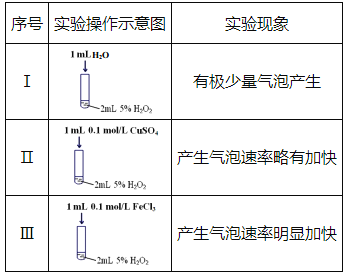
(1)实验I的作用是_________。
(2)实验III中反应的化学方程式为_________。
(3)根据实验I~III中现象的不同,可以得出的结论是:
①使用合适的催化剂,可提高双氧水分解的反应速率;
②___________________________。
(4)在一定温度下,10mL0.40mol/LH2O2溶液发生催化分解,6min后H2O2的浓度减小到0.10mol/L,以H2O2的浓度变化表示的反应速率为v(H2O2)=_________mol/(L·min)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想将不溶的碳酸盐材料通过特殊的加工方法使之变为纳米碳酸盐材料(即碳酸盐材料粒子直径是纳米级),这将使建筑材料的性能发生巨大变化,下列关于纳米碳酸盐材料的推测正确的是
A. 纳米碳酸盐材料是与胶体相似的分散系
B. 纳米碳酸盐材料分散到水中会产生丁达尔效应
C. 纳米碳酸盐材料的化学性质已与原来的碳酸盐材料完全不同
D. 纳米碳酸盐材料的粒子不能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体,图1表示各物质浓度随时间的变化,图2表示速率随时间的变化。t2、t3、t4、t5时刻后各改变一种条件,且改变条件均不同。若t4时刻改变条件是压强,则下列说法错误的是
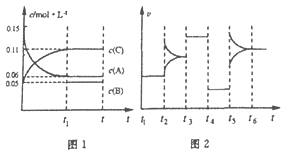
A. 若t1=15s,则前15s的平均反应速率v(C)=0.004mol·L-1·s-1
B. 该反应的化学方程式为:3A(g) ![]() B(g)+2C(g)
B(g)+2C(g)
C. t2、t3、t5时刻改变的条件分别是升高温度、加入催化剂、增大反应物浓度
D. B的起始物质的量为0.04mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达700 -900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。下列说法正确的是

A. 电极甲发生还原反应
B. 电池内的O2-由电极乙移向电极甲
C. 电池总反应为N2H4 +2O2= 2NO +2H2O
D. 当甲电极上有lmol N2H4消耗时,乙电极上有22.4L O2参与反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com