
【题目】亚硝酰氯(ClNO)是有机合成中的重要试剂。可通过以下反应制得:2NO(g)+Cl2(g)![]() 2ClNO(g)。按投料比[n(NO):n(Cl2)]=2:1把NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率 与温度T、压强p(总压)的关系如图所示:
2ClNO(g)。按投料比[n(NO):n(Cl2)]=2:1把NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率 与温度T、压强p(总压)的关系如图所示:
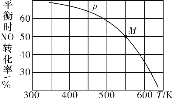
(1)该反应的△H____(填“>”“<”或“=”)0。
(2)在压强为p条件下,M点时容器内NO的体积分数为_______。
(3)若反应一直保持在p=b Pa压强条件下进行,则M点的分压平衡常数Kp=________(用含b的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
(4)实验测得,v正=k正·c2(NO)·c(Cl2),v逆=k逆·c2(ClNO)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数____(填“>”“<”或“=”)k逆增大的倍数。
②若在2 L的密闭容器中充入1 mol Cl2和1 mol NO,在一定温度下达到平衡时,NO的转化率为40%,则k正:k逆=________。(保留一位小数)
【答案】< 40% ![]() Pa-1 < 1.1
Pa-1 < 1.1
【解析】
(1)根据图象,升高温度,NO的转化率减小,说明平衡逆向移动,正反应为放热反应;
(2)由差量法进行计算,根据2NO(g)+Cl2(g)=2ClNO(g)可知,气体减小的物质的量为反应的NO的物质的量的一半;
(3)设NO的物质的量为2mol,则Cl2的物质的量为1mol,列三段式求解平衡K;
(4)①结合温度对反应速率的影响回答;
②平衡时v正=v逆,则k正c2(NO)C(Cl2)=k逆C2(ClNO),则![]() =K,已知起始量1molCl2和1mol NO,NO的转化率为40%,列三段式求解。
=K,已知起始量1molCl2和1mol NO,NO的转化率为40%,列三段式求解。
(1)根据图象,升高温度,NO的转化率减小,说明平衡逆向移动,说明该反应正反应为放热反应,△H<0;
(2)根据图象,在压强为P条件下,M点时容器内NO的转化率为50%,根据2NO(g)+Cl2(g)=2ClNO(g)可知,气体减小的物质的量为反应的NO的物质的量的一半,因此NO的体积分数为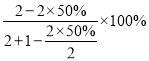 =40%;
=40%;
(3)设NO的物质的量为2mol,则Cl2的物质的量为1mol,列三段式如下:
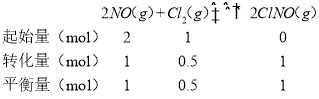
平衡常数K=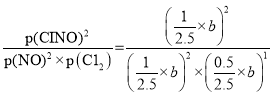
![]() =
=![]() Pa-1;
Pa-1;
(4)①平衡时正逆反应速率相等,温度升高,正逆反应速率增大,即k正、k逆均增大,因为反应放热,平衡逆向移动,所以k逆比k正增大多;
②已知起始量1molCl2和1mol NO,NO的转化率为40%,则c(NO)=1mol÷2L=0.5mol/L,c(Cl2)=1mol÷2L=0.5mol/L,△c(NO)=0.5mol/L×40%=0.2mol/L,列三段式如下:

平衡常数K=![]() =1.1(mol/L)-1,平衡时v正=v逆,则k正c2(NO)c(Cl2)=k逆c2(ClNO),则
=1.1(mol/L)-1,平衡时v正=v逆,则k正c2(NO)c(Cl2)=k逆c2(ClNO),则![]() =K=1.1(mol/L)-1。
=K=1.1(mol/L)-1。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下:

为了研究X的结构,将化合物A在一定条件下水解只得到 和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。

(ⅰ)写出有机物的结构简式:D:______________,C:________________,E:______________。
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)
反应①__________________________________;反应⑥_____________________________。
(ⅲ)变化过程中的②属于____________反应,⑦属于________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气(CO 和H2)是合成甲醇的重要原料,它可用水蒸气通过炽热的炭层制得:C(s)+H2O(g)![]() CO(g)+H2(g) △H=+131.3kJ/mol
CO(g)+H2(g) △H=+131.3kJ/mol
⑴该反应的平衡常数的表达式为:_________________;升高温度,K值将 ;容器中气体的平均相对分子质量将 。(填“增大”、“减小”或“不变”)。
⑵上述反应达到平衡后,将体系中的C(s)部分移走,平衡将 (填序号)。
A.向左移 B.向右移 C.不移动
⑶下列事实能说明该反应在一定条件下已达到平衡状态的有 (填序号)。
A.单位体积内每消耗1molCO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
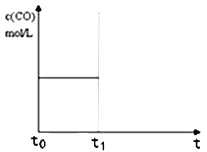
⑷上述反应在t0时刻达到平衡(如图),若在t1时刻改变某一条件,请在图中继续画出t1时刻后c(CO)随时间的变化曲线:
①缩小容器体积(用实线表示)。
②降低温度(用虚线表示)。
⑸某温度下,将4.0mol H2O(g)和足量的炭充入2L的密闭容器中,发生如下反应,C(s)+H2O(g)![]() CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳足量,反应C(s)+H2O(g)![]() CO(g)+H2(g)在一个可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加碳的量且表面积保持不变 ②将容器的体积缩小一半 ③保持体积不变,充入He,使体系压强增大 ④保持压强不变,充入He使容器体积变大
A.①④B.②③C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.1000 mol·L![]() NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L![]()
![]() 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是
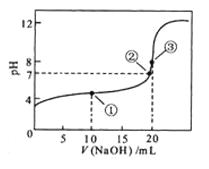
A.点①所示溶液中:![]()
B.点②所示溶液中:![]()
C.点③所示溶液中:![]()
D.滴定过程中可能出现:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4 5H2O是铜的重要化合物,有着广泛的应用。
(一)CuSO4·5H2O制取
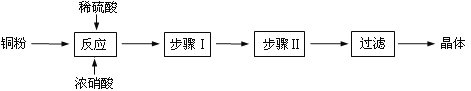
完成下列填空:
(1)向含铜粉的稀硫酸中滴加少量浓硝酸(可加热),铜粉溶解时可以观察到的实验现象:_____。
(2)根据反应原理,硝酸与硫酸的理论配比(物质的量之比)为______________________。
(3)步骤Ⅰ______________;步骤Ⅱ______________。
(二)胆矾中CuSO4·5H2O含量的测定
已知:CuSO4 + 2NaOH → Cu(OH)2 ↓+ Na2SO4
(1)实验方案如下,并将步骤④补全:
①将12.500g胆矾样品溶解,配成100mL溶液,取25mL于烧杯中;
②向溶液中加入100mL0.2500mol/L氢氧化钠溶液使Cu2+完全沉淀(不考虑其它副反应);
③过滤,多余的氢氧化钠溶液用0.5000mol/L盐酸滴定至终点,耗用10.00mL盐酸;
④___________________________
⑤数据处理。
(2)在滴定中,眼睛应注视__________;滴定终点时,准确读数应该是滴定管上________所对应的刻度。
(3)就方案中数据进行处理,则样品CuSO4·5H2O中质量分数为___________。步骤③中沉淀未洗涤,导致结果______(填偏大、偏小、无影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 的相对原子质量为34.969,下列相关说法正确的是( )
的相对原子质量为34.969,下列相关说法正确的是( )
A.氯元素的近似相对原子质量为35
B.氯元素的某种同位素的质量数为35
C.氯元素的中子数为18
D.氯原子的质量为34.969
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s,白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1
②Sn(s,灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2
③Sn(s,灰)![]() Sn(s,白) △H3=+2.1kJmol-1
Sn(s,白) △H3=+2.1kJmol-1
下列说法正确的是( )
A.△H1>△H2
B.锡在常温下以灰锡状态存在
C.灰锡转为白锡的反应是放热反应
D.锡制器皿长期处在低于13.2℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向恒温恒压容器中充入2 mol NO、1 mol O2,发生反应:2NO(g)+O2(g)![]() 2NO2(g)。下列情况不能说明反应已达到平衡状态的是( )
2NO2(g)。下列情况不能说明反应已达到平衡状态的是( )
A.NO与O2的物质的量的比值不再改变B.混合气体的颜色不再改变
C.容器体积不再改变D.混合气体的密度不再改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com