
| ||
| ||
| A����Ӧ���е�TiO2�������� |
| B��TiCl4�ڷ�Ӧ�����ǻ�ԭ����ڷ�Ӧ������������ |
| C��a=b=c=2 |
| D��ÿ����9.6gTi����Ӧ���й�ת��0.8mol���� |
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
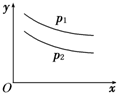 ��Ӧ��L��s��+aG��g��?bR��g���ﵽƽ�⣬�¶Ⱥ�ѹǿ�Ը÷�Ӧ��Ӱ����ͼ��ʾ��ͼ�У�ѹǿP1��P2��x���ʾ�¶ȣ�y���ʾƽ��������G������������ݴ˿��жϣ�������
��Ӧ��L��s��+aG��g��?bR��g���ﵽƽ�⣬�¶Ⱥ�ѹǿ�Ը÷�Ӧ��Ӱ����ͼ��ʾ��ͼ�У�ѹǿP1��P2��x���ʾ�¶ȣ�y���ʾƽ��������G������������ݴ˿��жϣ�������| A��������Ӧ�Ƿ��ȷ�Ӧ |
| B��������Ӧ�����ȷ�Ӧ |
| C��a��b |
| D����ȷ��a��b�Ĵ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��[H+]�����¶ȵ����߶����� |
| B����35��ʱ��[H+]��[OH-] |
| C��ˮ�ĵ���̶Ȧ���25�棩������35�棩 |
| D��ˮ�ĵ��������ȵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��KCl |
| B��MnCl2 |
| C��H2O |
| D��Cl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������6.5g |
| B������6.5g |
| C������5.6g |
| D������5.6g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2mol/L |
| B��1.2mol/L |
| C��0.8mol/L |
| D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH2�TCH-CH�TCH2 1��4-����ϩ |
B��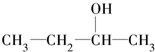 2-���� 2-���� |
C��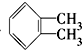 �ڶ��ױ� �ڶ��ױ� |
D��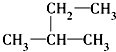 2-������ 2-������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com