
����Ŀ��ij��ѧ��ȤС��������ͼװ���Ʊ��������������۲�����ɫ���ṩ��ѧҩƷ�����ۡ�ϡ���ᡢ����������Һ��
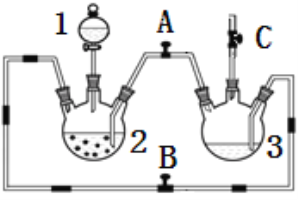
��1��ϡ����Ӧ����___________�У���д����������.
��2����ʵ��ͨ������A��B��C�����������������еĿ����ž����ٹرտ���______������_______�Ϳɹ۲쵽��������������ɫ���Է���ʵ�鿪ʼʱ�ž�װ���п���������_________________��
��3����ʵ��ʹ�����ۣ�����Ӧ���ʿ���̫���⣬�����ܻ���ɵIJ��������__________________��
��4����FeSO4��Һ�м���(NH4��2SO4������Ʊ���������茶���[(NH4��2SO4��FeSO4��6H2O] ��ʽ��Ϊ392�����þ����һ���������ȶ������ױ�������������ˮ���������Ҵ���
��Ϊϴ��(NH4��2SO4��FeSO4��6H2O�ֲ�Ʒ�����з���������ʵ���__________��
A������ˮϴ B��������ˮϴ��������ˮ�Ҵ�ϴ
C����30%���Ҵ���Һϴ D����90%���Ҵ���Һϴ
��Ϊ�˲ⶨ��Ʒ�Ĵ��ȣ���ȡa g��Ʒ����ˮ�����Ƴ�500mL��Һ����Ũ��Ϊc mol��L-1������KMnO4��Һ�ζ���ÿ����ȡ����Һ�����Ϊ25.00mL��ʵ������¼���£�
ʵ����� | ��һ�� | �ڶ��� | ������ |
���ĸ��������Һ���/mL | 25.52 | 25.02 | 24.98 |
�ζ������з�����Ӧ�����ӷ���ʽΪ______________________.�ζ��յ��������_____________________.ͨ��ʵ�����ݼ���ĸò�Ʒ����Ϊ______________������ĸac�������ϱ��е�һ��ʵ���м�¼�������Դ��ں����Σ���ԭ�������_______��
A��ʵ�����ʱ���ӿ̶��߶�ȡ�ζ��յ�ʱ���Ը��������Һ�����
B���ζ�ǰ�ζ��ܼ��������ݣ��ζ�����������
C����һ�εζ��õ���ƿ�ô�װҺ��ϴ����������δ��ϴ
D�������Ը�����ر�Һ����ʱ��������в��ֱ�����Ũ�Ƚ���
���𰸡� ��Һ©�� B A ��ֹ���ɵ����������������� ���۽��뵼�ܴӶ��������� D MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O ���һ�ε�������Һ����ɫ��Ϊdz��ɫ����30s����ɫ ![]() ��100% BC
��100% BC
����������1��ʵ�鿪ʼ��ʱ��ϡ����Ӧ�÷��ڷ�Һ©���У�ʵ�����μӣ������۷�Ӧ��������������������
��2���ž������رտ���B����A��������Ӧ�������ɵ��������ݳ���ֻ����2�оۼ���ѹǿ����������Һ������Aѹ��װ��3�ڡ��ž�װ���ڵĿ�������ҪĿ����Ϊ���ų�������������������������������Ϊ����������
��3�����ۿ���̫С�����ܽ����ܿڶ�ס��
��4������Ϊ�þ���������ˮ���������Ҵ�������Ӧ��ѡ����90%���Ҵ���Һϴ���������Ա����Ʒ����ʧ��
�����Ը��������Һ��������������Ϊ�����ӣ����Ӧ����ʽΪ��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O���ﵽ�ζ��յ��ʱ������Һ�����е��������Ӷ�����Ӧ������Ĺ����ĸ������ʹ��Һ��dz��ɫ�������յ�����Ϊ�����һ�ε��룬��Һ����ɫ��Ϊdz��ɫ����30s����ɫ����һ�ε�ʵ������̫��������ȥ�������ε�ƽ��ֵΪ25.00mL�����Ը������Ϊ25c/1000mol����������Ϊ��5����������c/8mol�����500mL��Һ��ȡ��25ml������ԭ��������Ϊ![]() ��������������茶���Ϊ5c/2 mol������Ϊ392��5c/2�����Բ�Ʒ����Ϊ��392��5c/2a=980c/a��ʵ�����ʱ���ӿ̶��߶�ȡ�ζ��յ㣬�Ὣ������ص������С������ѡ��A���ζ�ǰ�ζ��ܼ��������ݣ��ζ����������ݣ��Ὣ����ĸ�����ص�������ѡ��B��ȷ����һ�εζ��õ���ƿ�ô�װҺ��ϴ����������δ��ϴ����ƿ�Dz���Ҫ��ϴ�ģ������ϴ�ˣ���ƿ�ڱ��ϻ���һ������������泥���������Ҫ�������ĸ��������Һ��ѡ��C��ȷ�������Ը�����ر�Һ����ʱ��������в��ֱ��ʣ���ô���εζ�����ʹ����ͬ�ĸ������Ũ�����Ӧ�ò����С��ѡ��D����
��������������茶���Ϊ5c/2 mol������Ϊ392��5c/2�����Բ�Ʒ����Ϊ��392��5c/2a=980c/a��ʵ�����ʱ���ӿ̶��߶�ȡ�ζ��յ㣬�Ὣ������ص������С������ѡ��A���ζ�ǰ�ζ��ܼ��������ݣ��ζ����������ݣ��Ὣ����ĸ�����ص�������ѡ��B��ȷ����һ�εζ��õ���ƿ�ô�װҺ��ϴ����������δ��ϴ����ƿ�Dz���Ҫ��ϴ�ģ������ϴ�ˣ���ƿ�ڱ��ϻ���һ������������泥���������Ҫ�������ĸ��������Һ��ѡ��C��ȷ�������Ը�����ر�Һ����ʱ��������в��ֱ��ʣ���ô���εζ�����ʹ����ͬ�ĸ������Ũ�����Ӧ�ò����С��ѡ��D����


 ��ս100��Ԫ����Ծ�ϵ�д�
��ս100��Ԫ����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ֺ����ӻ�������ںϳ��л����Ϻ�ҩƷ������ҪӦ�á���ṹ����ͼ��ʾ�����й��ڸ��л����˵������ȷ����

A. 1mol��������������4mol NaOH
B. 1mol���л�����H2��Ӧʱ���������6mol H2
C. ���л���ı����ϵ�һ�ȴ�����3��
D. �÷�������ԭ�ӿ��ܴ���ͬһƽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ⶨˮ���ܽ����ķ����ǣ�
����ȡa mLˮ����Ѹ�ټ���̶���MnSO4��Һ�ͼ���KI��Һ(��KOH)����������ƿ����������ʹ֮��ַ�Ӧ���䷴ӦʽΪ��2Mn2����O2��4OH��===2MnO(OH)2(�÷�Ӧ����)��
�ڲⶨ��������Ѹ�ټ���1��2 mLŨ����(�ữ���ṩH��)��ʹ֮����I2������b mol/L��Na2S2O3��Һ�ζ�(�Ե���Ϊָʾ��)������V mL���йط�ӦʽΪ��MnO(OH)2��2I����4H��===Mn2����I2��3H2O��I2��2S2O![]() ===2I����S4O
===2I����S4O![]() ��
��
�Իش�
��1���ζ��������õ��IJ�������������ʽ�ζ��ܡ���ʽ�ζ����ȱ��_____________��
��2���ζ�����ʱ�����ֿ��Ƶζ��ܣ�����________���۾�Ҫע��________��
��3��ˮ���ܽ����ļ���ʽ��______(��g/LΪ��λ)��
��4���ζ�(I2��S2O![]() ��Ӧ)�Ե���Ϊָʾ�����յ�ʱ��Һ��________ɫ��Ϊ________ɫ���Ұ�����ڲ���ɫ��
��Ӧ)�Ե���Ϊָʾ�����յ�ʱ��Һ��________ɫ��Ϊ________ɫ���Ұ�����ڲ���ɫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������[(NH4)2SO4��FeSO4��6H2O]�ֳ�Ħ���Ρ�ij��ȤС���Ʊ���������淋�ʵ�鷽��ʾ��ͼ���£�
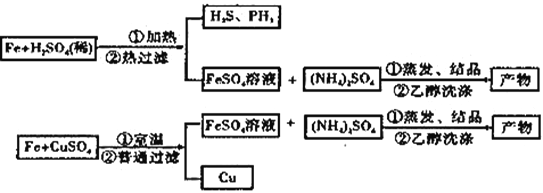
����A����ͼ������B����ͼ��
��֪��H2S��PH3Ϊ�ж����壬���ܱ�CuSO4��Һ���ճ�ȥ��
��ش��������⣺
��1��ʵ��ǰ������н�����м����̼������Һ����У��㵹��Һ�壬��ˮϴ����м�IJ������衣������������ѡ����װ����ɸò��������������_________�����ţ���
������̨�ڲ������۹��ƿ��ʯ�������ձ���©���߾ƾ���
��2������A��FeSO4��Һ���Ʊ����������õ���м������ƿ�����������3 mol��L��1H2SO4��Һ����������ַ�ӦΪֹ�����ȹ��ˣ��ռ���Һ��ϴ��Һ������ͼװ���з�����ѡ����ʺ�����ʵ�鷽��A��װ����________����ס����ҡ�����
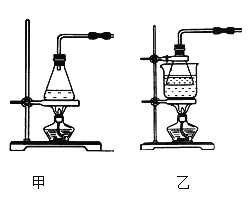
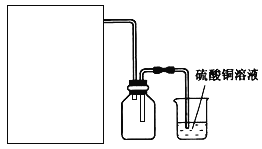
��3������A�з���м�к����������������Ʊ�ǰ��ȥ�������ǣ������ӷ���ʽ�ش�___________������ˮ�Ҵ�ϴ�Ӿ����ԭ����___________________��
��4��ʵ�鷽��B��FeSO4��Һ���Ʊ����á���ˮ����ͭ�ᾧˮ�IJⶨ��ʵ���еķ��������ˮ����ͭ��ĩ����ϡ��������м��Ӧ�Ʊ�����������������ˮ����ͭ���Ƶ���Һ����ɫ��ȫ��Ϊdz��ɫʱֹͣ��Ӧ�����ˣ��ռ���Һ��������������Һ���˷������ŵ���_______________�����ţ���
a.���������ʵ���ҷ����������ͭ��ĩ��������ҩƷ�˷ѣ��ֻ����˽���ͭ��ʵ���˱��Ϊ����
b.�������ж�������ŷŶԻ�����ɵ���Ⱦ��
c.ԭ�������ʴﵽ100%��
d.�������ڼ�����Fe2+��������Fe3+�� �����ڲ�Ʒ�����ȼ�����ߣ�����Լ����Դ��
��5����Ʒ��Fe3+���ʵĶ�������
������Fe3+Ũ��Ϊ1.0mg/mL�ı���Һ100mL����ȡ_______mg�ߴ��ȵ��������[(NH4)Fe(SO4)2��12H2O]����2.00 mL��������ȥ����ˮ�����ܽ����2mol��L��1HBr��Һl m L��l mol��L��1KSCN��Һ0.5 mL����ˮ�Ƴ�100 mL��Һ�����ƹ����б����õ��Ķ�������Ϊ____________��ѡ���ţ���
a.��ȷ��Ϊ0.001g�ĵ�����ƽb.��ȷ��Ϊ0.1mg�ĵ�����ƽ
c.100 mL����ƿd.��ʽ�ζ���e.10mL��Ͳ
�ڽ�������Һϡ��ΪŨ�ȷֱ�Ϊ0.2��1.0��3.0��5.0��7.0��10.0����λ��mg/L������Һ���ֱ�ⶨ��ͬŨ����Һ�Թ�����ճ̶ȣ������ⶨ������Ƴ��������¡�
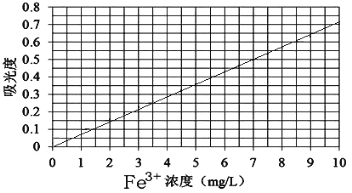
��ȡ����ȤС�����õ���������鱗�Ʒ�����������ò�Ʒ��Һ10mL��ϡ����100 mL��Ȼ����ڵķ������вⶨ�����βⶨ���õ�����ȷֱ�Ϊ0.490��0.510�������ȤС�������Ʒ�����������Һ������Fe3+Ũ��Ϊ_________mg/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���У���ѡװ�û�ʵ����ƺ�������
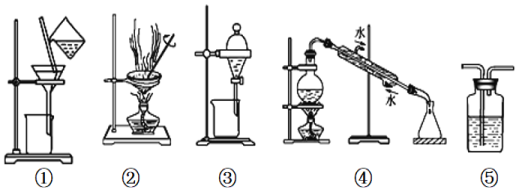
A. ��ͼ�ٺ͢���ʾװ�ÿ��Գ�ȥNa2CO3�е�CaCO3���ʣ������Na2CO3����
B. ���Ҵ���ȡ��ˮ�е���ѡ��ͼ����ʾװ��
C. ��ͼ����ʾװ�ÿ��Է����Ҵ�ˮ��Һ
D. ͼ����ʾװ����ʢ�б���Na2CO3��Һ��ȥCO2�к��е�����HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. �ƺ���ˮ��Ӧ��Na��2H2O��Na+��2OH��H2��
B. ����ʯ��ˮ������NaHCO3��Һ��ϣ�Ca2+ + OH��+ HCO3��![]() CaCO3��+ H2O
CaCO3��+ H2O
C. ���ˮ�е��������ı����Ȼ�����Һ��Fe 3++3H2O![]() Fe(OH)3��+3H+
Fe(OH)3��+3H+
D. ̼�������Һ�м����������������Һ HCO3��+ OH����CO32��+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ1��ͭпԭ���ʾ��ͼ��ͼ2�У�x���ʾʵ��ʱ���������ĵ��ӵ����ʵ�����y���ʾ��������

A. ͭ�������� B. c(Zn2��) C. c(H��) D. c(SO42-) -
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10mL0.1mol/L��Ԫ����H2A��Һ�еμ�0.1mol/LNaOH��Һ����Һ�и�������ʵ���������(X) [��(X)=![]() ]��pH�ı仯��ͼ��ʾ�����������������
]��pH�ı仯��ͼ��ʾ�����������������
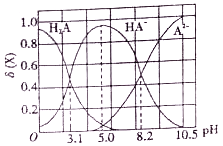
A. Ka1(H2A)Ϊ10-3.1
B. pH=5.0ʱ��c(Na+)>c(HA-)>c(H+)>c(OH-)>c(A2-)
C. pH=8.2ʱ��c(Na+)+c(H+)=c(OH-)+3c(A2-)
D. pH��5.0����10.5ʱ����Ҫ��Ӧ�����ӷ���ʽΪHA-+OH-=A2-+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���з��ӻ����������������¶�������KI�������������±仯��
H2O2��H2O IO3����I2 MnO4����Mn2�� HNO2��NO
����ֱ��õ����ʵ�������Щ��������������KI���õ�I2������( )
A.H2O2
B.IO3��
C.MnO4��
D.HNO2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com