
| A.-82kJ/mol | B.-41kJ/mol | C.-312kJ/mol | D.+82kJ/mol |
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源:不详 题型:单选题
| A.HCl+NH3=NH4Cl | B.2KClO3=2KCl+3O2↑ |
| C.2Na2O2+2H2O=4NaOH+O2↑ | D.Ba(OH)2·8H2O+2 NH4Cl=BaCl2+ 2NH3↑+10H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
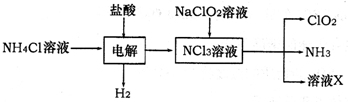
| ||
| . |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.两者对应反应的△H均小于0 |
| B.两者的单位均为kJ/mol,但mol-1的含义不同 |
| C.两者的数值均不随反应物用量改变而改变 |
| D.两者的数值均随反应物改变而改变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.该中和滴定过程,最宜用石蕊作指示剂 |
B.图中点②所示溶液中, |
| C.图中点①所示溶液中水的电离程度大于点③所示溶液中水的电离程度 |
D.滴定过程中的某点,会有 的关系存在 的关系存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com