
X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同。回答下列问题:
(1)X、Y和Z的元素符号分别为________、________和________。
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有________、________。
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是________。此化合物在酸性条件下与高锰酸钾反应的离子方程式为_______________________________________;
此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为________________________________________________________________________。
解析 (1)密度最小的气体为氢气,所以X为氢元素。Y原子的最外层电子数是其周期数的三倍,因为最外层电子数不超过8个(K层为最外层不超过2个),所以Y最外层应有6个电子,为氧元素。Z与氢元素最外层电子数相同,而且原子序数大于氧元素,Z为钠元素。
(2)由这三种元素组成的物质中既含有共价键又含有离子键的化合物有NaOH、Na2O2等,由H、O组成的化合物中既含有极性共价键又含有非极性共价键的是H2O2。
(3)在H2O2中氧元素显-1价,既有氧化性又有还原性。当H2O2与酸性高锰酸钾溶液反应时氧元素被氧化成氧气;与CN-反应时氧元素被还原成-2价。
答案 (1)H O Na (2)NaOH Na2O2 (3)H2O2 5H2O2+2MnO +6H+===2Mn2++8H2O+5O2↑ H2O2+CN-+OH-===CO
+6H+===2Mn2++8H2O+5O2↑ H2O2+CN-+OH-===CO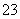 +NH3
+NH3


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为______________________________________________。
(2)W与Y可形成化合物W2Y,该化合物的电子式为___________________________。
(3)X的硝酸盐水溶液显____________性,用离子方程式解释原因:____________________。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为_________________。
(5)比较Y、Z气态氢化物的稳定性:______________>____________。(用分子式表示)
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是_________>___________>____________>__________。
(7)Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量。写出该反应的热化学方程式:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铊(Tl)是某超导材料的组成元素之一,与铝同族,位于第6周期。Tl3+与Ag在酸性介质中发生反应:Tl3++ 2Ag ==Tl+ + 2Ag+。下列推断正确的是
A.Tl+ 的最外层有1个电子
B.Tl3+ 的氧化性比Al3+弱
C.Tl能形成+3价和+1的化合物 
D.Tl+ 的还原性比Ag强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于元素周期表、元素性质的说法正确的是
A.目前使用的元素周期表中最长的周期含有36种元素
B.ⅠA族金属元素是同周期中金属性最强的元素
C.同种元素的原子均有相同的质子数和中子数
D.ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
某种元素的电离能数据如下(单位:kJ·mol-1),该元素最可能是
| I1 | I2 | I3 | I4 |
| 740 | 1 500 | 7 700 | 10 500 |
A.s区元素 B.f区元素
C.p区元素 D.d区元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )

①食盐水 ②KNO3溶液 ③适量稀硫酸铜溶液
④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
A.①③⑤ B.②⑥
C.③⑤ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
有关溶液中所含离子的检验,下列判断正确的是( )
A.加入硝酸酸化,再滴加KSCN溶液后有红色物质生成,则原溶液中一定有Fe3+存在
B.加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有CO32-存在
C.用某溶液做焰色反应时火焰为黄色,则该溶液中一定有钠元素,可能有钾元素
D.分别含Mg2+、Cu2+、Fe2+和Al3+的四瓶盐溶液,只用NaOH溶液不能一次鉴别开
查看答案和解析>>
科目:高中化学 来源: 题型:
现有化合物Z,它的阳离子可能是Na+、K+、Cu2+、Ag+,阴离子可能是SO42—、Cl—、CO32—,进行以下实验(填离子符号)
⑴做焰色反应,透过蓝色的钴玻璃观察无紫色火焰,肯定无 离子。
⑵取少量固体Z放入水中,得到无色溶液,肯定无 离子。
⑶向Z溶液中加入硝酸酸化的AgNO3溶液,无白色沉淀产生,肯定无 离子。
⑷另取Z溶液,先用盐酸酸化,无白色沉淀产生但有气泡产生,再加入BaCl2溶液,也没有白色沉淀产生,肯定无 、 离子。
(5)由上述实验事实,可推断化合物Z是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
试回答下列中学化学实验室中常见仪器的有关问题:
(1)在仪器①分液漏斗、②试剂瓶、③集气瓶、④滴瓶、⑤滴定管、⑥容量瓶、⑦量筒、⑧托盘天平中,标有“0”刻度的是(填序号,下同)________;标有使用温度的仪器是________。
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺。在仪器①试管、②分液漏斗、③细口试剂瓶、④广口试剂瓶、⑤集气瓶、⑥滴瓶、⑦酸式滴定管、⑧碱式滴定管中,用到“磨砂”的有________。
(3)在仪器①漏斗、②容量瓶、③蒸馏烧瓶、④分液漏斗、⑤烧杯、⑥蒸发皿中,可用于粗盐提纯实验的有________;可用于分离两种沸点接近且互不相溶的液态混合物实验的有________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com