
中学所学的A、B、C三种物质都是由H、O、S、Na中的三种元素组成的强电解质。A、B的水溶液均呈碱性,测得pH相等的A、B溶液c(A)<c(B);C的水溶液呈酸性。有关说法正确的是
A.A是Na2SO3
B. B溶于溴水中,不可能生成沉淀
C. B、C反应的离子方程式可能是:SO3-+2H+→ SO2↑+H2O
D. 若A、B两溶液的pH=9,则两溶液中水电离的OH-的物质的量浓度之比为1:1
C
解析试题分析:显碱性的物质可能是NaOH、Na2SO3、NaHS,pH相等的A、B溶液c(A)<c(B),说明A是NaOH,B是Na2SO3(或NaHS)。C的水溶液显酸性且为强电解质,应为硫酸;若B为NaHS,与溴水发生反应(HS-+Br2=S↓+2Br-+H+)会生成S沉淀;A为NaOH,水电离的OH-与溶液中H+浓度相同,为10-9 mol/L。B为能水解的盐,溶液中的OH-全部由水电离,其浓度为10-5 mol/L,故二者之比为1:104.A、A是NaOH,故A错误;B、若B为NaHS,与溴水发生反应(HS-+Br2=S↓+2Br-+H+)会生成S沉淀;故B错误;C、依据推断,B、C反应的离子方程式可能是:SO32-+2H+=SO2↑+H2O,故C正确;D、A为NaOH,水电离的OH-与溶液中H+浓度相同,为10-9 mol/L,B为能水解的盐,溶液中的OH-全部由水电离,其浓度为10-5mol/L,故二者之比为1:104;故D错误,答案选C。
考点:考查物质的推断、pH计算、硫及其化合物的性质以及盐类水解等


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:单选题
将导出H2S气体的导管点燃后伸入盛有一定量O2的集气瓶内,下列3个反应发生的先后顺序是
① 2H2S + O2 → 2S + 2H2O ② 2H2S + SO2 → 3S + 2H2O ③ 2H2S + 3O2 → 2SO2 + 2H2O
| A.①②③ | B.③①② | C.①③② | D.③②① |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
能证明碳酸比硅酸酸性强的实验事实是
| A.H2CO3比H2SiO3受热易分解 |
B.高温下能发生反应Na2CO3+SiO2 Na2SiO3+CO2↑ Na2SiO3+CO2↑ |
| C.CO2能溶于水生成碳酸,而SiO2却不溶于水 |
| D.CO2通入Na2SiO3溶液中有胶状沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于硅元素的说法,不正确的是
| A.光导纤维的主要成分是二氧化硅 | B.二氧化硅可以和水直接反应来制取硅酸 |
| C.硅可用作太阳能电池 | D.硅酸钠是制备硅胶和木材防火剂等的原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列陈述正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | 浓硫酸有强氧化性 | 浓硫酸可用于干燥H2和CO |
| D | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(15分)二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。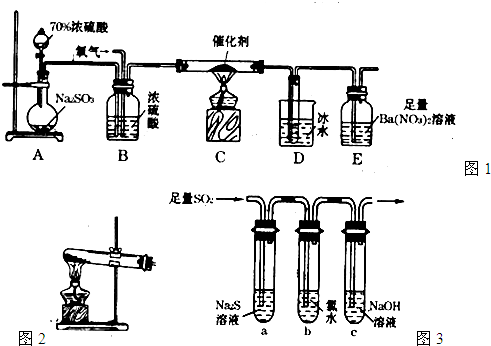
(1)实验室用图1装置测定SO2催化氧化为SO3的转化率。(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响。)
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作: 。
②实验过程中,需要通入氧气。试写出一个用如图2所示装置制取氧气的化学方程式: 。
③当停止通入SO2熄灭酒精灯后,需要继续通一段时间的氧气,其目的是: 。
④实验结束后,若装置D增加的质量为mg,装置E中产生白色沉淀的质量为ng,则此
条件下二氧化硫的转化率是 (用含字母的代数式表示,不用化简)。
(2)某学习小组设计用如图3装置验证二氧化硫的化学性质。
①能说明二氧化硫具有氧化性的实验现象为: 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分三份,分别进行如下实验。
方案I:向第一份溶液中加入AgNO3溶液,有白色沉
淀生成。
方案II:向第二份溶液中加入品红溶液,红色褪去。
方案III:向第三份溶液中加入BaC12溶液,产生白色沉淀
上述方案中合理的是 (填“I”、“II”、或“III”);
试管b发生反应的离子方程式: 。
③当通入二氧化硫至试管c中溶液显中性时,该溶液中
c(Na+)= (用含硫微粒浓度的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com