
【题目】已知:pK=-lgK,25℃时,二元酸H2A的pK1=1.85,pK2=7.19。25℃时,用0.1mol/LNaOH溶液滴定20mL0.1mol/LH2A溶液的滴定曲线如图所示。下列说法正确的是

A. a点所得溶液中:Vo=10mL
B. C点所得溶液中:c(A2-)=c(HA-)
C. b点所得溶液中:c(H2A)+c(H+)=c(HA-)+c(OH-)
D. d点所得溶液中:A2-的水解平衡常数K1=1×10-7.19
【答案】B
【解析】A、a点所得溶液中对H2A有:K1=c(H+)c(HA-)/c(H2A),10-1.85=10-1.85×c(HA-)/c(H2A)可得HA-与H2A的浓度相等,当V0=10mL时,生成的NaHA和剩余的H2A的物质的量相等,a点溶液显酸性,H2A的电离程度大于HA-的水解程度,故V0=10mL时混合溶液中的HA-和H2A的浓度不会相等,V0<10mL时才可能相等,A错误;B、C点所得溶液中:对HA-有K2=c(H+)xc(A2-)/c(HA-),10-7.19=10-7.19×c(A2-)/c(HA-)解得A2- 的浓度与HA-的浓度相等,B正确;C、b点加入的NaOH溶液体积为20mL,NaOH与H2A恰好完全反应生成NaHA,根据质子守恒有:c(H2A)+c(H+)=c(A2-)+ c(OH-),C错误;D、d点加入的NaOH的物质的量为H2A的物质的量的2倍,恰好生成Na2A,此时A2-第一步水解生成HA-,第一步水解的常数与H2A的第二电离常数的乘积为水的离子积常数,故第一步水解常数K1=1.0×10-14÷10-7.19=10-6.81,D错误。正确答案为B。


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】现有反应:CO(g)+H2O(g)CO2(g)+H2(g)△H<0,在850℃时,平衡常数K=1.现在850℃时,向2L的密闭容器中充入CO、H2O(g)各4mol,试回答下列问题(写出具体的计算过程):
(1)达平衡时,CO转化率为多少?
(2)H2的体积分数为多少?
(3)若温度仍为850℃,初始时CO浓度为2mol/L,H2O(g)为6mol/L,则平衡时CO转化率为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有5瓶失去标签的液体,已知它们可能是乙醇、乙酸、苯、乙酸乙酯、葡萄糖中的一种。现通过如下实验来确定各试剂瓶中所装液体的名称:
实验步骤和方法 | 实验现象 |
①把5瓶液体分别依次标号A、B、C、D、E,然后闻气味 | 只有E没有气味 |
②各取少量于试管中 ,加水稀释 | 只有C、D不溶解而浮在水面上 |
③分别取少量5种液体于试管中,加新制Cu(OH)2并加热 | 只有B使沉淀溶解,E中产生砖红色沉淀 |
④各取C、D少量于试管中,加稀NaOH溶液并加热 | 只有C仍有分层现象,且在D的试管中闻到特殊香味 |
(1)写出这6种物质的名称。
A____________ B____________ C____________ D____________ E____________
(2)在D中加入NaOH溶液并加热的化学方程式为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所示物质的工业制备方法合理的是
A. 制Si:SiO2![]() SiCl4
SiCl4![]() Si
Si
B. 制H2SO4:黄铁矿![]() SO2
SO2![]() H2SO3
H2SO3![]() H2SO4
H2SO4
C. 卤水中提取Mg:卤水(主要含MgCl2) ![]() Mg(OH)2
Mg(OH)2![]() …
…![]() MgCl2
MgCl2![]() Mg
Mg
D. 侯氏制碱法:饱和食盐水![]() NaHCO3(s)
NaHCO3(s) ![]() Na2CO3
Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依饮增大的四种短周期元素,A、B、C、D、F是由其中的两种或三种元素组成的化合物,E是由元素Z形成的单质,0.1mol/LD溶液的pH=13(25℃)。它们满足如图转化关系,则下列说法正确的是

A. 元素Z的最高正价为+6
B. F中含有共价键和离子键
C. 常温下,X、Y、Z、W四种元素组成的盐溶液的pH一定小于7
D. 0.1molB与足量C完全反应共转移电子数为0.2×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏伽德罗常数,下列说法中正确的是( ) ①常温常压下,17g甲基(﹣14CH3)所含的中子数为9NA
②常温常压下,22.4L NO气体的分子数小于NA
③室温下,28.0g乙烯和丙烯的混合气体中含有的共价键约为3×6.02×1023个
④7.2g CaO2中含有的阴离子数目约为6.02×1022
⑤标准状况时,22.4L氟化氢所含有的原子数为2NA
⑥标况下,7.8g苯中含有碳碳双键的数目为0.3NA .
A.①②⑥
B.②④⑤
C.②④
D.⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为周期表中短周期的一部分,W、X、Y、Z四种元素最外层电子数之和为24。下列说法正确的是
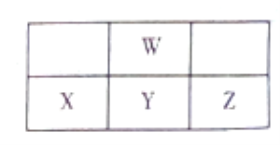
A. X、Y、Z的含氧酸的酸性依次增强
B. W元素形成的单核阴离子还原性强于X
C. Y、W形成的化合物一定能使酸性KMnO4溶液褪色
D. W与氢元素形成的化合物中可能含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述与图象对应符合的是( ) 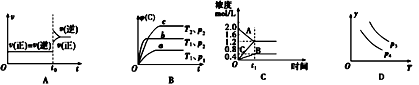
A.对于达到平衡状态的N2(g)+3H2(g)2NH3 (g)在t0时刻充入了一定量的NH3 , 平衡逆向移动
B.对于反应 2A(g)+B(g)C(g)+D(g)△H<0,p2>p1 , T1>T2
C.该图象表示的化学方程式为:2A═B+3C
D.对于反应 2X(g)+3Y(g)2Z(g)△H<0,y可以表示Y的百分含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见三大强酸,a的一种同素异形体的晶胞如图B(正四面体立体网状结构)所示. 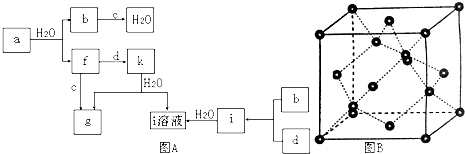
回答下列问题:
(1)图B对应的物质名称是 ,
(2)d中元素的原子核外电子排布式为 .
(3)图A中由二种元素组成的物质中,沸点最高的是 , 原因是 , 该物质的分子构型为 .
(4)图A中的双原子分子中,极性最大的分子是 .
(5)k的分子式为 , 中心原子的杂化轨道类型为 , 属于分子(填“极性”或“非极性”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com