
【题目】下列各项反应对应的图像正确的是( )


A.图甲为25℃时,向亚硫酸溶液中通入氯气
B.图乙为向NaAlO2溶液中通入HCl气体
C.图丙为向少量氯化铁溶液中加入铁粉
D.图丁为向BaSO4饱和溶液中加入硫酸钠
【答案】C
【解析】
A.亚硫酸为酸性,其pH小于7,与图象不符,发生Cl2+H2SO3+H2O=2Cl-+4H++SO42-后,随着氯气的通入,pH会降低,直到亚硫酸反应完全,pH不变,故A错误;
B.NaAlO2溶液中通入HCl气体,发生H++AlO2-+H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O,图中上升与下降段对应的横坐标长度之比应为1:3,故B错误;
C.向少量氯化铁溶液中加入铁粉,发生Fe+2FeCl3=3FeCl2,则Fe元素的质量增加,Cl元素的质量不变,所以Cl的质量分数减小,至反应结束不再变化,故C正确;
D.BaSO4饱和溶液中,存在溶解平衡,加硫酸钠,硫酸根离子浓度增大,溶解平衡逆向移动,溶解度减小,故D错误;
故答案为C。


科目:高中化学 来源: 题型:
【题目】火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会对环境造成严重影响。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为______________。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
①该反应的平衡常数表达式为_____________。
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如右图所示。
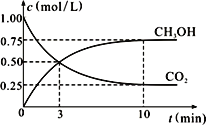
试回答:0~10 min内,氢气的平均反应速率为______________mol/(L·min)。
(3)脱硫。
①有学者想利用如图所示装置用原电池原理将SO2转化为重要的化工原料,A、B是惰性电极。
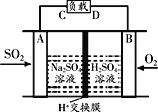
A极的电极反应式为_____________。
②某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物,可作为化肥。硫酸铵和硝酸铵的水溶液pH<7,常温下,向一定物质的量浓度的硝酸铵溶液中滴加适量的氨水溶液,使溶液中的NO3-和NH4+的物质的量浓度相等,则溶液的pH__________7(填写“>”“=”或“<”)。
(4)金属冶炼和金属化合物处理常涉及氧化还原反应。
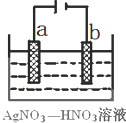
若用惰性电极电解饱和NaCl溶液一段时间当阳极产生56 mL(标准状况下)气体,电解后溶液体积为500 mL时,求所得溶液在25℃时的pH =__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能使H2O+H2O![]() H3O++OH-电离平衡向正反应方向移动,且所得溶液呈酸性的是
H3O++OH-电离平衡向正反应方向移动,且所得溶液呈酸性的是
A.在水中加Na2CO3固体B.在水中加入CuCl2固体
C.在水中加入稀硫酸D.将水加热到99℃,其中c(H+)=1×10-6mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜并制备氯化铁晶体的流程如下:
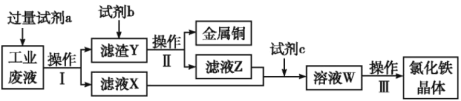
则下列说法正确的是( )
A.试剂a是铁、试剂b是稀硫酸
B.操作Ⅰ、操作Ⅱ、操作Ⅲ所用仪器相同
C.试剂c是氯气,相应的反应为2Fe2++Cl2═2Fe3++2Cl-
D.用酸性KMnO4溶液可检验溶液W中是否含有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述不正确的是( )
A.9g克13CO2与N217O的混合物中所含中子数为4.6NA
B.7.8克Na2O2中含有离子数为0.3NA
C.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA
D.5.6克铁与标况下2.24L氯气充分反应,转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中,不正确的是( )

A.HA的电离方程式为:HA=H++A- B.MOH为一元弱碱
C.K点对应的溶液中有:c(MOH)+c(M+)=0.02mol ![]() L-1 D.N点对应的溶液中有:c(M+)=c(A-)
L-1 D.N点对应的溶液中有:c(M+)=c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.含氨废水和废气对环境造成的污染越来越严重,某课外活动小组先测定废水中含NO3-为3×10-4 mol/L,而后用金属铝将NO3-还原为N2,从而消除污染。
(1)配平下列有关离子方程式:_____NO3-+_______Al+_______H2O→_______N2↑+______Al(OH)3+________OH-。
(2)上述反应中被还原的元素是____________,每生成2 molN2转移_________mol电子。
(3)有上述废水100 m3,若要完全消除污染,则所消耗金属铝的质量为_________g。
Ⅱ.NO与Cl2在常温常压下可以合成亚硝酰氯(NOCl)。它是一种红褐色液体或黄色气体,其熔点-64.5 ℃,沸点-5.5℃,遇水易水解。亚硝酰氯(NOCl)是有机合成中的重要试剂。实验室制备原料气Cl2的装置如图所示:
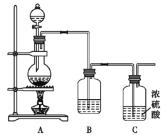
(4)实验室制Cl2时,装置A中烧瓶内发生反应的化学方程式为_________________________。
(5)将上述收集到的Cl2充入D的集气瓶中,按图示装置制备亚硝酰氯。
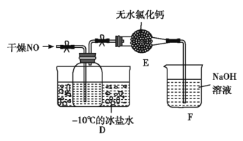
①装置D中发生的反应方程式为__________________________。
②如果不用装置E会引起什么后果:__________________。
③某同学认为装置F不能有效吸收尾气中的某种气体,该气体为_____________,为了充分吸收尾气,可将尾气与________________同时通入氢氧化钠溶液中。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25mL 0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是

A.在A、B间任一点(不含A、B点),溶液中可能有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.在D点,c(CH3COO-)+c(CH3COOH)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法可以证明反应![]()
![]() 已达到平衡状态的是
已达到平衡状态的是![]()
A.1个![]() 分解的同时,有3个
分解的同时,有3个![]() 的形成
的形成
B.1个![]() 分解的同时,有3个
分解的同时,有3个![]() 的分解
的分解
C.1个![]() 分解的同时,有1个
分解的同时,有1个![]() 的分解
的分解
D.1个![]() 分解的同时,有2个
分解的同时,有2个![]() 的形成
的形成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com