
【题目】Ⅰ.含氨废水和废气对环境造成的污染越来越严重,某课外活动小组先测定废水中含NO3-为3×10-4 mol/L,而后用金属铝将NO3-还原为N2,从而消除污染。
(1)配平下列有关离子方程式:_____NO3-+_______Al+_______H2O→_______N2↑+______Al(OH)3+________OH-。
(2)上述反应中被还原的元素是____________,每生成2 molN2转移_________mol电子。
(3)有上述废水100 m3,若要完全消除污染,则所消耗金属铝的质量为_________g。
Ⅱ.NO与Cl2在常温常压下可以合成亚硝酰氯(NOCl)。它是一种红褐色液体或黄色气体,其熔点-64.5 ℃,沸点-5.5℃,遇水易水解。亚硝酰氯(NOCl)是有机合成中的重要试剂。实验室制备原料气Cl2的装置如图所示:
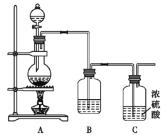
(4)实验室制Cl2时,装置A中烧瓶内发生反应的化学方程式为_________________________。
(5)将上述收集到的Cl2充入D的集气瓶中,按图示装置制备亚硝酰氯。
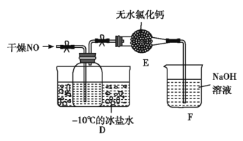
①装置D中发生的反应方程式为__________________________。
②如果不用装置E会引起什么后果:__________________。
③某同学认为装置F不能有效吸收尾气中的某种气体,该气体为_____________,为了充分吸收尾气,可将尾气与________________同时通入氢氧化钠溶液中。
【答案】6 10 18 3 10 6 N 20 1350 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 2NO+Cl2═2NOCl F中的水蒸气进入D装置中,会导致产品水解 NO O2
MnCl2+Cl2↑+2H2O 2NO+Cl2═2NOCl F中的水蒸气进入D装置中,会导致产品水解 NO O2
【解析】
Ⅰ.N元素化合价由+5降低为0,铝元素化合价由0升高为+3;根据反应的离子方程式计算消耗金属铝的质量;
Ⅱ.实验室在加热条件下用二氧化锰与浓盐酸反应制备氯气;NO与Cl2发生化合反应生成NOCl,根据NOCl遇水易水解分析装置E的作用;尾气中含有NO,NO不能与氢氧化钠溶液反应。
(1) N元素化合价由+5降低为0,铝元素化合价由0升高为+3,根据得失电子守恒、元素守恒、电荷守恒配平离子方程式为6NO3-+10Al+18H2O==3N2↑+10Al(OH)3+6OH-。
(2)上述反应中,N元素化合价由+5降低为0,被还原的元素是N,每生成2 molN2转移2mol×2×(5-0)=20mol电子。
(3) 100 m3废水含有NO3-的物质的量是100×103L×3×10-4 mol/L=30mol,设反应消耗铝的物质的量是n
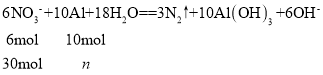
![]() =50mol,则所消耗金属铝的质量为50mol×27g/mol= 1350g。
=50mol,则所消耗金属铝的质量为50mol×27g/mol= 1350g。
(4) 实验室在加热条件下用二氧化锰与浓盐酸反应制备氯气,制Cl2时发生反应的化学方程式为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(5) ①装置D中NO与Cl2发生化合反应生成NOCl,发生的反应方程式为2NO+Cl2═2NOCl。
②NOCl遇水易水解,若没有E装置,F中的水蒸气进入D装置中,会导致产品水解。
③尾气中含有NO,NO不能与氢氧化钠溶液反应,该气体为NO,氧气与NO反应生成NO2,为了充分吸收尾气,可将尾气与O2同时通入氢氧化钠溶液中。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】以链烃A为原料合成两种高分子材料的路线如下图所示:
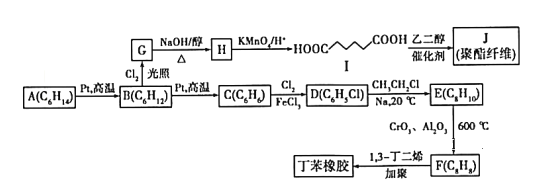
已知以下信息:①分子式A(C6H14)、B(C6H12) 、C(C6H6) 、D(C6H5Cl) 、E(C8H10) 、F(C8H8)
②B(C6H12)的核磁共振氢谱中只有1组峰,G为一氯代烃;
③R1-X+R2-X ![]() R1- R2 (X代表卤素原子,R1、R2代表烃基)。
R1- R2 (X代表卤素原子,R1、R2代表烃基)。
④![]()
![]()
![]() +R3-COOH(R1、R2、R3代表烃基)。
+R3-COOH(R1、R2、R3代表烃基)。
请回答以下问题:
(1) B的化学名称为______________________。
(2)由G生成H的化学方程式为_____________________。
(3)由C生成D的反应类型为_____________。
(4)F的结构简式为_________________。
(5)I的同分异构体中能同时满足下列条件的共有____________种(不含立体异构)。
①能与饱和NaHCO3溶液反应产生气体;②既能发生银镜反应,又能发生水解反应。其中核磁共振氢谱中有4组峰,且峰面积之比为6:2:1:1的是________(写出其中一种的结构简式)。
(6)参照上述合成路线,以2-甲基己烷和一氯甲烷为原料(无机试剂任选),设计制备化合物E的合成路线___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的A、B两种一元酸溶液各1mL, 分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示, 则下列说法正确的是

A. A、B两种酸溶液物质的量浓度一定相等
B. 稀释后A酸溶液的酸性比B酸溶液强
C. a = 5时, A是弱酸, B是强酸
D. 若A、B都是弱酸, 则5 > a > 2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项反应对应的图像正确的是( )


A.图甲为25℃时,向亚硫酸溶液中通入氯气
B.图乙为向NaAlO2溶液中通入HCl气体
C.图丙为向少量氯化铁溶液中加入铁粉
D.图丁为向BaSO4饱和溶液中加入硫酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年5月美国研究人员成功实现在常温常压下用氮气和水生产氨,原理如下图所示:
下列说法正确的是( )

A. 图中能量转化方式只有2种
B. H+向a极区移动
C. b极发生的电极反应为:N2+6H++6e-=2NH3
D. a极上每产生22.4LO2流过电极的电子数一定为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进入冬季北方开始供暖后,雾霾天气愈发严重,各地PM2.5、PM10经常“爆表”。引发雾霾天气的污染物中,最为常见的是机动车尾气中的氮氧化物和燃煤产生的烟气。
I、用NH3催化还原NOx可以消除氮氧化物的污染。反应原理为:NO(g)+NO2(g)+2NH3(g) ![]() 2N2(g)+3H2O(g)。
2N2(g)+3H2O(g)。
(1)该反应的△S________0(填“>”、“=”或“<”)。
(2)II、已知反应N2O4(g) ![]() 2NO2(g) △H,随温度升高,混合气体的颜色变深。将一定量N2O4气体充入绝热容器一段时间后,研究压缩和拉伸活塞过程中混合气体的气体的透光率(气体颜色越浅,透光率越大)随时间变化情况。下列说法能说明透光率不再发生改变的有________。
2NO2(g) △H,随温度升高,混合气体的颜色变深。将一定量N2O4气体充入绝热容器一段时间后,研究压缩和拉伸活塞过程中混合气体的气体的透光率(气体颜色越浅,透光率越大)随时间变化情况。下列说法能说明透光率不再发生改变的有________。
a.气体颜色不再改变b.△H不再改变
c.v正(N2O4)=2v逆(NO2)d.N2O4的转化率不再改变
(3)III、用CH4催化还原NOx也可以消除氮氧化物的污染。
已知:CH4(g)的标准燃烧热为-890kJ/mol,蒸发1mol H2O(l)需要吸收44kJ热量。
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=﹣1114 kJ/mol
2NO(g)+O2(g)=2NO2(g)△H=﹣114 kJ/mol
写出CH4催化还原NO2(g)生成N2和H2O(g)的热化学方程式:________。
(4)在温度为T1℃和T2℃时,分别将0.5mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得NO2的物质的量随时间变化数据如下表:
温度/℃ | 0 | 10 | 20 | 40 | 50 |
T1 | 1.2 | 0.9 | 0.7 | 0.4 | 0.4 |
T2 | 1.2 | 0.8 | 0.56 | … | 0.5 |
①温度为T1℃时,0~20min内,v(CH4)=________。
②温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2,达新平衡时CH4的转化率将________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是![]()
A.已知![]() 可溶于KI形成
可溶于KI形成![]() ,向两支盛有
,向两支盛有![]() 溶液的试管中,分别滴加淀粉溶液和
溶液的试管中,分别滴加淀粉溶液和![]() 溶液,前者溶液变蓝,后者有黄色沉淀,说明
溶液,前者溶液变蓝,后者有黄色沉淀,说明![]() 溶液中存在平衡:
溶液中存在平衡:![]()
B.物质的量浓度相等的![]() 和
和![]() 溶液等体积混合后的溶液:
溶液等体积混合后的溶液:![]()
C.已知:![]() ,
,![]() ,将等体积的浓度为
,将等体积的浓度为![]() 的
的![]() 溶液滴入到浓度均为
溶液滴入到浓度均为![]() 的KCl和
的KCl和![]() 的混合溶液中产生两种不同沉淀,且
的混合溶液中产生两种不同沉淀,且![]() 沉淀先产生
沉淀先产生
D.![]() 时,溶液中水电离出的
时,溶液中水电离出的![]() 和水电离出的
和水电离出的![]() 的乘积一定等于
的乘积一定等于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL某浓度的硫酸溶液中滴入0.1mol/L氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图。下列分析正确的是( )
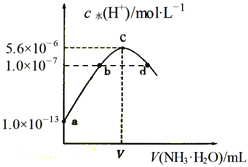
A. V=40
B. c点所示溶液中:c(H+ )-c(OH-)=2c(NH3·H2O)
C. NH3·H2O的电离常数K=10-4
D. d点所示溶液中:c(NH4+)=2c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种分解海水制氢气的方法为2H2O(l) ![]() 2H2(g)+O2(g)。下图为此反应的能量变化示意图,则下列说法错误的是
2H2(g)+O2(g)。下图为此反应的能量变化示意图,则下列说法错误的是

A.该反应正反应的活化能小于逆反应的活化能
B.TiO2可以提高H2O的分解速率
C.催化剂对该反应的反应热无影响
D.使用氢气作燃料有利于控制温室效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com