
【题目】下列有关说法正确的是![]()
A.已知![]() 可溶于KI形成
可溶于KI形成![]() ,向两支盛有
,向两支盛有![]() 溶液的试管中,分别滴加淀粉溶液和
溶液的试管中,分别滴加淀粉溶液和![]() 溶液,前者溶液变蓝,后者有黄色沉淀,说明
溶液,前者溶液变蓝,后者有黄色沉淀,说明![]() 溶液中存在平衡:
溶液中存在平衡:![]()
B.物质的量浓度相等的![]() 和
和![]() 溶液等体积混合后的溶液:
溶液等体积混合后的溶液:![]()
C.已知:![]() ,
,![]() ,将等体积的浓度为
,将等体积的浓度为![]() 的
的![]() 溶液滴入到浓度均为
溶液滴入到浓度均为![]() 的KCl和
的KCl和![]() 的混合溶液中产生两种不同沉淀,且
的混合溶液中产生两种不同沉淀,且![]() 沉淀先产生
沉淀先产生
D.![]() 时,溶液中水电离出的
时,溶液中水电离出的![]() 和水电离出的
和水电离出的![]() 的乘积一定等于
的乘积一定等于![]()
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】已知:2NO2(g)+CH4(g)![]() N2(g)+CO2(g)g+2H2O(g) △H,向容积为2 L的恒容密闭容器中,充入NO2和CH4的混合气体0.3 mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如图所示。[投料比X=
N2(g)+CO2(g)g+2H2O(g) △H,向容积为2 L的恒容密闭容器中,充入NO2和CH4的混合气体0.3 mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如图所示。[投料比X=![]() ];下列说法不正确的是
];下列说法不正确的是

A.△H<0
B.X>2
C.400K时,反应的平衡常数为5×10-2
D.投料比为2时,Q点v逆(CH4)小于P点的v逆(CH4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述不正确的是( )
A.9g克13CO2与N217O的混合物中所含中子数为4.6NA
B.7.8克Na2O2中含有离子数为0.3NA
C.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA
D.5.6克铁与标况下2.24L氯气充分反应,转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.含氨废水和废气对环境造成的污染越来越严重,某课外活动小组先测定废水中含NO3-为3×10-4 mol/L,而后用金属铝将NO3-还原为N2,从而消除污染。
(1)配平下列有关离子方程式:_____NO3-+_______Al+_______H2O→_______N2↑+______Al(OH)3+________OH-。
(2)上述反应中被还原的元素是____________,每生成2 molN2转移_________mol电子。
(3)有上述废水100 m3,若要完全消除污染,则所消耗金属铝的质量为_________g。
Ⅱ.NO与Cl2在常温常压下可以合成亚硝酰氯(NOCl)。它是一种红褐色液体或黄色气体,其熔点-64.5 ℃,沸点-5.5℃,遇水易水解。亚硝酰氯(NOCl)是有机合成中的重要试剂。实验室制备原料气Cl2的装置如图所示:
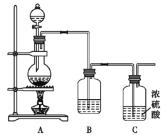
(4)实验室制Cl2时,装置A中烧瓶内发生反应的化学方程式为_________________________。
(5)将上述收集到的Cl2充入D的集气瓶中,按图示装置制备亚硝酰氯。
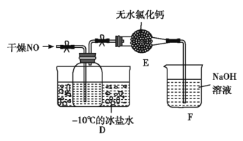
①装置D中发生的反应方程式为__________________________。
②如果不用装置E会引起什么后果:__________________。
③某同学认为装置F不能有效吸收尾气中的某种气体,该气体为_____________,为了充分吸收尾气,可将尾气与________________同时通入氢氧化钠溶液中。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.元素单质及其化合物有广泛用途,请根据周期表中第三周期元素知识回答问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是_________。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素为__________(填名称);氧化性最弱的简单阳离子是________________(填离子符号)。
(3)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是_________(填字母)。
a.NH3 b.HI c.SO2 d.CO2
(4)KClO3可用于实验室制O2,若不加催化剂,400 ℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:__________。
Ⅱ.氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙,甲和乙是二元化合物。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 L H2(已折算成标准状况)。甲与水反应也能产生H2,同时还产生一种白色沉淀物, 该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25 g/L。请回答下列问题:
(5)甲的化学式是___________________;乙的电子式是___________。
(6)甲与水反应的化学方程式是______________________。
(7)判断:甲与乙之间____________(填“可能”或“不可能”)发生反应产生H2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25mL 0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是

A.在A、B间任一点(不含A、B点),溶液中可能有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.在D点,c(CH3COO-)+c(CH3COOH)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸式盐NaHB在水溶液中,HB﹣的电离程度小于HB﹣的水解程度,下列说法正确的是( )
A.NaHB的存在抑制了水的电离
B.HB﹣水解方程式:HB﹣+H2O![]() H3O++B2﹣
H3O++B2﹣
C.相同物质的量浓度溶液的pH值:NaHB>Na2B
D.溶液中离子浓度大小为:c(Na+)>c(HB﹣)>c(OH﹣)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,下列反应不可能自发进行的是
A.2O3(g)=3O2(g) △H<0
B.CaCO3(s)=CaO(s)+CO2(g) △H>0
C.N2(g)+3H2(g) ![]() 2NH3(g) △H<0
2NH3(g) △H<0
D.2CO(g)=2C(s)+O2(g) △H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)暴露在空气中容易爆炸,但利用其制作的燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示,下列叙述正确的是( )

A. 电池工作时,正极附近的pH降低
B. 当消耗1 mol O2时,有2 mol Na+由甲槽向乙槽迁移
C. 负极反应为4OH-+N2H4-4e-===N2↑+4H2O
D. 若去掉阳离子交换膜,电池也能正常工作
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com