
����Ŀ����֪��2NO2(g)+CH4(g)![]() N2(g)+CO2(g)g+2H2O(g) ��H�����ݻ�Ϊ2 L�ĺ����ܱ������У�����NO2��CH4�Ļ������0.3 mol��ַ�Ӧ����ͬͶ�ϱ�ʱ��NO2��ƽ��ת�������¶ȵĹ�ϵ��ͼ��ʾ��[Ͷ�ϱ�X=
N2(g)+CO2(g)g+2H2O(g) ��H�����ݻ�Ϊ2 L�ĺ����ܱ������У�����NO2��CH4�Ļ������0.3 mol��ַ�Ӧ����ͬͶ�ϱ�ʱ��NO2��ƽ��ת�������¶ȵĹ�ϵ��ͼ��ʾ��[Ͷ�ϱ�X=![]() ]������˵������ȷ����
]������˵������ȷ����

A.��H<0
B.X>2
C.400Kʱ����Ӧ��ƽ�ⳣ��Ϊ5��10-2
D.Ͷ�ϱ�Ϊ2ʱ��Q��v��(CH4)С��P���v��(CH4)
���𰸡�C
��������
A���¶�����NO2��ƽ��ת���ʼ�С���������»�ѧƽ�������ȷ�Ӧ������У�����Ϊ���ȷ�Ӧ����˸÷�Ӧ������ӦΪ���ȷ�Ӧ����H<0��A��ȷ��
B�����ַ�Ӧ������һ�ַ�Ӧ���Ũ�ȣ��������һ�ַ�Ӧ���ת���ʣ��������ʱ�����ת���ʼ�С����ͬ�¶���Ͷ�ϱ�Ϊ2ʱ����������ת���ʴ���Ͷ�ϱ�ΪXʱ�Ķ�������ƽ��ת���ʣ�˵��X>2��B��ȷ��
C�����ݻ�Ϊ2 L�ĺ����ܱ������У�����NO2��CH4�Ļ������0.3 mol��ַ�Ӧ��400��CͶ�ϱ�Ϊ2ʱ�����������Ϊ0.2 mol������Ϊ0.1 mol����������ƽ��ת����50%����Ӧ��NO2�����ʵ�����0.1 mol���ı�Ũ��Ϊ��c(NO2)=![]() =0.05mol/L�����ݷ���ʽ�����ʷ�Ӧת����ϵ��֪��ƽ��ʱc(NO2)=
=0.05mol/L�����ݷ���ʽ�����ʷ�Ӧת����ϵ��֪��ƽ��ʱc(NO2)=![]() =0.05mol/L��c(CH4)=
=0.05mol/L��c(CH4)=![]() c(NO2)=0.025 mol/L��c(N2)=c(CO2)=
c(NO2)=0.025 mol/L��c(N2)=c(CO2)=![]() ��c(NO2)= 0.025 mol/L��c(H2O)=��c(NO2)= 0.05 mol/L�����Ի�ѧƽ�ⳣ��K=
��c(NO2)= 0.025 mol/L��c(H2O)=��c(NO2)= 0.05 mol/L�����Ի�ѧƽ�ⳣ��K=![]() =0.025��C����
=0.025��C����
D��Ͷ�ϱ�Ϊ2ʱ��Q��δ�ﵽƽ��״̬��P��Ϊƽ��״̬��Q����Ҫ�ﵽƽ��״̬����Ҫ��Ӧ������У���ʱ�淴Ӧ����С��P��ƽ��״̬�µ��淴Ӧ���ʣ���Q��v��(CH4)С��P���v��(CH4)��D��ȷ��
�ʺ���ѡ����C��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п���㷺Ӧ����ҽҩ�����ũҵ��������ҵ��������п����Ҫ�ɷ�ΪZnO������ZnSiO3��FeCO3��CuO�ȣ�����ZnSO47H2O��һ��������ͼ��

��1���������IJ�����____________��
��2������������ϡ����������ʱ���費��ͨ�����ˮ������Ŀ����______________��
��3���������У���pHԼΪ5.1����Һ�м��������أ�����Fe(OH)3��MnO(OH)2���ֳ������÷�Ӧ�����ӷ���ʽΪ____________________________________________��
��4���������У�����п�۵�������______________��
��5����֪����п���ܽ�����¶�֮��Ĺ�ϵ���±���
�¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 |
�ܽ��/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
������п��Һ�л������п�����ʵ�����Ϊ________________����ȴ�ᾧ�����ˡ���ɲ������ڼ�ѹ���������½��У�ԭ����_________________________________��
��6��ȡ28.70 g ZnSO47H2O��������ͬ�¶ȣ�ʣ�����������仯��ͼ��ʾ���������ݣ�680��ʱ���ù���Ļ�ѧʽΪ______��

a��ZnO b��Zn3O(SO4)2 c��ZnSO4 d��ZnSO4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A.��ӦN2(g)+3H2(g)![]() 2NH3(g)����H < 0����S <0
2NH3(g)����H < 0����S <0
B.���¸����ܵ��õ�������п����Լ����ܵ��ĸ�ʴ
C.�����£�Ksp=5.6��1012��pH=10�ĺ�Mg2+��Һ�У�c(Mg2+)��5.6��104 mol��L1
D.���³�ѹ�£�п��ϡH2SO4��Ӧ����11.2 L H2����Ӧ��ת�Ƶĵ�����Ϊ6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������AΪԭ�Ϻϳ����ָ߷��Ӳ��ϵ�·������ͼ��ʾ��
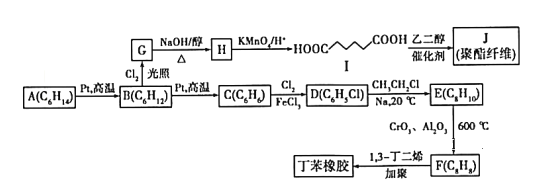
��֪������Ϣ���ٷ���ʽA(C6H14)��B(C6H12) ��C(C6H6) ��D(C6H5Cl) ��E(C8H10) ��F(C8H8)
��B(C6H12)�ĺ˴Ź���������ֻ��1��壬GΪһ�ȴ�����
��R1-X+R2-X ![]() R1- R2 (X����±��ԭ�ӣ�R1��R2��������)��
R1- R2 (X����±��ԭ�ӣ�R1��R2��������)��
��![]()
![]()
![]() +R3-COOH(R1��R2��R3��������)��
+R3-COOH(R1��R2��R3��������)��
��ش��������⣺
(1) B�Ļ�ѧ����Ϊ______________________��
(2)��G����H�Ļ�ѧ����ʽΪ_____________________��
(3)��C����D�ķ�Ӧ����Ϊ_____________��
(4)F�Ľṹ��ʽΪ_________________��
(5)I��ͬ���칹������ͬʱ�������������Ĺ���____________��(���������칹)��
�����뱥��NaHCO3��Һ��Ӧ�������壻�ڼ��ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ�����к˴Ź�����������4��壬�ҷ����֮��Ϊ6��2��1��1����________(д������һ�ֵĽṹ��ʽ)��
(6)���������ϳ�·�ߣ���2-�������һ�ȼ���Ϊԭ��(���Լ���ѡ)������Ʊ�������E�ĺϳ�·��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��г���10��Ԫ����Ԫ�����ڱ��е�λ�ã�
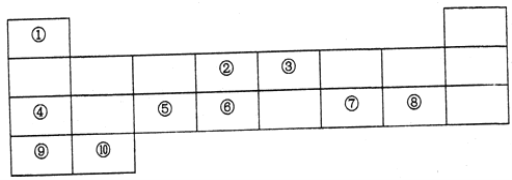
������Ӧ�Ļ�ѧ����ش��������⣺
��1��Ԫ�آ���Ԫ�����ڱ��д��ڵ�_____��������______�塣
��2������10��Ԫ���У���������ǿ��Ԫ�صķ���Ϊ_________������������Ӧˮ�����У�������ǿ�����ʵķ���ʽΪ ________��
��3���ڡ��ۡ�������Ԫ�ذ�ԭ�Ӱ뾶�ɴ�С��˳������Ϊ __________��
��4�����ڿ�����ȼ�յĻ�ѧ����ʽΪ ___________________ ��
��5��Ԫ�آܡ��ݵ�����������Ӧˮ�������Ӧ�����ӷ���ʽ�ֱ�Ϊ ________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�����ܱ������г���A(g)��B(g)��������ӦA(g)+B(g) ![]() 2C(g)+D(s)������ʵ���������±���
2C(g)+D(s)������ʵ���������±���
ʵ���� | �¶�/�� | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol | |
n(A) | n(B) | n(C) | ||
�� | 600 | 0.30 | 0.20 | 0.30 |
�� | 700 | 0.20 | 0.30 | 0.24 |
�� | 800 | 0.10 | 0.10 | a |
����˵������ȷ����
A. ʵ����У���5minʱ���n(B)=0.050mol����0��5minʱ����ƽ����Ӧ����v(A)=0.015mol/(L��min)
B. ʵ����дﵽƽ�������ѹǿ��A��ת���ʲ��䣬ƽ�ⳣ������
C. 700��ʱ�÷�Ӧ��ƽ�ⳣ��K=4.0
D. ʵ����У��ﵽƽ��ʱ��a>0.10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ (COCl2)��һ����Ҫ�Ļ���ԭ�ϣ�����ũҩ��ҽҩ����������ϵ���������ҵ��ͨ��Cl2(g) ��CO(g)![]() COCl2(g)�Ʊ�����ͼΪ�˷�Ӧ�ķ�Ӧ�������¶ȱ仯�����ߣ���ͼΪij��ģ��ʵ���о������������ڸ����ʵ�Ũ����ʱ��仯�����ߡ�����˵������ȷ����
COCl2(g)�Ʊ�����ͼΪ�˷�Ӧ�ķ�Ӧ�������¶ȱ仯�����ߣ���ͼΪij��ģ��ʵ���о������������ڸ����ʵ�Ũ����ʱ��仯�����ߡ�����˵������ȷ����
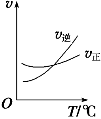
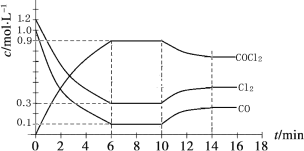
A��0~6 min�ڣ���Ӧ��ƽ������v(Cl2)��0.15 mol ��L��1��min ��1��
B���������¶Ȳ��䣬�ڵ�7 min ����ϵ�м������������ʸ�2 mol����ƽ��������Ӧ�����ƶ���
C�� ���¶����ߣ��÷�Ӧƽ�ⳣ����С;�Ƚϵ�8 min��Ӧ�¶�T(8)���15 min��Ӧ�¶�T(15)�ĸߵͣ�T(8) >T(15)��
D��������ʼͶ��Ũ�ȱ�Ϊc(Cl2)��0.7 mol/L��c(CO)��0.5 mol/L��c(COCl2)��0.5 mol/L�����ַ�Ӧ�¶Ȳ��䣬�����մﵽ��ѧƽ��ʱ��Cl2�����������������6 minʱCl2�����������ͬ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pH��2��A��B����һԪ����Һ��1mL, �ֱ��ˮϡ�͵�1000mL,����Һ��pH����Һ���(V)�Ĺ�ϵ��ͼ��ʾ, ������˵����ȷ����

A. A��B��������Һ���ʵ���Ũ��һ�����
B. ϡ�ͺ�A����Һ�����Ա�B����Һǿ
C. a �� 5ʱ, A������, B��ǿ��
D. ��A��B��������, ��5 > a > 2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����![]()
A.��֪![]() ������KI�γ�
������KI�γ�![]() ������֧ʢ��
������֧ʢ��![]() ��Һ���Թ��У��ֱ�μӵ�����Һ��
��Һ���Թ��У��ֱ�μӵ�����Һ��![]() ��Һ��ǰ����Һ�����������л�ɫ������˵��
��Һ��ǰ����Һ�����������л�ɫ������˵��![]() ��Һ�д���ƽ�⣺
��Һ�д���ƽ�⣺![]()
B.���ʵ���Ũ����ȵ�![]() ��
��![]() ��Һ�������Ϻ����Һ��
��Һ�������Ϻ����Һ��![]()
C.��֪��![]() ��
��![]() �����������Ũ��Ϊ
�����������Ũ��Ϊ![]() ��
��![]() ��Һ���뵽Ũ�Ⱦ�Ϊ
��Һ���뵽Ũ�Ⱦ�Ϊ![]() ��KCl��
��KCl��![]() �Ļ����Һ�в������ֲ�ͬ��������
�Ļ����Һ�в������ֲ�ͬ��������![]() �����Ȳ���
�����Ȳ���
D.![]() ʱ����Һ��ˮ�������
ʱ����Һ��ˮ�������![]() ��ˮ�������
��ˮ�������![]() �ij˻�һ������
�ij˻�һ������![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com