
【题目】利用废旧镀锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO,制备流程图如下:
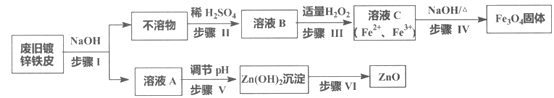
已知反应:①Zn+2NaOH=Na2ZnO2+H2↑ ②Zn(OH)2+2NaOH=Na2ZnO2+2H2O
回答下列问题:
(1)步骤I中的分离操作名称是_______,溶液A中的溶质有_______(填化学式)。
(2)步骤III中反应的离子方程式是___________________________________。
(3)步骤IV中反应的离子方程式是____________________________。
(4)步骤V可选用的试剂是_______(填序号)。
a. NaOH溶液 b. 氨水 c. 盐酸
(5)步骤VI的实验操作是______________。
【答案】过滤 Na2ZnO2、NaOH 2Fe2++2H++H2O2=2Fe3++2H2O Fe2++2Fe3++8OH-![]() Fe3O4+4H2O c 灼烧(或加热)
Fe3O4+4H2O c 灼烧(或加热)
【解析】
向废旧镀锌铁皮加入过量的NaOH溶液,发生反应,Zn溶解生成Na2ZnO2和H2,铁不溶解,过滤得到滤液A含有Na2ZnO2、NaOH,调节溶液pH生成Zn(OH)2沉淀,过滤、洗涤、灼烧得到ZnO,固体不溶物A是Fe,将其溶于稀硫酸反应产生FeSO4,向溶液中加入适量H2O2,调节溶液pH=1~2,部分Fe2+被氧化为Fe3+,得到含Fe2+、Fe3+的B溶液,加热促进水解生成Fe3O4胶体粒子。
(1) 步骤I是分离难溶性固体和可溶性液体混合物,该分离操作名称是过滤;溶液A中的溶质有Na2ZnO2、NaOH;
(2)步骤Ⅲ是H2O2在酸性溶液中氧化Fe2+为Fe3+,反应的离子方程式为:2Fe2++2H++H2O2═2Fe3++2H2O;
(3)步骤IV是向含有Fe2+、Fe3+的溶液中加入NaOH溶液,加热,发生反应产生Fe3O4,同时反应产生水,该反应的离子方程式是Fe2++2Fe3++8OH-![]() Fe3O4+4H2O;
Fe3O4+4H2O;
(4)溶液A含有Na2ZnO2、NaOH,若使Zn2+转化为Zn(OH)2沉淀,步骤Ⅴ是向该混合溶液中加入盐酸,调整溶液的pH,首先发生反应:HCl+NaOH=NaCl+H2O,然后发生:Na2ZnO2+2HCl =2NaCl+ Zn(OH)2↓;故合理选项是c;
(5)步骤VI的实验操作是将Zn(OH)2加热,Zn(OH)2发生分解反应:Zn(OH)2 ![]() ZnO+H2O,故步骤Ⅵ的实验操作是灼烧(或加热。
ZnO+H2O,故步骤Ⅵ的实验操作是灼烧(或加热。


科目:高中化学 来源: 题型:
【题目】四支试管分别充满O2、NO2、Cl2、NH3四种气体,把它们分别倒立于盛有下列各种液体的水槽中,发生的现象如图所示,其中充满NO2的试管是( )。
A. 
B. 
C. 
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3+→Fe2+;MnO![]() →Mn2+;Cl2→2Cl-;HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,则得到I2最多的是( )
→Mn2+;Cl2→2Cl-;HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,则得到I2最多的是( )
A. Fe3+ B. MnO![]() C. Cl2 D. HNO2
C. Cl2 D. HNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)![]() 2AB3(g) 化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)。下列判断正确的是( )
2AB3(g) 化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)。下列判断正确的是( )
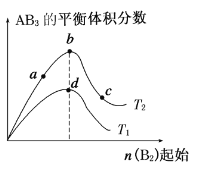
A.在T2和n(A2)不变时达到平衡,AB3的物质的量大小 为:c>b>a
B.若T2>T1,则正反应一定是放热反应
C.达到平衡时A2的转化率大小为:b>a>c
D.若T2>T1,达到平衡时b、d点的反应速率为vd>vb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用丁烷催化脱氢侧备丁烯:C4H10(g)![]() CH4(g)+H2(g)(正反应吸热)。将丁烷和氢气以一定的配比通过填充有催化剂的反应器(氢气的作用是活化催化剂),反应的平衡转化率、产率与温度、投料比有关。下列判断不正确的是
CH4(g)+H2(g)(正反应吸热)。将丁烷和氢气以一定的配比通过填充有催化剂的反应器(氢气的作用是活化催化剂),反应的平衡转化率、产率与温度、投料比有关。下列判断不正确的是
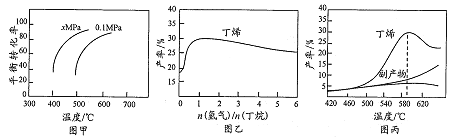
A. 由图甲可知,x小于0.1
B. 由图乙可知,丁烯产率先增大后减小,减小的原因是氢气是产物之一,随着n(氢气)/n(丁烷)增大,逆反应速 率减小
C. 由图丙可知产率在590℃之前随温度升高面增大的原因可能是溫度升高平衡正向移动
D. 由图丙可知,丁烯产率在590℃之后快速降低的主要原因为丁烯高温分解生成副产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
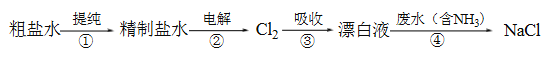
下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应式:①Fe+Cu2+═Fe2++Cu ②2Fe3++Cu═2Fe2++Cu2+可判断离子的氧化性从强到弱的顺序是( )
A. Fe2+、Fe3+、Cu2+ B. Fe2+、Cu2+、Fe3+
C. Cu2+、Fe2+、Fe3+ D. Fe3+、Cu2+、Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种常见化合物,已知它们包含的阳离子有K+、Ag+、Na+、Ba2+、Fe2+、Al3+,阴离子有Cl-、OH-、AlO2-、NO3-、SO42-、CO32-。将它们分别配成0.1mol·L-1的溶液进行如下实验:
①测得A、C、E溶液均呈碱性,且碱性A>E>C,E的焰色呈浅紫色(透过蓝色钴玻璃观察);②向B溶液中滴加稀氨水至过量,先生成沉淀,后沉淀全部溶解;③向F溶液中滴加稀硝酸,溶液变成棕黄色,且有无色气体生成;④向D溶液中滴加Ba(NO3)2溶液,无明显现象。
(1)写出A、D、E、F的化学式:A.________;D.________;E._______;F.________。
(2)用离子方程式解释C溶液呈碱性的原因:____________________________________。
(3)写出实验③中反应的离子方程式: ___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验现象及其解释不正确的是
A. 金属钠在Cl2中燃烧产生白烟,这是因为产生的NaCl固体颗粒分散到空气中所致
B. 把烧红的铁丝放在氧气中,发出耀眼白光,产生黑色固体,这是因为该反应放热多,生成的Fe3O4为黑色
C. 单质Mg、Al与O2反应,条件不同,可能产生不同的产物
D. 镁带在空气中点燃发出耀眼光芒,并发生三个反应:2Mg+O2![]() 2MgO、3Mg+N2
2MgO、3Mg+N2![]() Mg3N2、2Mg+CO2
Mg3N2、2Mg+CO2![]() 2MgO+C(黑色),Mg常用于照明弹。在这些反应中,Mg都是作还原剂
2MgO+C(黑色),Mg常用于照明弹。在这些反应中,Mg都是作还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com