
【题目】下列属于非氧化还原反应的是
A. 2H2O2![]() 2H2O +O2↑B. Cl2+H2O
2H2O +O2↑B. Cl2+H2O![]() HCl+HClO
HCl+HClO
C. SO2 + 2NaOH=Na2SO3 + H2OD. C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
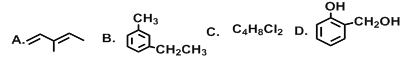

(1)G在同一直线上的碳原子数为___________;
(2)上述有机物互为同分异构体的是__________(填字母);
(3)A的系统命名为______________,它与Cl2以1:1比例反应时产物有_________种;
(4)上述有机物能与金属钠反应的是_________(填字母),能与碳酸氢钠反应的是______(填字母),B与酸性高锰酸钾反应的产物是______________(填结构简式);
(5)C的同分异构体有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种工业盐,在生产、生活中应用广泛,外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,但使用过量会使人中毒。某学习小组通过如下装置(夹持及加热装置略去)制取NaNO2样品并对样品含量进行测定
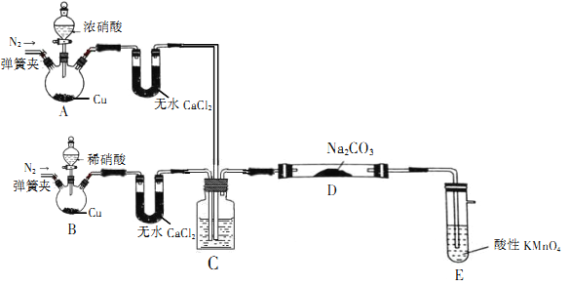
该小组先查阅资料知:NO、NO2能被酸性高锰酸钾氧化为NO3-。
(1)装置A中用于盛放浓硝酸的仪器名称为__________,装置D中发生的化学反应方程式为___________。
(2)①装置C中所装的液体需满足的条件是____________________。
②其作用为____________________。
(3)装置E的作用是____________________。
(4)为测定制得样品中NaNO2的含量,该实验中需配制KMnO4标准溶液并酸化,应选择__________(填化学式)来酸化KMnO4溶液。
(5)已知:在酸性溶液中,NO2-可将MnO4-还原为Mn2+。为测定样品中亚硝酸钠的含量,该小组称取4.0g样品溶于水配制成250mL溶液,取25.00mL溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液进行滴定,消耗20.00mL酸性KMnO4溶液(杂质不反应)。滴定过程中酸性KMnO4溶液的作用是____________________,所得样品中NaNO2的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯酚的叙述中,正确的是 ( )
A.纯净的苯酚是粉红色晶体B.苯酚不溶于水
C.苯比苯酚容易发生苯环上的取代反应D.可用浓溴水鉴别苯和苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)烷烃分子可看成由—CH3、—CH2—、![]() 和
和![]() 等结合而成的。试写出同时满足下列条件的烷烃的结构简式:___________ ,此烷烃可由烯烃加成得到,则该烯烃可能有___________种。
等结合而成的。试写出同时满足下列条件的烷烃的结构简式:___________ ,此烷烃可由烯烃加成得到,则该烯烃可能有___________种。
① 分子中同时存在上述4种基团;② 分子中所含碳原子数最少;
③ 该烷烃的一氯代物同分异构体的数目最少。
(2)碳原子数为8的单烯烃中,与HBr加成产物只有一种结构,符合条件的单烯烃有_______种。
(3)已知烯烃通过臭氧氧化并经锌和水处理得到醛或酮。例如:
 CH3CH2CHO+
CH3CH2CHO+
上述反应可用来推断烃分子中碳碳双键的位置。
某烃A的分子式为C6H10,经过上述转化生成![]() ,则烃A的结构可表示为_______________。
,则烃A的结构可表示为_______________。
(4) 请写出 物质与足量的金属钠发生反应的化学方程式_________。
物质与足量的金属钠发生反应的化学方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置由甲、乙两部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)2NH2]氧化为环境友好物质形成的化学电源;乙是利用装置甲模拟工业电解法来处理含Cr2O72-废水,电解过程中溶液发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。当电池工作时,下列说法错误的是

A. 甲中H+透过质子交换膜由左向右移动
B. 乙池中Fe棒应与甲池中的M极相连
C. M极电极反应式:H2N(CH2)2NH2+4H2O-16e-=2CO2↑+N2↑+16H+
D. 若溶液中减少了0.OlmolCr2O72-,则电路中至少转移了0.06 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中粒子的物质的量浓度关系正确的是( )
A. 0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO![]() )>c(HCO
)>c(HCO![]() )>c(OH-)
)>c(OH-)
B. 20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C. 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH![]() )+c(OH-)
)+c(OH-)
D. 0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中: c(OH-)>c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H为某合成药物的中间体,其合成路线如下:

已知:
① R-CH=CH-CH3 ![]() R-CH=CH-CH2-Br
R-CH=CH-CH2-Br
② RCH=CH2+HBr![]() RCH2CH2Br
RCH2CH2Br
回答下列问题:
(1)A的结构简式为_______。H中含有的含氧官能团名称是__________。
(2)F→G的反应类型为__________,设计C→D的目的为___________。
(3)D→E反应的化学方程式为_____________________________。
(4)M和N与G互为同分异构体。M含有苯环,苯环上有2个支链,且苯环上一氯代物只有2种,遇FeCl3溶液显紫色,能与新制Cu(OH)2悬浊液反应生成砖红色沉淀,则M有_____种(不考虑顺反异构)。N为芳香族化合物,0.5molN与足量银氨溶液反应生成2molAg,核磁共振氢谱显示其峰面积比为1:2:2,则N的结构简式为________。
(5)参考上述合成路线,以丙烯为原料(无机试剂任选)设计制备![]() 的合成路线____________________。
的合成路线____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com