
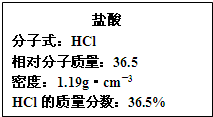
 �Իش��������⣺
�Իش��������⣺| V��1000mL��1.19g?cm-3��36.5% |
| 36.5mol/L |
| 11.9Vmol |
| VL |
| m(����) |
| m(��Һ) |
| ||
|


 һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
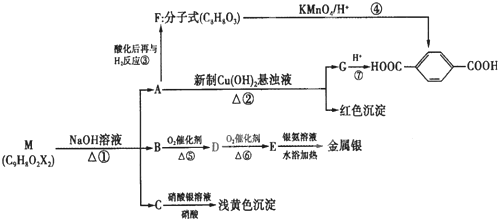




| ŨH2SO4 |
| �� |
| ŨH2SO4 |
| �� |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
- 2 |
| 3 |
| ||
| 3 |
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� |

| KMnO4 |
| H+ |










 ��
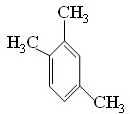
��
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪���淴Ӧ��AsO43-+2I-+2H+?AsO33-+I2+H2O�ݴ���Ƴ���ͼ��ʾ��ʵ��װ�ã�װ�������ŵ�������ʹ����װ���γ�һ���պϻ�·�����������²�����
��֪���淴Ӧ��AsO43-+2I-+2H+?AsO33-+I2+H2O�ݴ���Ƴ���ͼ��ʾ��ʵ��װ�ã�װ�������ŵ�������ʹ����װ���γ�һ���պϻ�·�����������²������鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com