
【题目】某模拟“人工树叶”电化学实验装置如下图所示、该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是

A. a电极的反应为: 3CO2 + 18H+-18e-= C3H8O+5H2O
B. 该装置将化学能转化为光能和电能
C. 该装置工作时H+从b极区向a极区迁移
D. 每生成1molO2,有44gCO2被还原
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】BaCl2xH2O是用途广泛的基础化工产品.我国目前主要是用盐酸和硫化钡(含少量Mg2+、Fe3+等)反应生产BaCl2xH2O,工艺流程如图所示.请回答: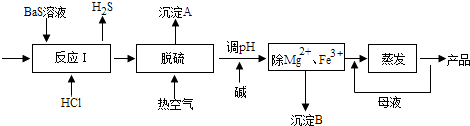
已知:室温时Ksp[Mg(OH)2]=1.8×10﹣11 Ksp[Fe(OH)3]=4.0×10﹣38
(1)反应I中生成的H2S用足量氨水吸收,一定条件下向所得溶液中通人空气,又可得到单质硫并使吸收液再生,再生反应的化学方程式为 .
(2)所得氯化钡粗液中含硫化合物(H2S、HS﹣等)影响产品质量,可鼓入预热后的空气吹除,预热空气的目的是;沉淀A的主要成分是 .
(3)热空气吹除时会有部分HS﹣转变为S2O32﹣ , 使产品仍不能达到纯度要求,可再行酸化脱硫,酸化脱硫时的离子方程式为 .
(4)室温时,为使Mg2+、Fe3+完全沉淀(当溶液中离子浓度小于1×l05molL﹣1时认为该离子完全沉淀),应将溶液的pH调至(只列算式)以上.
(5)实验室测定产品中x的步骤如下:
①准确称取12.23gBaCl2xH2O样品,加入l00mL稀盐酸加热溶解;
②边搅拌,边逐滴加入0.lmolL﹣1H2SO4溶液,待BaSO4完全沉淀,过滤,沉降后洗涤沉淀2﹣3次;
③将沉淀充分干燥后称量,质量为11.65g.
检验BaSO4沉淀是否洗涤干净的方法是;经计算x的数值为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化钾样品含少量的碳酸钾、硫酸钾和不溶于水的杂质,为了提纯氯化钾,先将样品溶于适量的水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作.下列说法正确的是( ) 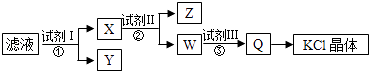
A.图示的步骤中必需要经过2次过滤操作
B.起始滤液呈中性
C.试剂Ⅱ为Na2CO3溶液
D.试剂Ⅲ为盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、铬都是用途广泛的金属.工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收金属铜和铬的流程如图甲,已知:部分物质沉淀的pH如表:
Fe3+ | Cu2+ | Cr3+ | |
开始沉淀pH | 2.1 | 4.7 | 4.3 |
完全沉淀pH | 3.2 | 6.7 | a |
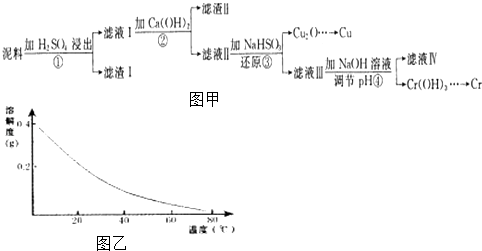
CaSO4的溶解度曲线如图乙,请回答下列问题:
(1)滤液I中所含溶质主要有(填化学式).
(2)第②步操作中,先加人Ca(OH)2调节溶液的pH,调节范围为 , 然后将浊液加热至80℃趁热过滤,所得滤渣Ⅱ的成分为 .
(3)第③步操作中,发现除了生成砖红色沉淀外,还产生了无色刺激性气味的气体.写出该步骤中发生反应的离子方程式
(4)当离子浓度≤1×10﹣5molL﹣1l时,可以认为离子沉淀完全.第④步操作中,若要使Cr3+完全沉淀,则室温下溶液中a的最小值为 . (已知Kap[Cr(OH)3]=6.3×10﹣31 , ![]() ≈4.0;lg4=0.6)
≈4.0;lg4=0.6)
(5)Cr(OH)3受热分解为Cr2O3 , 用铝热法可以冶炼金属铬.写出铝热法炼铬的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图甲、乙是电化学实验装置.
(1)若甲、乙两烧杯中均盛有饱和NaCl溶液.①甲中石墨棒上的电极反应式 , 电子的移动方向为 .
②乙中总反应的离子方程式为 , Cl﹣移向电极(填Fe或C).
③将湿润的淀粉﹣KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2 . 若反应中Cl2和I2的物质的量之比为5:1,且生成两种酸,该反应的化学方程式为: .
(2)如果起始时乙中盛有200mL pH=5的CuSO4溶液(25℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入CuO的质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1×105Pa和298K时,将1mol气态AB分子分离成气态A原子和B原子所需要的能量称为键能(kJ/mol)。下面是一些共价键的键能:(已知氨分子中有三个等价的氮氢共价键)
共价键 | H-H键 | N三N键 | N-H键 |
键能(kJ/mo1) | 436 | 945 | 391 |
工业合成氨的化学方程式:N2+3H2![]() 2NH3
2NH3
(1)断开1molN2中的化学键需_______(填“吸收”或“放出”)_____kJ能量;
(2)形成2molNH3中的化学键需_______(填“吸收”或“放出”)__kJ能量;
(3)在298K时,取1molN2和3molH2放入一密闭容器中,在催化剂存在下进行反应。理论上放出或吸收的热量为Q1,则Q1为_____kJ。根据上表中的数据判断工业合成氨的反应是_______(填“吸热”或“放热”)反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一些常见物质间的相互转化关系,其中F为金属,高温下能与某些金属氧化物反应,是工业冶炼金属的方法之一. A为无色气体,B为淡黄色固体,C为无色液体,E和J为无色气体单质.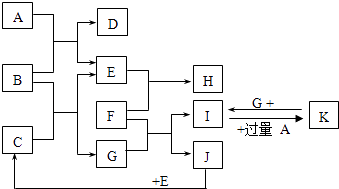
试回答下列问题:
(1)写出B的化学式: , 写出A的电子式;
(2)写出I→K的离子方程式;
(3)写出F与Fe3O4在高温下反应的化学方程式;
(4)已知3g J完全燃烧放出a kJ的热量,请写出表示J的燃烧热的热化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.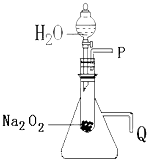
(1)由上述实验现象所推出的结论是:第一:有氧气生成;第二: . Na2O2跟水反应的化学方程式是 .
(2)某研究性学习小组拟用右图所示装置(气密性良好)进行实验,以证明上述结论.①用以验证第一条结论的实验操作及现象是:
②用以验证第二条结论的实验操作及现象是:
(3)实验(2)向试管中加水至固体完全溶解且不再有气泡生成后,滴入酚酞试液,发现溶液先变红后褪色,为探究其原因,该小组同学从查阅有关资料中得知:Na2O2与水反应可生成H2O2 , H2O2具有强氧化性和漂白性.请从另外一个角度(即不能再使用酸碱指示剂)设计一个简单的实验,验证Na2O2跟足量水充分反应后的溶液中有H2O2存在. .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com