
����Ŀ�����ĵ��ʼ��仯�������ʶ�������;�㷺�� ���������գ�
��1����ѧ�������о����ô������������ٷɻ�β���е�NO��COת���CO2��N2��2NO+2CO ![]() 2CO2+N2+Q��Q��0�� ij�¶��²�ø÷�Ӧ�ڲ�ͬʱ���COŨ�������
2CO2+N2+Q��Q��0�� ij�¶��²�ø÷�Ӧ�ڲ�ͬʱ���COŨ�������
ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
c��CO�� | 3.60��10��3 | 3.05��10��3 | 2.85��10��3 | 2.75��10��3 | 2.70��10��3 | 2.70��10��3 |
�÷�Ӧƽ�ⳣ��K�ı���ʽΪ���¶����ߣ�Kֵ��ѡ���������С���������䡱����ǰ2s�ڵ�ƽ����Ӧ����v��N2��=����������Ӧ���ܱ������з������ﵽƽ��ʱ�����NOת���ʵĴ�ʩ֮һ�� ��
��2����ҵ�ϳɰ��ķ�Ӧ�¶�ѡ��500�����ҵ�ԭ���� ��
��3��ʵ�����ڹ̶��ݻ����ܱ������м���1mol������3mol����ģ�ҵ�ϳɰ�����Ӧ��һ���������Ѵﵽƽ��ı�־�� �� a��N2��H2��NH3��Ũ��֮��Ϊ1��3��2
b�������ڵ�ѹǿ���ֲ���
c��N2��H2��NH3��Ũ�Ȳ��ٷ����仯
d����Ӧֹͣ�������淴Ӧ�����ʶ�������
��4����������1mol���ʵ�ϡ�����л���ͨ��1mol NH3����Һ����仯���Բ��ƣ�����Ӧ��������Һ������Ũ���ɴ�С��˳��������ͨ��NH3�Ĺ�������Һ�ĵ���������ѡ��������С�������������䡱����
���𰸡�
��1�� ����С��1.875��10��4mol/��L?s��������ѹǿ
����С��1.875��10��4mol/��L?s��������ѹǿ
��2��������500�����Ҿ�����ѻ���
��3��bc
��4��c��Cl��������NH4+����c��H+����c��OH��������������
���������⣺��1������ƽ�ⳣ������������Ũ�ȵ�ϵ������֮�����Է�ӦŨ��ϵ������֮��������K= ![]() ���÷�ӦΪ���ȷ�Ӧ���¶�ʱƽ�������ƶ�������ƽ�ⳣ����С��v��CO��=
���÷�ӦΪ���ȷ�Ӧ���¶�ʱƽ�������ƶ�������ƽ�ⳣ����С��v��CO��= ![]() =
= ![]() =3.75��10��4mol/l��v��N2��=
=3.75��10��4mol/l��v��N2��= ![]() =1.875��10��4mol/��Ls����һ��������ת���ʱ��˵��ƽ�������ƶ�����ͨ���ı�ѹǿ��ʹƽ�������ƶ������Դ��ǣ�
=1.875��10��4mol/��Ls����һ��������ת���ʱ��˵��ƽ�������ƶ�����ͨ���ı�ѹǿ��ʹƽ�������ƶ������Դ��ǣ� ![]() ����С��1.875��10��4mol/��Ls��������ѹǿ����2����ҵ�ϳɰ��ķ�Ӧ�ǿ���ģ�ѡ��500�����ҵĽϸ��¶���ʹ��Ӧ������У������ڻ�ѧƽ��������ƶ���ʹ�ø��¶���Ҫ�ǿ��Ǵ����Ĵ�Ч���Լ���Ӧ���ʵ�֪ʶ���ʴ��Ϊ��������500�����Ҿ�����ѻ��ԣ���3��a��N2��H2��NH3��Ũ��֮��Ϊ1��3��2�������Dz��䣬�ʴ���
����С��1.875��10��4mol/��Ls��������ѹǿ����2����ҵ�ϳɰ��ķ�Ӧ�ǿ���ģ�ѡ��500�����ҵĽϸ��¶���ʹ��Ӧ������У������ڻ�ѧƽ��������ƶ���ʹ�ø��¶���Ҫ�ǿ��Ǵ����Ĵ�Ч���Լ���Ӧ���ʵ�֪ʶ���ʴ��Ϊ��������500�����Ҿ�����ѻ��ԣ���3��a��N2��H2��NH3��Ũ��֮��Ϊ1��3��2�������Dz��䣬�ʴ���
b�������ڵ�ѹǿ���ֲ��䣬˵����������ʵ������䣬��Ӧ��ƽ��״̬������ȷ��
c��N2��H2��NH3��Ũ�Ȳ��ٷ����仯��˵�����淴Ӧ������ȣ���Ӧ��ƽ��״̬������ȷ��
d����ѧƽ��״̬�Ƕ�̬ƽ�⣬��Ӧ������ֹͣ���ʴ���
��ѡ��bc����4������ǡ�÷�Ӧ�����Ȼ�泥���Һ�����ԣ���c��H+����c��OH������������Һ�ʵ������У�c��H+��+c��NH4+��=c��OH����+c��Cl��������Ϊc��H+����c��OH��������c��NH4+����c��Cl������������Ũ�ȴ�С��ϵΪ��c��Cl��������NH4+����c��H+����c��OH��������Һ������Ũ�ȼ������䣬���Ե��������������䣬���Դ��ǣ�c��Cl��������NH4+����c��H+����c��OH�������������䣮
�����㾫����������Ҫ�����˻�ѧƽ��״̬���ʼ������ͻ�ѧƽ��״̬���жϵ����֪ʶ�㣬��Ҫ���ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч����״̬�жϣ���v(B��)=v(B��)��v(C��):v(D��)=x : y��c(C)��C%��n(C)%�Ȳ������A��B��C��DΪ���壬��m+n��x+y��ѹǿ�㶨����ϵ��ɫ�����λʱ����ij�����ڻ�ѧ���Ķ����������γ�������ϵƽ��ʽ���㶨��m+n �� x+y���Ȳ�����ȷ�����⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100��ʱ����0.200mol�������������������2L��յ��ܱ������У�ÿ��һ����ʱ��Ը������ڵ����ʽ��з������õ������
| 0 | 2 | 4 | 6 | 8 | 10 |
c��N2O4�� | 0.100 | c1 | 0.050 | c3 | a | b |
c��NO2�� | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
����գ�
��1���÷�Ӧ�ﵽƽ��ʱ��������������ת����Ϊ%������c2c3��ab�����������������=������
��2��2minʱ������������Ũ��c1=mol/L����0��2minʱ����ڣ�������������ƽ����Ӧ����Ϊmol/��Lmin����
��3��100��ʱ���÷�Ӧ��ƽ�ⳣ��K=
��4��������ͬ���������������������Ƕ����������壬Ҫ�ﵽ����ͬ����ƽ��״̬��������������ʼŨ����mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������ķ�����ᴿ����������ǣ� ��
A.�ù��˵ķ�������CaCO3��CaCl2��Һ�Ļ����
B.�ýᾧ���ᴿNaCl��KNO3������е�KNO3
C.���Ҵ���ȡ��ˮ�еĵ�
D.�ü��ȷ��������Ȼ��صĻ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ƭ�����������ð֢״����ṹ��ʽ��ͼ�������й�˵��������ǣ� �� 
A.����ҵķ���ʽΪC13H18O2
B.������뱽������ͬϵ��
C.1mol ������������3mol ���������ӳɷ�Ӧ
D.������ڱ����Ϸ���ȡ����Ӧ����һ�ȴ�����4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��뭡�뮡�밶�����Ԫ�ص�ԭ�ӣ�����Ϊ���Ǿ�����ͬ��
A.������B.������C.������D.������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ַ��������Ƶð�ɫ��Fe(OH)2����:
������һ���ò���Fe3+��FeSO4��Һ���ò���O2������ˮ���Ƶ�NaOH��Һ��Ӧ���Ʊ���
ʵ��������������������������FeSO4��Һʱ��һ����������ۺ�ϡ�������������۵�Ŀ����_____________��
��������������ͼ��ʾ��װ��������NaOH��Һ����м��ϡH2SO4���Լ����Ʊ���

��1��ʵ�鿪ʼʱ��ֹˮ��e��______(�������������ر���)�ġ�
��2����μ���װ���ڿ����Ѿ��ž�?________________��
��3���ž�װ���ڿ�����Ϊ���Ƶð�ɫFe(OH)2����������������________��
��4����������f�ŵ�Լ2/3Һ������ʱ�b��B���Լ�ƿ�з����Ļ�ѧ��Ӧ����ʽΪ________��
��5�����и�ͼʾ��________(�����)�ܽϳ�ʱ�俴��Fe(OH)2��ɫ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ���H+��Fe2+��Mg2+��Cu2+��NH4+��A13+��OH-��SO42- �е�һ�ֻ��֡�������һ�ֵ���ɫ���岢������Һʱ���д̼�����ζ������ų��Ͱ�ɫ�������������뵭��ɫ��������ʵ���(������)�����������Ͳ�����������ʵ���(������)�Ĺ�ϵ����ͼ��ʾ������д���пհ�:
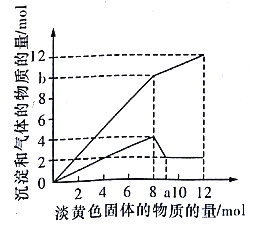
��1��ͼ��a���ֵ��__________�����ӵĵ���ɫ������_________ (�ѧʽ)��
��2������Һ�к��е�������_________��
��3����μ�����Һ�д��ڵ�������? _________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽�������巴Ӧ�ķ�Ӧԭ�����ؽ�������ʵ�飬����AΪ�ɾ���֧�ܵ��Թ��Ƴɵķ�Ӧ�����������¶˿���һ��С�ף�����ʯ���ޣ��ټ���������м�ۣ� 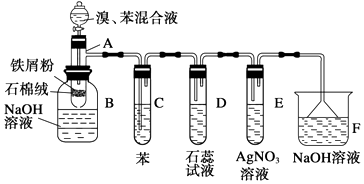
��д���пհף�
��1����Ӧ����A����μ�����ͱ��Ļ��Һ���������ھͷ�����Ӧ��д��A����������Ӧ�Ļ�ѧ����ʽ���л���д�ṹ��ʽ����
��2���Թ�C�б��������� �� ��Ӧ��ʼ�۲�D������ΪE������Ϊ
��3������װ���У����з��������õ�������������ĸ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȸʯ��Ҫ��Cu2��OH��2CO3 �� �Լ�����Fe��Si�Ļ���������ÿ�ȸʯΪԭ���Ʊ�������CuSO45H2O����������ͼ�� 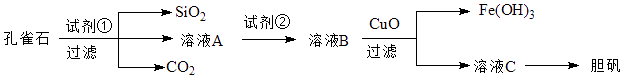
��ش��������⣺
��1���Լ�����һ�ֳ������ᣬд���仯ѧʽ �� ��������Ҫ�IJ���������
��2��ʵ���Ҽ���Fe3+�ij��÷����� ��
��3����ҺA�еĽ���������Cu2+��Fe2+��Fe3+ �� ������������Ҫ���Լ��ڽ���ҺA�е�Fe2+ȫ��ת��ΪFe3+ �� �Ӷ��γ���ҺB�����Լ����ܷ�����ˮ����ܡ����ܡ����������ܡ��������ԭ��
��4������ҺC��õ�������Ҫ�����������˵Ȳ�����
��5��ȡ25.00mL��ҺA����1.000��10��2mol/LKMnO4����Һ�ζ�����Ӧ���ӷ���ʽΪ��5Fe2++MnO4��+8H+��5Fe3++Mn2++4H2O�������ı���Һ20.00mL������ҺA��Fe2+��Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com