
【题目】中药药剂砒霜(主要成分As2O3,微溶于水)在医疗上用于治疗急性白血病。某课题组以一种含砷精矿石粉(主要成份为As4S4、As2S3、FeS2及其它惰性杂质)为原料制取As2O3,工艺流程图如下:

(1)过程 I 中所得SO2气体可回收再利用,下列有关SO2用途的说法正确的是_______。
A 工业制硫酸 B 漂白纸张 C 自来水消毒
(2)过程II中发生的反应_______氧化还原反应(填“是”或“不是”)。
(3)过程V中操作为_______(填实验基本操作名称)。
(4)①检验Na3AsO3溶液中是否含有Fe3+的实验操作_______。
②过程IV中生成As2O3的离子反应方程式为_______。
(5)有毒的AsO33-通过电解反应可转化为无毒的AsO43-。用石墨为电极,在强碱性溶液中电解含AsO33-的溶液,阳极的电极反应式为_______。
(6)测定某As2O3粗产品(含As2O5杂质)中As2O3的质量分数的实验过程如下:
a.称取m g粗产品溶解于NaOH溶液,得到含AsO33-、AsO43-的混合溶液100mL。
b.分别移取25.00mL上述溶液,用0.02500mol·L1的I2标准溶液进行滴定(I2将AsO33-氧化为AsO43-,淀粉溶液为指示剂)。每次滴定开始时液面读数如图一所示,三次滴定结束时,I2 标准溶液液面读数如图二~图四所示。

①描述滴定终点的现象_______。
②粗产品中As2O3的质量分数为_______(用含有m的代数式表示)。
【答案】AB 不是 过滤、洗涤、干燥 取Na3AsO3溶液少许,加入少量KSCN溶液,若溶液变为血红色,则说明该溶液中含有Fe3+ 2AsO43-+2SO2+2H+=As2O3↓+2SO42-+H2O 2OH-+AsO33--2e-=AsO43-+H2O 溶液由无色变为蓝色,且半分钟内不再变化 ![]()
【解析】
(1)SO2可以用来合成硫酸、漂白纸张,但是不能作自来水的消毒剂;
(2)氧化还原反应的特征是化合价的变化,可以从元素的化合价是否变化着手分析;
(3)含As2O3的悬浊液经过滤、洗涤、干燥,可得As2O3固体;
(4)①检验Fe3+,一般使用KSCN溶液,若溶液中有Fe3+,对应的现象是溶液变为血红色;
②过程IV中,SO2和Na3AsO4溶液在H2SO4的所用下反应生成As2O3,据此写出离子方程式;
(5)阳极发生氧化反应,由于电解质溶液呈碱性,故阳极的电极反应为:2OH-+AsO33--2e-=AsO43-+H2O;
(6)①该实验中,I2将AsO33-氧化为 AsO43-,淀粉作指示剂,则滴定终点的现象是溶液由无色变为蓝色,且半分钟内不再变化;
②根据AsO33-~I2,进行相关计算。
(1)SO2可以用来合成硫酸、漂白纸张,但是不能作自来水的消毒剂,故选AB;
(2)Fe2O3不和NaOH溶液反应,As2O3和NaOH溶液反应生成Na3AsO3,这两种含As的化合物中,As都呈+3价,该过程不涉及化合价的变化,则该反应不是氧化还原反应;
(3)由含As2O3的悬浊液得到As2O3固体,需要经过过滤、洗涤、干燥;
(4)①检验Na3AsO3溶液中是否含有Fe3+的实验操作是:取Na3AsO3溶液少许,加入少量KSCN溶液,若溶液变为血红色,则说明该溶液中含有Fe3+;
②过程IV中,SO2和Na3AsO4溶液在H2SO4的所用下反应生成As2O3,相关的离子反应方程式为:2AsO43-+2SO2+2H+=As2O3↓+2SO42-+H2O;
(5)阳极发生氧化反应,由于电解质溶液呈碱性,故阳极的电极反应为:2OH-+AsO33--2e-=AsO43-+H2O;
(6)①该实验中,I2将AsO33-氧化为 AsO43-,淀粉作指示剂,则滴定终点的现象是溶液由无色变为蓝色,且半分钟内不再变化;
②由图可知,三次滴定所用的溶液体积分别为19.90mL、18.50mL(舍去)、20.10mL,则所用溶液体积平均为20.00mL;则25.00mL的溶液消耗I2 0.5mmol(=20.00mL×0.025mol·L1),由于AsO33-~I2,故25.00mL的溶液中含有0.5mmol AsO33-,则100mL溶液中含有2mmol AsO33-,根据As元素守恒可得,m g粗产品中含1mmol As2O3,故粗产品中As2O3的质量分数为:![]() =
=![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是( )
A.标准状况下0.5molNT3分子中所含中子数为6.5NA
B.0.1molFe与0.1molCl2完全反应后,转移的电子数为0.2NA
C.13.35gAlCl3水解形成的Al(OH)3胶体粒子数小于0.1NA
D.一定条件下的密闭容器中,2molSO2和1molO2催化反应充分发生后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态链烃能使溴水褪色,经测定0.1 mol该烃充分燃烧可以生成7.2 g水,请据此回答下列问题。
(1)通过计算确定该烃具有的分子式__________。
(2)请写出满足上述条件的所有物质的同分异构体并用系统命名法命名__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(分子式 N2H4,沸点 113.5℃)是一种良好的火箭燃料,是一种易溶 于水和醇类等有机溶剂的无色油状液体。在工业上有重要用途。实验室可用如下 装置(略去部分夹持装置)模拟利用氨气和次氯酸钠合成肼的过程。
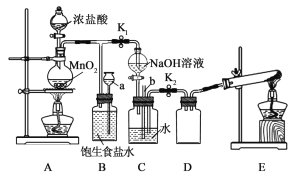
(1)装置 A 可用来制备 Cl2,装置 B 中饱和食盐水的作用是_____,当合成肼的反应结束时关闭止水夹 K1,装置 B 可以观察到的实验现象_____。
(2)装置 C 中长玻璃导管 b 与装置 B 中的_____(填仪器名称)的作用相同。
(3)装置 E 中可用熟石灰和氯化铵制备 NH3,反应的化学方程式为_____
(4)当反应一段时间,关闭两个止水夹,打开装置 C 中分液漏斗的活塞,将溶液 全部滴入集气瓶中,反应生成肼。反应的离子方程式为_____。 有同学说装置 D 没有什么作用,若去掉装置 D,对实验是否有影响?请说明理由:___________。
(5)将足量的 Cl2 与含有 0.4mol NaOH 的水溶液反应,分液漏斗中液体全部滴入 C 中,并向 C 中通入标准状况下的 13.44L NH3,从 C 中蒸馏分离得到 3.6g 液态肼, 则该实验中肼的实验产率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃类化合物A在一定条件下可发生如图转化。
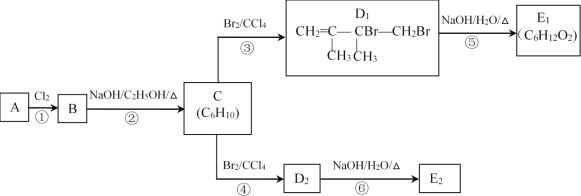
已知:A的质谱图表明其相对分子质量为84,其核磁共振氢谱只有一种氢。E1、E2互为同分异构体。
(1)D1是否存在顺反异构___(填“是”或“否”)。
(2)①至⑥的反应中,属于加成反应的是___。
(3)C的化学名称是___。
(4)写出A在一定条件下发生加聚反应的化学方程式___。
(5)E2的结构简式为___。
(6)写出反应②的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能存在![]() 、
、![]() 、
、![]() 、
、![]() 、Cl
、Cl![]() 、
、![]() 六种离子中的几种.现进行下列实验:
六种离子中的几种.现进行下列实验:
①取少量溶液滴加KSCN溶液,溶液呈血红色;
②另取少量原溶液滴加盐酸,溶液的棕黄色加深.
据此可以推断,该溶液中肯定不存在的离子是![]()
A.![]() 、
、![]() 、
、![]() B.
B.![]() 、
、![]() 、
、![]()
C.![]() 、
、![]() D.
D.![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基于新材料及3D打印技术,科学家研制出一种微胶囊吸收剂,它能将工厂排放的CO)以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充有Na2CO3溶液,其原理如图所示。
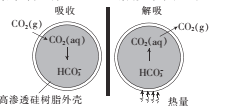
(1)这种微胶囊吸收CO2的原理是 ____用离子方程式表示),此过程是_____填“吸收”或“放出”)能量的过程。
(2)在吸收过程中下列关于胶囊内溶液的说法正确的是 ___(填字母)。
a.吸收前溶液中c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
b.吸收过程中,体系中的含碳微粒只有CO32-、HCO3-、H2CO3
c.当n(CO2):n(Na2CO3)=1:3时,溶液中c(CO32-)<c(HCO3-)
d.溶液中始终有c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
(3)将解吸后的CO2催化加氢可制取乙烯。
已知:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) △H1=-1323kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H2=-483.6kJ·mol-1
2CO2(g)+6H2(g)=C2H4(g)+4H2O(g) △H3=_______________
(4)在体积为2L的恒容容器中发生反应:2CO2(g)+6H2(g)=C2H4(g)+4H2O(g)。当投料为1 mol CO2(g)和3molH2 (g)时,测得温度对CO2平衡转化率的影响为曲线a,改变投料比![]() 测量后得到曲线b。
测量后得到曲线b。
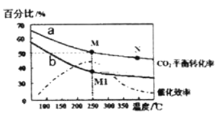
①根据曲线a计算250℃时该反应的化学平衡常数K= ____代入数值列出计算式即可)。
②b条件下投料比![]() ____(填“>” “<”或“=”)3,判断依据是 __ 。
____(填“>” “<”或“=”)3,判断依据是 __ 。
③下列说法正确的是 ___(填字母)。
A.平衡常数大小:M>N>M1
B.其他条件不变,b条件时增加催化剂用量,则250℃时CO2的平衡转化率可能达到M
C.当压强、混合气体的密度或![]() 不变时均可视为化学反应已达到平衡状态
不变时均可视为化学反应已达到平衡状态
D.工业生产中采取较高温度(250℃左右)是为了提高催化剂活性加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种常见药物①阿司匹林②青霉素③胃舒平④麻黄碱。请回答:
(1)某同学胃酸过多,应选用的药物是___(填序号),抗酸药的成分Al(OH)3中和胃酸过多的离子方程式为___。
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是___(填序号,下同)。
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是___。
(4)阿司匹林药品标签上贴有OTC,它表示___, 滥用药物会导致不良后果,如过量服用___会出现水杨酸中毒,应立即停药,并静脉注射NaHCO3溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中能大量共存的是( )
A.遇甲基橙变红的溶液中:K+、Na+、Cl-、SiO32-
B.0.1molL-1NaA1O2溶液中:Na+、NO3-、NH4+、HCO3-
C.常温下,![]() =1012的溶液中:SO32-、SO42-、Na+、Br-
=1012的溶液中:SO32-、SO42-、Na+、Br-
D.澄清透明的溶液中:Fe3+、A13+、I-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com