
【题目】将SO2通入足量Fe2(SO4)3溶液中,完全反应后再加入K2CrO4溶液,发生的两个化学反应为SO2+2Fe3++2H2O=SO42-+2Fe2++W ①,Cr2O72-+aFe2++bH+![]() Cr3++Fe3++H2O ②,下列有关说法正确的是
Cr3++Fe3++H2O ②,下列有关说法正确的是
A. 还原性:Cr3+>SO2 B. 配平后方程式②中,a=6,b=7
C. Cr2O72-能将Na2SO3氧化成Na2SO4 D. 方程式①中W为OH-
【答案】C
【解析】
由反应①②中各元素的价态变化可知,反应①中,SO2为还原剂,Fe3+为氧化剂,且还原性为SO2>Fe2+,氧化性为Fe3+>SO42-。反应②中,Fe2+为还原剂,Cr2O72-为氧化剂,且还原性为Fe2+>Cr3+,氧化性为Cr2O72->Fe3+。由此可见选项A错误。选项B,配平反应②:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,故a=6,b=14,错误。选项C,由于Cr2O72-具有氧化性,Na2SO3具有还原性,故Cr2O72-能将Na2SO3氧化成Na2SO4,正确。选项D,根据质量守恒定律,可知反应①中W为H+,错误。


科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与 H2O(g)发生反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时φ(CH4)的体积分数与 Z 和 T(温度)的关系如图所示。下列说法正确的是
=Z,在恒压下,平衡时φ(CH4)的体积分数与 Z 和 T(温度)的关系如图所示。下列说法正确的是

A. 该反应的焓变 ΔH>0
B. 图中 Z 的大小为 a>3>b
C. 图中 X 点对应的平衡混合物中![]()
D. 温度不变时,图中X 点对应的平衡在加压后φ(CH4)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂和氮的相关化合物在化工、医药、材料等领域有着广泛的应用。请回答下列问题
(1)Li的氢标电势是最负的,达到-3.045V,与水有很大的反应倾向,然而将Li单质加入水中,其反应烈程度远不如其他碱金属,试解释原因__________。
(2)基态氮原子中,核外电子占据的最高能层的符号为_______,核外电子能量最高的电子的电子云轮廓图形状为_________。
(3)氮元素既可与其他元素形成正离子,比如N2O5结构中存在NO2+的结构,其空间构型为__________,氮原子的杂化形式为____________;它也可以形成全氮的正离子,比如N5AsF6中存在高能量的N5+,N5+的空间构型为_______。(每个N原子都满足8电子稳定结构)
(4)下图为一种N和Li形成的二元化合物的晶体结构,试在图中画出其晶胞_____,并写出该化合物的化学式_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以CH4为原料制备H2的原理为CH4(g)+H2O(g)![]() CO(g)+3H2(g)。在一定条件下向a、b两个恒温恒容的密闭容器中均通入1.1molCH4(g)和1.1molH2O(g),测得两容器中CO的物质的量随时间的变化曲线分别为a和b。已知容器a的体积为10L,温度为Ta,下列说法不正确的是
CO(g)+3H2(g)。在一定条件下向a、b两个恒温恒容的密闭容器中均通入1.1molCH4(g)和1.1molH2O(g),测得两容器中CO的物质的量随时间的变化曲线分别为a和b。已知容器a的体积为10L,温度为Ta,下列说法不正确的是
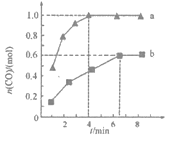
A. 容器a中CH4从反应开始到怡好平衡时的平均反应速率为0.025mol·L-1·min-1
B. a、b两容器的温度可能相同
C. 在达到平衡前,容器a的压强逐渐增大
D. 该反应在Ta温度下的平衡常数为27(mol·L-1)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类对锡(50Sn)的使用有悠久的历史,可以追溯到大约公元前3000年,但这也是对锡的“异常”不断加深认识,不断“驯服”它的历史。
(1)锡与硅同主族,稳定化合价均为+4价,锡原子比硅原子核外多2个电子层,锡元素在周期表中的位置为___________________。
(2)锡单质在常温下稳定(主要单质类别为白锡),但是它既怕冷又怕热。在-13.2℃以下,白锡转变成一种无定形的灰锡(粉末状),而且只要白锡接触到很少的灰锡。很失就会变成灰锡完全毁坏,就像得了瘟疫一样。
①克服锡单质这一弱点的方法之一就是做成合金,合金与组分金属相比一般具有____性质。
a.不导电 b硬度大 c.耐腐蚀
②对锡器的“瘟疫”作分析,以下推测合理的是_________________。
a.灰锡携带病毒
b.灰锡与白锡形成原电池,加速白锡的转化
c.灰锡是白锡转化的催化剂,加速反应
(3)实验室配制氯化亚锡(SnCl2)溶液时发现,向SnCl2固体中加水的过程中,产生刺激性气味气体,且只能得到悬浊液。配制、保存SnCl2溶液时,要用到的试剂为氯化亚锡固体、__________、______________和水(填试剂名称)。
(4)工业上,硫离子是一种很好的沉淀剂。但向1L 0.01 mol·L-1硫化钠溶液(pH=12)中逐渐加入SnCl2粉末时,一开始却并没观察至沉淀。请分析原因_________________。当加SnCl2至溶液pH=9时,有两种沉淀生成。此时溶液中硫离子浓度为__________(保留两位有效数字)。(提示:25℃时,Ksp[Sn(OH)2]=1.4×10-28,Ksp(SnS)=1.0×10-25。 Sn(OH)2 是两性物质。)
(5)测定固体中锡的含量时,常用的一种方法为:在强酸性环境中将固体溶解,然后将锡元素全部转化成Sn2+,以淀粉为指示剂,用碘酸钾标准溶液滴定。但在滴定初始并没有出现蓝色,滴定终点的现象为无色变蓝色。写出滴定过程中依次发生反应的离子反应方程式_______________,______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-选修3:物质结构与性质]固体电解质有广泛的用途。研究发现,晶体中有特殊结构为离子(如Li+)提供快速迁移的通道或者有“点缺陷”。都能使其具有导电潜力,比如:图(a)所示的锂超离子导体Li3SBF4和图(b)所示的有“点缺陷”的NaCl。
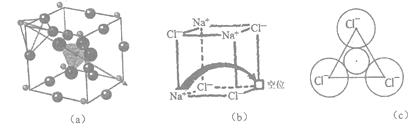
根据所学知识回答下列问题:
(1)在变化“Cl+e-→Cl-”过程中,所得电子填充在基态 Cl的________能级,此过程会________ (填“吸收”或“释放”)能量。
(2)BF4-中B的杂化形式为________________,其等电子体为___________(任写一种)。与其VSEPR模型相同,且有l对孤电子对的相对分子质量最小的分子是___________。
(3)图(a)所示晶胞中Li+位于_____位置;若将晶体中BF4-换成F-,导电能力会明显降低,原因是______________________________。
(4)图(6)中,若缺陷处填充了Na+,则它__________(填“是”或“不是”) NaCl的晶胞,在NaCl晶体中,Na+填充在Cl-堆积而成的__________面体空隙中。
(5)有人认为:高温下有“点缺陷”的NaCl晶伙导电性增照是由于Na+迁移到另一空位而造成。其中Na+经过一个由3个Cl-组成的最小三角形窗孔(如图c所示)。已知晶胞参数a=564 pm,r(Na+)=116pm, r(Cl-)=167 pm,通过计算三角形窗孔半径,判断该认识是否正确。__________。(已知:![]() ≈1.414,
≈1.414,![]() ≈1.732)
≈1.732)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的固定是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值。
反应 | 大气固氮 | 工业固氮 | |||
温度/℃ | 27 | 2000 | 25[ | 400 | 450 |
K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
①分析数据可知:大气固氮反应属于__________(填“吸热”或“放热”)反应。
②分析数据可知:人类不适合大规模模拟大气固氮的原因__________。
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因_______________________。
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,下图所示的图示中,正确的是______(填“A”或“B”);比较р1、р2的大小关系_______。

(3)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(1)![]() 4NH3(g)+3O2(g),则其反应热ΔH=___________________。
4NH3(g)+3O2(g),则其反应热ΔH=___________________。
(已知:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ·mol-1
2NH3(g) △H=-92.4kJ·mol-1
2H2(g) +O2(g)![]() 2H2O(l) △H=-571.6kJ·mol-1 )
2H2O(l) △H=-571.6kJ·mol-1 )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com