

| A、1mol M与氢氧化钠溶液反应完全,消耗3molNaOH |
| B、M不能与碳酸钠溶液反应 |
| C、M既能与乙酸反应,又能与乙醇反应 |
| D、1mol M分别与Na和NaHCO3完全反应时,产生气体的物质的量之比为3:1 |


科目:高中化学 来源: 题型:
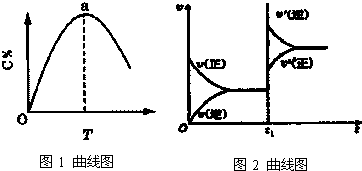
| A、m+n>p+q Q>0 |
| B、m+n>p+q Q<0 |
| C、m+n<p+q Q>0 |
| D、m+n<p+q Q<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、木糖醇与葡萄糖、果糖不一样,它不属于单糖 |
| B、木糖醇不能跟新制的Cu(OH)2反应生成砖红色沉淀 |
| C、木糖醇与乙醇属于同系物 |
| D、木糖醇是一种五元醇,可以与羧酸在一定条件下发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已经制得I(NO3)3、I(ClO4)3?2H2O等含I3+的化合物 |
| B、已经制得IBr、ICl 等卤素互化物 |
| C、碘易溶于KI溶液形成I3- |
| D、I4O9可以看成是碘酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间 | c(CO)/mol?L-1 | C(H2)/mol?L-1 | c(CH3OH)/mol?L-1 |
| 起始 | 1 | 3 | 0 |
| 第2min | 0.8 | 2.6 | 0.2 |
| 第4min | 0.4 | 1.8 | 0.6 |
| 第6min | 0.4 | 1.8 | 0.6 |
| A、第2min时,如果只改变某一条件,则改变的条件可能是降低温度 |
| B、第4min至第6 min该化学反应处于平衡状态 |
| C、第2min时,如果只改变某一条件,则改变的条件可能是使用催化剂 |
| D、第6min时,其他条件不变,如果升高温度,正逆反应速率均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 550 | 650 | 750 | 850 | 897 |
| 压强/Pa | 5.32×10 | 9.17×102 | 8.37×103 | 4.34×104 | 1.01×105 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com