
��һ���Ϊ10L���ܱտ����У�ͨ��һ������CO��H2O����85�淢�����·�Ӧ��
CO (g)+H2O(g)  CO2(g)+H2(g) ��H<O��
CO2(g)+H2(g) ��H<O��
CO��H2OŨ�ȱ仯��ͼ��ʾ��

��ش��������⣺
��1�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������___________________(��ѡ����ţ���
a��������ѹǿ����
b�����������c(CO)����
c�� ��(H2)=
��(H2)=  ��(H2O)
��(H2O)
d��c(CO2)=c(CO)
e�������������ܶȲ���
f��1 mol H-H�����ѵ�ͬʱ����2 mol H-O��
��2����0��4min�ڵ�ƽ����Ӧ���� (CO)=___________mol��L��1��min��1;
(CO)=___________mol��L��1��min��1;
��85��ʱ���÷�Ӧ��ѧƽ�ⳣ��K=____________��
��3��85��ʱ������ʼʱ��������г���1.0 molCO��3.0 molH2O�����ʱCO��ƽ��ת����Ϊ______________��
��1��b��c��f����2����0.03����1����3��75%
��������
�����������1��a�����ݷ�Ӧ����ʽ����֪����Ӧǰ������ϵ��֮����ȣ�˵����Ӧǰ���������ʵ������䣬����ѹǿ�ȵ������ʵ���֮�ȣ�Ҳ����˵�κ�ʱ��ѹǿ����ȣ����ѹǿ������Ϊ�ﵽƽ��ı�־������b�����ݻ�ѧƽ��״̬�Ķ��壺һ�������£����淴Ӧ�У���Ӧ���ʺ�������������Ҹ���ֵ�Ũ�Ȳ����״̬���������c(CO)���䣬����֤����Ӧ�ﵽ��ƽ�⣬��ȷ��c����ͬ���ʵ����ʱ�ʾ�ﵽƽ��ı�־����Ӧ������һ��һ�棬����֮�ȵ���ϵ��֮�ȣ�v��(H2)������H2������������Ӧ������У���H2O�Ƿ�Ӧ�v��(H2O)������H2O�ķ�����У����淴Ӧ���У�H2��H2O��ϵ����ȣ�v��(H2)=v��(H2O)��˵����Ӧ�ﵽ��ѧƽ�⣬��ȷ��d����֪��ʼͶ�����Ƕ��٣�ת�����Ƕ��٣�c(CO2)=c(CO)����˵����Ӧ�ﵽƽ�⣬����e����= ����ֶ������壬���������غ㶨�ɣ���Ӧǰ����������(m����)�������ǵ�������(v����)���Ѳ�����Ϊ�ﵽƽ��ı�־������f��1molH��H���ѣ�1molH2��1molH��H��˵����Ӧ��������H2�ķ�Ӧ���У����淴Ӧ������У�2molH��O����˵����Ӧ������Ӧ������У�1molH2O��2molH��O������2molH��O��1mol��H2O�����ģ����ϡ���������Ϊƽ���־������������ȷ����2���ٸ��ݷ�Ӧ���ʵĶ��壺
����ֶ������壬���������غ㶨�ɣ���Ӧǰ����������(m����)�������ǵ�������(v����)���Ѳ�����Ϊ�ﵽƽ��ı�־������f��1molH��H���ѣ�1molH2��1molH��H��˵����Ӧ��������H2�ķ�Ӧ���У����淴Ӧ������У�2molH��O����˵����Ӧ������Ӧ������У�1molH2O��2molH��O������2molH��O��1mol��H2O�����ģ����ϡ���������Ϊƽ���־������������ȷ����2���ٸ��ݷ�Ӧ���ʵĶ��壺 mol/(L��min)=0.03mol/(L��min)����CO(g)��H2O(g)
mol/(L��min)=0.03mol/(L��min)����CO(g)��H2O(g)  CO2(g)��H2(g)������Ũ�ȱ仯ͼ����֪���ĵ�CO��H2O��Ũ����0.12mol��L��1�������ɵ�CO2��H2��Ũ����0.12mol��L��1��
CO2(g)��H2(g)������Ũ�ȱ仯ͼ����֪���ĵ�CO��H2O��Ũ����0.12mol��L��1�������ɵ�CO2��H2��Ũ����0.12mol��L��1��
K= ����3���¶Ȳ��䣬ƽ�ⳣ�����䣬�跴Ӧ��COΪxmol
����3���¶Ȳ��䣬ƽ�ⳣ�����䣬�跴Ӧ��COΪxmol =1 ,���x=0.75����CO��ת����=
=1 ,���x=0.75����CO��ת����= ��100%=75%��
��100%=75%��
���㣺����ﵽ��ѧƽ��ı�־����ѧ��Ӧ���ʵļ��㡢ƽ�ⳣ�������֪ʶ��
��������� ����1����ѧƽ��״̬���ƶ� ��������

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�����и�һ��ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ��ƶ���
(8��)�����ֽ�������A��B��C������A����ɫ��ӦΪ��ɫ��B��C�dz������������ֽ�������A��B��C��������ס��ҡ���������D��E��F��G��H֮�䷢������ת����ϵ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û�б������

��1��д���������ʵĻ�ѧʽ��F�е����� _________����____________��
��2����Ӧ�۵����ӷ���ʽ__________________
��3��H���ȷֽ��Ĺ�����������B�����µĻ�ѧ����ʽ��_______________________
��4��A��ˮ��Ӧ�����ӷ���ʽ__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������и߶���ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A���ɱ�����Ҫ���մ������ȣ�����ǻ�ѧ��Ӧ�е����ȷ�Ӧ
B�������ڼ��Ȼ��ȼ�����½��еķ�Ӧ�������ȷ�Ӧ
C�������������溸�ӻ��и��������Ҫ����������������������ʱ���ų�������
D�������о�ˮ���ã���������������Ӳˮ������ʹӲˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱���з�̨��������һѧ����ĩ��ϰ��ѧ�Ծ��������棩 ���ͣ�ѡ����
������ʵ����Ӧ�ķ���ʽ����ȷ����
A����Na2S��ȥ��ˮ�е�Hg2+��Hg2+ +S2- === HgS
B��������Һ����ϴ���ۣ�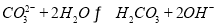
C���������Ȼ���ʱ�������̣�
D�����ҽ���Һ�м������ᡢ˫��ˮ��2I- +2H+ +H2O2=== I2 +2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ɽ��ʡ̩���и߶���ѧ����ĩͳ���߶���ѧ�Ծ��������棩 ���ͣ������
����ͼ���װ�ã�ͼ��Aװ����ʢ1 L 2 mol�� L��1AgNO3��Һ��Bװ����ʢ1L 2 mol��L��1Na2SO4��Һ��ͨ���ʪ���KI������ֽ��C�˱���ɫ�����һ��ʱ����Իش�

��1��A�з�����Ӧ�Ļ�ѧ����ʽΪ___________________________________________��
��2����Bװ���й۲쵽��������____________________________________________��
��3�������£����ӵ�ʼ��ʱ��ΪTʱ��A��Bװ���й��ռ�������0.168L(��״��)����������������������Ӧ����������Һ����仯���Բ��ơ��Լ��㣺Tʱ��Aװ����Һ��c(H+)��д��������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ɽ��ʡ̩���и߶���ѧ����ĩͳ���߶���ѧ�Ծ��������棩 ���ͣ�ѡ����
��Na2S��Һ�У����й�ϵ����ȷ����
A.c(Na+)=2c(HS��)+2c(S2��)+c(H2S)
B.c(Na+)+c(H+)=c(OH��)+c(HS��)+2c(S2��)
C.c(Na+)>c(S2��)>c(OH>c(HS��)
D.c(OH��)=c(HS��)+c(H+)+2c(H2S)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ɽ��ʡ̩���и߶���ѧ����ĩͳ���߶���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ϳɰ��������������ú��ˮ��ԭ�Ͼ��ಽ��Ӧ�Ƶã����е�һ����ӦΪCO(g)+H2O(g) CO2(g)+H2(g) ��H<O����Ӧ�ﵽƽ���Ϊ���CO��ת���ʣ����д�ʩ����ȷ����
CO2(g)+H2(g) ��H<O����Ӧ�ﵽƽ���Ϊ���CO��ת���ʣ����д�ʩ����ȷ����
A������ѹǿ B�������¶� C������CO��Ũ�� D����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ɽ��ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����
A��0.1mol/L�������Һ�и����ӵ�Ũ���ɴ�С��˳���ǣ�c (NH4+)>c(SO42��)>c(H+)>c(OH��)
B�����մ���С�մ�Ļ����Һ�д��ڣ�c(Na+)+c(H+) =c(OH -)+2c(CO32-)+c(HCO3-)
C���ڵ��з�̪��Na2CO3��Һ�У�����BaCl2��Һ���ɫ��ȥ��֤��Na2CO3��Һ�д���ˮ��ƽ��
D�����³�ѹ�����Է����еķ�Ӧ��һ�����Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ɽ��ʡУ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�������
(6��) ʵ������Zn��ϡ���ᷴӦ��ȡ4.48LH2����״����������㣺
��1������Zn��������
��2����ѡ��2.0mol/LH2SO4��������Ҫ�������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com