
| △c |
| △t |
| ||
| 4s |
| 2mol |
| 4mol |
| 4mol |
| 2mol+6mol-4mol |


科目:高中化学 来源: 题型:
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,5LCH4气体与5LNH3气体的原子个数之比为5:4 |
| B、常温常压下,11.2LO3中所含氧原子个数大于1.5×6.02×1023个 |
| C、同温、同压下,相同体积的N2和CO气体具有相同的分子数和相同的密度 |
| D、同温、同压下,等质量的一氧化碳和二氧化碳的密度比为7:11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 杂质 | 所选试剂 | ||
| CO2 | SO2 | |||
| NH3 | H2O | |||
| Cl2 | HCl | |||
| Fe | Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 滴定前读数 | 滴定后读数 |
| 1 | 0.00 | 20.10 |
| 2 | 1.00 | 20.90 |
| 3 | 0.00 | 21.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.
使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.滴定次数 实验数据/mL | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.80 | 15.00 | 15.02 | 14.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
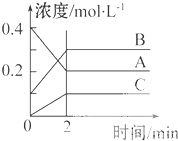 如图所示为800℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( )
如图所示为800℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( )| A、发生的反应可表示为:2A(g)?2B(g)+C(g) |
| B、前2 min A的分解速率为0.1mol?L-1?min-1 |
| C、开始时,正逆反应同时开始 |
| D、2 min时,A、B、C的浓度之比为2:3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
| A、Zn、Zn(OH)2 |
| B、Ag、Ag2O |
| C、Ag2O、Zn |
| D、Zn(OH)2、Ag2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com