
【题目】人造海绵的主要成分是聚氨酯,合成方法如下:
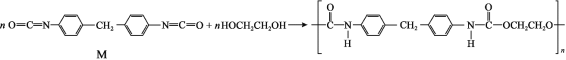
下列说法不正确的是( )
A.M的分子式为C15H10N2O2
B.合成聚氨酯的反应属于缩聚反应
C.聚氨酯在一定条件下可发生水解反应
D.聚氨酯和蛋白质分子中均含有![]() 结构
结构
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】将SO2通入足量Fe2(SO4)3溶液中,完全反应后再加入K2CrO4溶液,发生的两个化学反应为SO2+2Fe3++2H2O=SO42-+2Fe2++W ①,Cr2O72-+aFe2++bH+![]() Cr3++Fe3++H2O ②,下列有关说法正确的是
Cr3++Fe3++H2O ②,下列有关说法正确的是
A. 还原性:Cr3+>SO2 B. 配平后方程式②中,a=6,b=7
C. Cr2O72-能将Na2SO3氧化成Na2SO4 D. 方程式①中W为OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,以0.10mol/LNaOH溶液滴定20.00mL醋酸溶液和20.00mL盐酸,滴定曲线如图所示,下列说法不正确的是
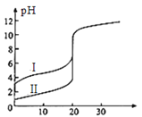
A.曲线Ⅰ、Ⅱ分别表示醋酸溶液和盐酸的滴定曲线
B.达到滴定终点时,两溶液pH均等于7
C.初始时盐酸的浓度为0.10mol/L
D.滴定醋酸溶液、盐酸时,均可选择酚酞溶液做指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验及现象能推出相应结论的是
实验操作及实验现象 | 结 论 | |
A | 向2mL 0.5mol/L FeCl3溶液中滴加2mL 1mol/L KSCN溶液,振荡后静置,观察到溶液变成红色,加入1mL 2mol/L KCl溶液后溶液红色变浅 | c(KCl)增大使该反应[FeCl3+ 3KSCN |
B | 向做了相同标记的2支试管中均加入2mL 0.1mol/L Na2S2O3溶液,再分别向2支试管中加入4mL浓度为0.1mol/L、0.5mol/L 的H2SO4溶液,测定恰好遮挡全部标记所用时间 | 其他条件一定时,反应物浓度越大,化学反应速率越快 |
C | 室温下,用广泛pH试纸测定0.1 mol/L Na2SO3溶液的pH为10,0.1mol/L NaHSO3溶液的pH为5 | 相同条件下,HSO3-的水解能力强于SO32- |
D | 向2 mL0.1mol/LAgNO3溶液中加入1mL0.1mol/LNaCl溶液,生成白色沉淀,再加入1mL0.1mol/L KI溶液,生成黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①Cu ②CO2 ③H2SO3④H2O⑤液态HCl ⑥H2SO4⑦Ba(OH)2 ⑧NaCl ⑨蔗糖 ⑩NaOH溶液
上述物质中属于电解质的是______________,属于非电解质的是________,能导电的是_________。 (填序号,必须填全,否则不得分)
(2)与16g氧气所含原子总数相同的氨气是_________________g。
(3)已知实验室制取氯气的反应原理为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
①该反应中氧化剂和还原剂的物质的量之比为________
②当2 mol MnO2参加反应时转移电子______mol
③当转移1 mol电子时能生成标准状况下的Cl2______L
④浓盐酸在反应中显示出来的性质是______(填字母)
a.还原性 b.酸性 c.氧化性 d. 挥发性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是
A.用玻璃棒搅拌漏斗中的液体以加快过滤速度
B.硅酸钠溶液应保存在带玻璃塞的试剂瓶中
C.蒸馏时蒸馏烧瓶中液体的体积不能超过容积的![]() ,液体也不能蒸干
,液体也不能蒸干
D.分液时,下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行的实验中,不能达到相应实验目的的是
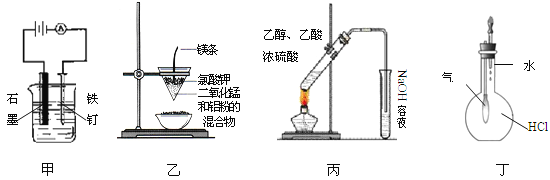
A.装置甲:防止铁钉生锈
B.装置乙:可制得金属锰
C.装置丙:实验室制取乙酸乙酯
D.装置丁:验证HCl气体在水中的溶解性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4溶液滴定H2C2O4溶液,当_________________时,滴定结束。
④记录数据,重复实验。整理数据如下:
实验序号 | V(KMnO4溶液) | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
回答下列问题:
(1)步骤①需要使用烧杯、量筒、玻璃棒,还缺少的玻璃仪器为_______(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为______(填名称)。
(2)该反应原理的化学方程式为_________________;
(3)请将步骤③补充完整__________________;
(4)根据数据,计算H2C2O4溶液的物质的量浓度为______________mol/L,x=____________;
(5)若滴定终点读数时俯视KMnO4溶液液面,则x值会__________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置示意图如图所示。下列说法不正确的是( )

A.燃料电池工作时,正极反应为O2+4H++4e﹣=2H2O
B.a极是铜,b极是铁时,可实现铁上镀铜
C.a极是含锌、铁的粗铜,b极是纯铜,a极溶解铜的质量与b极析出的铜质量相等
D.若a、b两极均为石墨时,在相同条件下,a极产生的气体与电池中消耗的H2体积不相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com