
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A.��Ca(ClO)2��Һ��ͨ�����CO2��ClO-+H2O+CO2=HClO+HCO3-
B.��(NH4)2Fe(SO4)2��Һ�м�������NaOH��Һ��NH4++OH-=NH3��H2O
C.��ͭ�缫���CuSO4��Һ��2Cu2++2H2O![]() 2Cu+O2��+4H+
2Cu+O2��+4H+
D.��Na2S2O3��Һ�еμ�ϡ���S2O32-+2H+=S��+SO2��+H2O
���𰸡�AD
��������
A. ��Ca(ClO)2��Һ��ͨ�����CO2��ClO�� + H2O + CO2 = HClO+HCO3������A��ȷ��
B. ��(NH4)2Fe(SO4)2��Һ�м�������NaOH��Һ�����������ȷ�Ӧ��Fe2+ + 2OH��= Fe(OH)2������B����
C. ��ͭ�缫���CuSO4��Һ������Cuʧȥ��������Cu2+������Cu2+�õ���������Cu����C����
D. ��Na2S2O3��Һ�еμ�ϡ���S2O32�� + 2H+ = S��+SO2��+H2O����D��ȷ��
������������ΪAD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л����������ȷ����
A.  3������2���һ�����
3������2���һ�����
B. (CH3)3CCH2CH(C2H5)CH32��2��������4���һ�����
C. ![]() �ڼ�����
�ڼ�����
D. ![]() 2������3����Ȳ
2������3����Ȳ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2008��10��8�գ����ʼҿ�ѧԺ������ŵ������ѧ�������ձ���ѧ���´��ޡ�������ѧ������ɳ���������������ѧ��Ǯ�������Ա����������ڷ��ֺ��о���ɫӫ�⵰���������Ĺ��ס���������һ�ิ�ӵĺ��������ÿ�ֵ����ʶ�����㶨�ĺ�����[Լ��14%��18%�������漰�ĺ�����Ϊ����������]����ʳƷ�е����ʵĺ����ⶨ���ÿ��϶���������ⶨԭ���ǣ�
�������еĵ����ð�����ʾ����ǿ�Ⱥ�CuSO4��ŨH2SO4�����£�����һ���������������ӦʽΪ��2����NH2��+H2SO4+2H+![]() ��
��
�����������ڿ��϶�������������ã�ͨ�������ͷų�NH3���ռ���H3BO3��Һ�У����ɣ�NH4��2B4O7��
������֪Ũ�ȵ�HCl����Һ�ζ�������HCl���ĵ�����������ĺ�����Ȼ�������Ӧ�Ļ���ϵ�������õ����ʵĺ�����
��1������ԭ���ڢ����ɵ������������ﻯѧʽΪ_________��
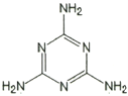
��2������Ʒ�Ļ���ϵ��Ϊ6.38�������������ĺ���Ϊ1%�������ʵĺ�����Ϊ6.38%����������ͨ���ڵ͵��������̷��м��������谷��Melamine��������ߡ��̷��еĵ����ʺ�������������Ӥ������ʯ��
�������谷�Ľṹ��ͼ��ʾ���仯ѧʽΪ_________������������Ԫ�ص�����������Ϊ_________��
�����й��������谷��˵���У���ȷ����_________��
A�������谷��һ�ְ�ɫ�ᾧ��ĩ����ɫ��ζ�����Բ����̷ۺ��ױ�����
B�������谷����������ԭ�ӿ�����ͬһ��ƽ����
C�������谷�������ԣ����Ժ��ᷴӦ������Ӧ����
�ۼٶ��̷��е����ʺ���Ϊ16%��Ϊ�ϸ���������һ��������Ϊ500g�������ʺ���Ϊ0�ļ��̷��в���_________g�������谷�Ϳ�ʹ�̷ۡ���ꡱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������![]() ������ɱ�����ͨ��������Ϊ��ɫҺ�壬�۵�Ϊ
������ɱ�����ͨ��������Ϊ��ɫҺ�壬�۵�Ϊ![]() ���е�Ϊ
���е�Ϊ![]() ���ڳ�ʪ����������������
���ڳ�ʪ����������������![]() ���Ͽ�ʼ�ֽ⣬���ɶ�����������������ڷ���Ҳ�ɷֽ⣬�Ʊ�ʱ�Ի���̿Ϊ��������Ӧ���Ȼ�ѧ����ʽΪ
���Ͽ�ʼ�ֽ⣬���ɶ�����������������ڷ���Ҳ�ɷֽ⣬�Ʊ�ʱ�Ի���̿Ϊ��������Ӧ���Ȼ�ѧ����ʽΪ![]()
![]() ������װ����ͼ��ʾ�����������������
������װ����ͼ��ʾ�����������������![]()

A.����������BӦ��a�ڽ�ˮb�ڳ�ˮ
B.��ͨ���۲�D��E�����ݲ������ʿ���ͨ��A�е�![]() ��
��![]() �������
�������
C.����C��D��E��ʢ�ŵ��Լ�����Ϊ��ˮ�Ȼ��ơ�Ũ���ᡢŨ����
D.���ڷ��õ�������Һ��ᷢ�Ƶ�ԭ�����ܽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���׳ص��ܷ�ӦʽΪ��N2H4+O2=N2+H2O�����й��ڸõ�ع���ʱ��˵����ȷ������ ��

A. ��װ�ù���ʱ��Ag�缫������������
B. �׳��и�����ӦΪN2H4-4e-=N2+4H+
C. �׳غ��ҳ��е���Һ��pH����С
D. ���׳�������0.1molN2H4ʱ���ҳ���������������6.4g����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȩ������ˮ�����Ա����Ƶ�![]() �������������õ��������ϣ�
�������������õ��������ϣ�
����1��HCHO+Cu(OH)2![]() Cu+CO��+2H2O��
Cu+CO��+2H2O��
����2��HCHO+4Cu(OH)2+2NaOH![]() 2Cu2O��+Na2CO3+6H2O��
2Cu2O��+Na2CO3+6H2O��
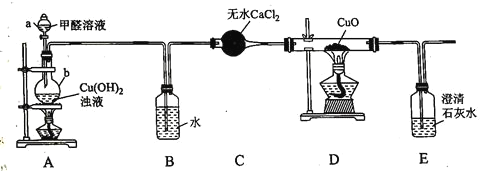
������ͼ��ʾװ�ý������Ƶ�![]() ������ȩ��Һ��ʵ�飬���Բ��ֲ�����м��顣
������ȩ��Һ��ʵ�飬���Բ��ֲ�����м��顣
��֪����![]() ���Լ�Ϊ
���Լ�Ϊ![]() ��Һ��
��Һ��![]() ��Һ����Ƴɵ���Һ��
��Һ����Ƴɵ���Һ��
��![]() ��ȩ��Һ������
��ȩ��Һ������
��![]() ��ɫ
��ɫ![]() ��ɫ
��ɫ![]() ��
��
��![]() ��ɫ
��ɫ![]() ��
��
�ش��������⣺
(1)����b������Ϊ__________�����װ��A�������ԵIJ�������Ϊ______��װ��B������Ϊ__________��
(2)ʵ�鿪ʼ��Ӧ�ȵ�ȼ________![]() ����A������D��
����A������D��![]() ���ƾ��ƣ�װ��A����ʱ�¶Ȳ��˹��ߣ�������ܲ����IJ��������___________
���ƾ��ƣ�װ��A����ʱ�¶Ȳ��˹��ߣ�������ܲ����IJ��������___________![]() ��дһ��
��дһ��![]() ��
��
(3)֤�������к���CO��ʵ������Ϊ_____������װ�õ�����д��ڵ�ȱ��Ϊ_______��
(4)ȡװ��A�����ɵĺ�ɫ�������Թ��У���������ʵ�飺
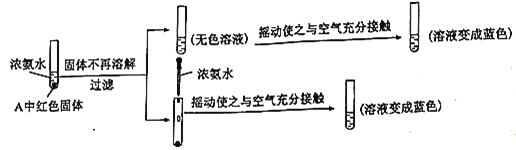
����֤����ɫ�����к���![]() ��ʵ������Ϊ______________��
��ʵ������Ϊ______________��
�ڹ��˺�ĺ�ɫ������Ũ��ˮ�ڿ����г��ҡ��������Ӧ�����ӷ���ʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����SO3��˵����ȷ���ǣ� ��
A. �ṹ��NH3���� B. �ṹ��SO2����
C. �ṹ��BF3���� D. �ṹ��P4����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£��ܱ������з�����ӦaX(g)![]() bY(g)��cZ(g)���ﵽƽ������¶Ȳ��䣬���������ݻ�ѹ����ԭ���ݻ���һ�룬���ﵽ��ƽ��ʱ������Y��Z��Ũ�Ⱦ���ԭ����1.8����������������ȷ����(����)
bY(g)��cZ(g)���ﵽƽ������¶Ȳ��䣬���������ݻ�ѹ����ԭ���ݻ���һ�룬���ﵽ��ƽ��ʱ������Y��Z��Ũ�Ⱦ���ԭ����1.8����������������ȷ����(����)
A.���淴Ӧ�Ļ�ѧ����ʽ�Ļ�ѧ��������a��b��c
B.ѹ���������ݻ�ʱ��v������v����С
C.�ﵽ��ƽ��ʱ������X��ת���ʼ�С
D.�ﵽ��ƽ��ʱ���������Z��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������͡G��һ�����������Ծ����ϰ���ҩ���һ�ֺϳ�·����ͼ��

��֪��LiAIH4��ǿ��ԭ���������ܻ�ԭȩ��ͪ�����ܻ�ԭ�������ɱ��ϸߡ�
�ش��������⣺
��1��̼ԭ��������4����ͬ��ԭ�ӻ����ʱ����̼��Ϊ����̼��д��D�Ľṹ��ʽ�����Ǻţ�*�����D�е�����̼___��
��2���ܵķ�Ӧ������___��
��3��C�Ľṹ��ʽΪ___��
��4��G�ķ���ʽΪ___��
��5����Ӧ�ݵĻ�ѧ����ʽΪ___��
��6����֪M��D��Ϊͬ���칹�壬��һ�������������Ȼ�����Һ������ɫ��Ӧ��M���ӵı�������3��ȡ����������������ͬ������������M��__�֡�
��7�� Ҳ��һ����������͡���м��壬�����
Ҳ��һ����������͡���м��壬�����![]() ��
��![]() Ϊ��Ҫԭ���Ʊ����ĺϳ�·��___�����Լ���ѡ����
Ϊ��Ҫԭ���Ʊ����ĺϳ�·��___�����Լ���ѡ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com