
【题目】工业上用铝土矿(主要成分Al2O3、Fe2O3、SiO2)提取氧化铝作冶炼铝的原料,提取的操作过程如下:
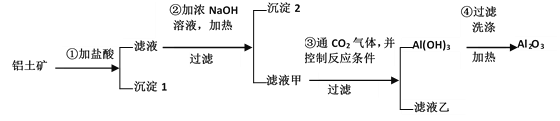
(1)写出步骤①中所发生反应的化学方程式____
(2)沉淀1是_________(写化学式);沉淀2是________(写化学式)。
(3)写出步骤②中所发生反应的离子方程式__________
(4)用氧化铝冶炼铝的化学方程式是______
(5)请设计另一个实验方案提取氧化铝________
【答案】Al2O3+6HCl=2AlCl3+3H2O、Fe2O3+6HCl=2FeCl3+3H2O SiO2 Fe(OH)3 Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=[Al(OH)4]- 2Al2O3![]() 4Al +3O2 ↑ ①为氢氧化钠时,则在①得到滤液中含有偏铝酸根离子、硅酸根离子,滤渣为氧化铁;②为盐酸,除去硅酸根离子,将偏铝酸根离子转化为铝离子,进入②得到滤液;试剂③为氨水,将铝离子转化为氢氧化铝沉淀,加热分解得氧化铝。
4Al +3O2 ↑ ①为氢氧化钠时,则在①得到滤液中含有偏铝酸根离子、硅酸根离子,滤渣为氧化铁;②为盐酸,除去硅酸根离子,将偏铝酸根离子转化为铝离子,进入②得到滤液;试剂③为氨水,将铝离子转化为氢氧化铝沉淀,加热分解得氧化铝。
【解析】
①为盐酸则在①得到滤液中含有铝离子、铁离子,滤渣(沉淀1)为二氧化硅;在滤液中加入浓氢氧化钠溶液并加热,除去铁离子,将铝离子转化为偏铝酸根,过滤得到沉淀2和滤液甲,则推出沉淀2为氢氧化铁,滤液甲为偏铝酸钠;向滤液甲中通入二氧化碳,将偏铝酸根转化为氢氧化铝沉淀,同时生成碳酸氢钠或碳酸钠溶液,得到的氢氧化铝沉淀再通过过滤洗涤加热分解得氧化铝,据此分析作答。
根据上述工艺流程分析可知,
(1)步骤①中氧化铝与氧化铁均会被盐酸溶解,所发生反应的化学方程式分别为Al2O3+6HCl=2AlCl3+3H2O、Fe2O3+6HCl=2FeCl3+3H2O;
(2)沉淀1是SiO2;沉淀2是Fe(OH)3;
(3)步骤②为氯化铁与氢氧化钠反应生成沉淀,同时氯化铝与氢氧化钠反应生成偏铝酸钠与水的过程,所发生反应的离子方程式为:Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=[Al(OH)4]-(或Al3++4OH-=AlO2-+2H2O);
(4)工业上通过冶炼氧化铝可得到铝单质,其化学方程式为:2Al2O3![]() 4Al +3O2 ↑;
4Al +3O2 ↑;
(5)氧化铝是两性氧化物,既溶液强酸又溶于强碱,而Fe2O3只溶于强酸,不溶于碱,SiO2只溶于强碱,不溶于酸。上述工艺流程若①为氢氧化钠时,则在①得到滤液中含有偏铝酸根离子、硅酸根离子,滤渣为氧化铁;②为盐酸,除去硅酸根离子,将偏铝酸根离子转化为铝离子,进入②得到滤液;试剂③为氨水,将铝离子转化为氢氧化铝沉淀,加热分解得氧化铝。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】聚合硫酸铁[Fex(OH)y(SO4)z](铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:①称取一定质量的聚合硫酸铁配成100.00 mL的溶液。②准确量取25.00 mL溶液,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体6.99g。③准确量取25.00mL溶液,加入足量的NaOH溶液至沉淀完全,过滤、洗涤、干燥、灼烧至恒重,得到红棕色固体1.92g。该聚合硫酸铁组成中x∶y∶z的值为
A. 6∶8∶5 B. 4∶2∶5 C. 1∶1∶2 D. 6∶3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.金属冶炼与处理中常涉及离子反应和氧化还原反应。
(1)实验室常用无水乙醇处理少量残留的金属钠,写出反应的化学方程式_________。
(2)镁与碳在加强热时可生成易水解的MgC2,其水解的化学方程式为________。
(3)我国古代劳动人民曾利用明矾溶液除去铜器表面的铜锈[Cu2(OH)2CO3],请简要解释其原理:_______。
Ⅱ.(4)0.1 mol·L-1NaHCO3溶液与0.1 mol·L-1NaOH溶液等体积混合,所得溶液中离子浓度由大到小的顺序是:______________。
(5)恒温恒容条件下,在密闭容器中通入等物质的量的CO2和H2,发生反应CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。下列描述能说明该反应达到平衡状态的是_____(填序号)。
CH3OH(g)+H2O(g)。下列描述能说明该反应达到平衡状态的是_____(填序号)。
A 容器内的混合气体的平均相对分子质量保持不变
B 水分子中断裂2NA个H-O键,同时氢分子中生成3NA个H-H键
C CH3OH和H2O的浓度保持不变
D 容器内的混合气体的密度保持不变
(6)现有反应CH3OCH3(g)+H2O(g) ![]() 2CH3OH(g) △H=+23.4 kJ/mol,在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到10min时测得各组分浓度如下:
2CH3OH(g) △H=+23.4 kJ/mol,在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到10min时测得各组分浓度如下:
物质 | CH3OCH3(g) | H2O(g) | CH3OH(g) |
浓度/mol·L-1 | 0.9 | 0.9 | 1.2 |
此时v正_______v逆(填“>”、“<”或“=”),v (CH3OH) =_______;当反应达到平衡状态时,混合气体中CH3OCH3体积分数(CH3OCH3)%=______%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废水中过量的氨氮(![]() 和
和![]() )会导致水体富营养化。某科研小组用
)会导致水体富营养化。某科研小组用![]() 氧化法处理氨氮废水。已知:①
氧化法处理氨氮废水。已知:①![]() 的氧化性比
的氧化性比![]() 强;②
强;②![]() 比
比![]() 更易被氧化;③国家相关标准要求经处理过的氨氮废水
更易被氧化;③国家相关标准要求经处理过的氨氮废水![]() 要控制在6~9 。
要控制在6~9 。
(1)![]() 时,
时,![]() 可与
可与![]() 反应生成
反应生成![]() 等无污染物质,该反应的离子方程式为___________。
等无污染物质,该反应的离子方程式为___________。
(2)进水![]() 对氨氮去除率和出水pH的影响分别如图1和图2所示:
对氨氮去除率和出水pH的影响分别如图1和图2所示:
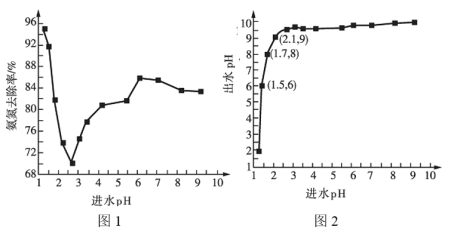
①进水![]() 在1.25~2.75范围内时,氨氮去除率随
在1.25~2.75范围内时,氨氮去除率随![]() 的升高迅速下降的原因是__________。
的升高迅速下降的原因是__________。
②进水![]() 在2.75~6范围内时,氨氮去除率随
在2.75~6范围内时,氨氮去除率随![]() 的升高而上升的原因是___________。
的升高而上升的原因是___________。
③进水![]() 应控制在____________左右为宜。
应控制在____________左右为宜。
(3)为研究空气对![]() 氢化氨氮的影响,其他条件不变,仅增加单位时间内通人空气的量,发现氨氮去除率几乎不变。其原因可能是______(填序号)
氢化氨氮的影响,其他条件不变,仅增加单位时间内通人空气的量,发现氨氮去除率几乎不变。其原因可能是______(填序号)
a.![]() 的氧化性比
的氧化性比![]() 弱
弱
b.![]() 氧化氨氮速率比
氧化氨氮速率比![]() 慢
慢
c.![]() 在废水中溶解度比较小
在废水中溶解度比较小
d.空气中的![]() 进入废水中
进入废水中
查看答案和解析>>
科目:高中化学 来源: 题型:
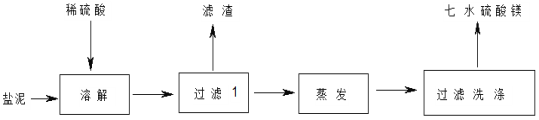
【题目】“盐泥”是氯碱工业中产生的。盐泥中含 NaCl(15%~20%)、Mg(OH)2(15%~20%)、
CaCO3(15%~20%)和BaSO4 等不溶于酸的物质。用“盐泥”生产七水硫酸镁,设计了如下工艺流程:
(1)电解食盐水前,为除去粗食盐水中的 Mg2+、Ca2+、SO42-等杂质离子,下列试剂加入的先后顺序合理的是_____(填序号)。
A.碳酸钠溶液 B.氢氧化钠溶液 C.氯化钡溶液 D.盐酸
(2)已知Ksp[Mg(OH)2]=6.0×10-12。设食盐水中 Mg2+的浓度为 0.06 mol·L-1,则加入氢氧化钠溶液后使溶液的 pH≥_____才可能产生 Mg(OH)2 沉淀。
(3)氯碱工业上电解食盐水阴极发生的反应是_____。
(4)三种化合物的溶解度(S)随温度变化曲线见下图

在“过滤Ⅰ” 中需要趁热过滤,其主要原因是_________;滤渣的主要成分有不溶于酸的物质、_________。
(5)检验 MgSO4·7H2O 中杂质是否洗涤干净的操作是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如右图,下列说法正确的是
5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如右图,下列说法正确的是

A. b点时,CO的转化率为20%
B. 容器内的压强保持恒定,表明反应达到平衡状态
C. b点和d点的化学平衡常数:Kb>Kd
D. 0到0.5min反应速率v(CO)=0.3mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A的相对分子质量为84。回答下列问题:
(1)烃A的分子式为_________。下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是_____;若总质量一定,充分燃烧消耗氧气的量不变的是____。
A. C7H8 B.C6H14 C.C7H14 D.C8H8
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。则A的结构简式为__________。若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为__________ 。若烃B的相对分子质量比烃A小6,且B为最简单芳香族化合物,写出B与浓硝酸,浓硫酸混合共热的化学方程式__________
(3)如图:

①该物质与足量氢气完全加成后环上一氯代物有________种;
②该物质和溴水反应,消耗Br2的物质的量为_______mol;
③该物质和H2加成需H2________mol;
(4)如图是辛烷的一种结构M(只画出了碳架,没有画出氢原子)按下列要求,回答问题:

①用系统命名法命名________。
②M的一氯代物有________种。
③M是由某烯烃加成生成的产物,则该烯烃可能有_______种结构。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某工厂废水中含游离态氯,通过下列实验测定其浓度。
①取水样10.0 mL于锥形瓶中,加入10.0 mL的KI溶液(足量),发生的反应为:Cl2+2KI=2KCl+I2,滴入指示剂2~3滴。
②取一滴定管依次用自来水、蒸馏水洗净后,再用0.01mol·L-1 Na2S2O3溶液润洗,然后装入0.01mol·L-1 Na2S2O3溶液到0刻度以上,排出下端尖嘴内的气泡,调整液面至0刻度或0刻度下某一位置,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+ 2Na2S4O6。试回答下列问答:
(1)步骤①加入的指示剂是_______________________________。
(2)步骤②应使用________式滴定管。
(3)判断达到滴定终点的实验现象是___________________________________。
Ⅱ.(4)若用0.1032 mol/L HCl溶液滴定未知浓度的NaOH溶液,下列情况对实验结果无影响的是____________。
A.酸式滴定管未用标准盐酸溶液润洗
B.锥形瓶未用待测液润洗
C.滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了
D.滴定时将标准液溅出锥形瓶外
(5)碳酸H2CO3,K1=4.3×10-7,K2=5.6×10-11,草酸H2C2O4 K1=5.9×10-2,K2=6.4×10-5。0.1 mol/L Na2CO3溶液的pH____________0.1 mol/L Na2C2O4溶液的pH(选填“大于”、“小于”或“等于”)。若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____________。
A.c(H+)>c(HC2O4-)>c(HCO3-)>c(CO32-)
B.c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
C.c(H+)>c(HC2O4-)>c(C2O42-)>c(CO32-)
D.c(H2CO3) >c(HCO3-)>c(HC2O4-)>c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。

(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是__________。
②称取样品,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为________、________。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是_______________。
②E处干燥管中盛放的药品是碱石灰,其作用是_____________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量_____________(填“偏大”“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1g、m2g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com