
【题目】有甲基、苯基、羟基、羧基四种基团,在它们两两组合形成的化合物中:
(1)能使石蕊试液变色的是_______________(只需写出一种物质的结构简式,下同);
(2)能与溴水反应的是____________;
(3)催化氧化后产物能与新制氢氧化铜反应的是_________________;
(4)能与氯化铁溶液反应的是__________________________;
(5)不同情况下与氢氧化钠反应能生成两种盐的是_______________。
【答案】CH3COOH(或C6H5COOH或HO-COOH) ![]() CH3OH
CH3OH ![]() HOCOOH
HOCOOH
【解析】
甲基、苯基、羟基、羧基四种基团两两组合对应的有机物有CH3COOH、![]() 、H2CO3、
、H2CO3、![]() 、CH3OH等,结合有机物官能团的性质分析解答。
、CH3OH等,结合有机物官能团的性质分析解答。
甲基、苯基、羟基、羧基四种基团两两组合对应的有机物有CH3COOH、![]() 、H2CO3、
、H2CO3、![]() 、CH3OH等。
、CH3OH等。
(1)能使石蕊试液变色的物质具有酸性,对应的有CH3COOH、![]() 、HO-COOH(H2CO3),苯酚不能使石蕊变色,故答案为:CH3COOH(或
、HO-COOH(H2CO3),苯酚不能使石蕊变色,故答案为:CH3COOH(或![]() 或HO-COOH);
或HO-COOH);
(2)能与溴水反应的是![]() ,与溴水发生取代反应生成三溴苯酚沉淀,故答案为:
,与溴水发生取代反应生成三溴苯酚沉淀,故答案为:![]() (或C6H5OH);
(或C6H5OH);
(3)催化氧化后产物能与新制氢氧化铜反应,说明产物中含有-CHO,只有CH3OH符合,故答案为:CH3OH;
(4)能与氯化铁溶液发生显色反应的是![]() ,反应后溶液显紫色,为
,反应后溶液显紫色,为![]() 的特征反应,故答案为:
的特征反应,故答案为:![]() ;
;
(5)不同情况下与氢氧化钠反应能生成两种盐的是HOCOOH(H2CO3),可生成Na2CO3或NaHCO3,故答案为:HOCOOH。


科目:高中化学 来源: 题型:
【题目】如图是两个氢原子相互接近时的能量变化图,则有关该图的说法正确的是( )
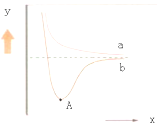
A.y代表两原子之间的核间距
B.x代表体系具有的能量
C.a代表核外电子自旋相反的两个氢原子能量变化
D.A点时表示两原子间形成了稳定的共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科学技术的发展,阿伏加德罗常数的测定手段越来越多,测定精确度也越来越高,现有一种简单可行的测定方法,具体步骤为:
(1)将固体NaCl研细、干燥后,准确称取mgNaCl固体并转移到定容仪器A中。
(2)用滴定管向A仪器中滴加苯,不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为Vcm3。
①步骤(1)中A仪器最好用__________(仪器名称)。
②步骤(2)中用酸式滴定管好还是碱式滴定管好,__________,理由是______________。
③能否用胶头滴管代替步骤(2)中的滴定管__________;理由是____________________。
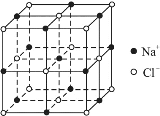
④已知NaCl晶体的结构如上图所示,用X射线测得NaCl晶体中靠得最近的Na+与Cl-间的平均距离为acm,则用上述测定方法测得阿伏加德罗常数NA的表达式为:NA=______mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种氧化镍NiO晶体中就存在如下图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但此化合物中Ni和O的比值却发生了变化。某氧化镍样品组成中个数比Ni∶O=97∶100
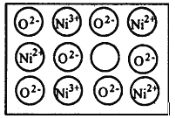
(1)写出该氧化镍样品的化学式_________________。
(2)试计算晶体中Ni2+与Ni3+的离子个数之比__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中可能大量含有的离子如下表所示:
阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
阴离子 | Cl-、OH-、CO32-、AlO2- |
为探究其成分,某同学将Na2O2逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系分别如图所示。

(1)该溶液中一定含有的阳离子是________________________________,其对应物质的量浓度之比为 ____________,溶液中一定不存在的阴离子是_______________________。
(2)写出沉淀减少的离子方程式 ________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第16届海南国际车展上:展出了中国研制的新型燃料电池汽车,该车装有“绿色心脏”---质子交换膜燃料电池。某种质子交换膜燃料电池如图所示。下列说法正确的是
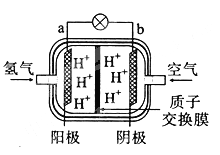
A.该电池的a极发生氧化反应B.正极反应为:O2+4e-+2H2O=4OH-
C.质子(H+)通过质子交换膜移动到a电极D.该燃料电池的能量转化率可达到100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于恒容密闭容器中发生的可逆反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,能说明反应达到化学平衡状态的为( )
2NH3(g) ΔH<0,能说明反应达到化学平衡状态的为( )
A.断开一个N≡N键的同时有6个N—H键生成
B.混合气体的密度不变
C.混合气体的平均相对分子质量
D.N2、H2、NH3分子数比为1∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表中短周期的下列内容回答问题:
H | ① | ||||||
② | ③ | O | ④ | ||||
⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素①~⑨形成的单质中,化学性质最稳定的是_____(填化学式)。④在元素周期表中的位置是________,⑥的简单离子的结构示意图为________________
(2)③、⑨和H元素可形成一种常见的盐,其中存在的化学键类型为________________,⑤、⑧按原子个数比2:1形成的化合物的电子式为________________
(3)写出一个可证明②和⑦非金属性强弱的离子方程式:________________
(4)在酸性溶液中,②的简单氢化物与O2组成燃料电池,其负极的电极反应式为________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是
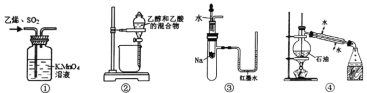
A.用装置①除去C2H4中少量SO2B.用装置②分离乙醇和乙酸的混合物
C.用装置③验证Na和水反应为放热反应D.用装置④分馏石油并收集60~ 150℃馏分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com